Clear Sky Science · ar
الأصول والموائل المميزة تحدد استجابة البلاعم الخلوية في الجهاز العصبي المركزي بعد إعادة التجدد
لماذا يهُمّ حراس حدود الدماغ
أدمغتنا ليست مكوَّنة من خلايا عصبية فقط. فهي أيضاً مكان تجوال لخلايا مناعية تجلس إما داخل النسيج نفسه أو على حدوده، حيث يلتقي الدماغ بأغشيته الواقية والأوعية الدموية. تستعرض هذه الدراسة كيف تختفي مجموعات مختلفة من هذه الحراس المناعيين ثم تنمو مجدداً، وتظهر أن طريقة استبدالها يمكن أن تغيّر كيفية استجابة الدماغ للالتهاب والسكتة. فهم هذا التجدد يفتح الباب أمام علاجات تعدّل خلايا الحدود المناعية دون المساس ببقية الدماغ.
أحياء مختلفة، حراس دماغيون مختلفون
تشغل خلايا مناعية تُسمى البلاعم أحياءً مميزة داخل الجهاز العصبي المركزي. تعيش الخلايا النجمية الصغيرة داخل نسيج الدماغ نفسه، بينما تجلس ما يُسمى ببلاعم الحدود على أسطح الدماغ وحول الأوعية الدموية. ضمن هذه الخلايا الحدّية، تقع البلاعم تحت الجافية مباشرة فوق نسيج الدماغ، محيطة بالمساحات السحائية والمساحات المحيطة بالأوعية، في حين تستوطن مجموعة أخرى الغشاء الخارجي المتين المسمى الجافية. وعلى الرغم من أن هذه المجموعات جميعها تساهم في مراقبة وتشكيل الاستجابات المناعية في الدماغ، إلا أن لها أصولاً وأعماراً مختلفة، وكانت أعمال سابقة تشير إلى أن الخلايا النجمية الصغيرة تستطيع المحافظة على نفسها محلياً دون مساعدة من خلايا سائلة في الدم.
إعادة ضبط النظام ومراقبة نموه من جديد
لمعرفة كيف تتعافى كل مجموعة بلاعم بعد القضاء عليها، استخدم الباحثون دواءً يعرقل إشارة بقاء رئيسية ويؤدي مؤقتاً إلى نضوب هذه الخلايا في الفئران. ثم تتبعوا كيف ومن أين عادت الخلايا باستخدام مزيج من فئران ذات «بصمة» جينية فريدة، وتسلسل RNA الخلوي المفرد، وبروفايل الكروماتين والمجهر عالي الدقة. استعادت الخلايا النجمية الصغيرة في نسيج الدماغ توازنها بسرعة وبشكل شبه كامل عن طريق الانقسام من بين الناجين النادرين الذين نجوا من النضوب، ولم يظهر أي دليل على أن خلايا مناعية دموية تنفذت لتحلّ مكانها. في المقابل، أعيدت تعبئة البلاعم تحت الجافية على السطح الدماغي ببطء وبشكل غير متكافئ عبر المناطق، ما يلمّح إلى أنها كانت تستمد مصادر إضافية تتجاوز الخلايا المقيمة الأصلية. 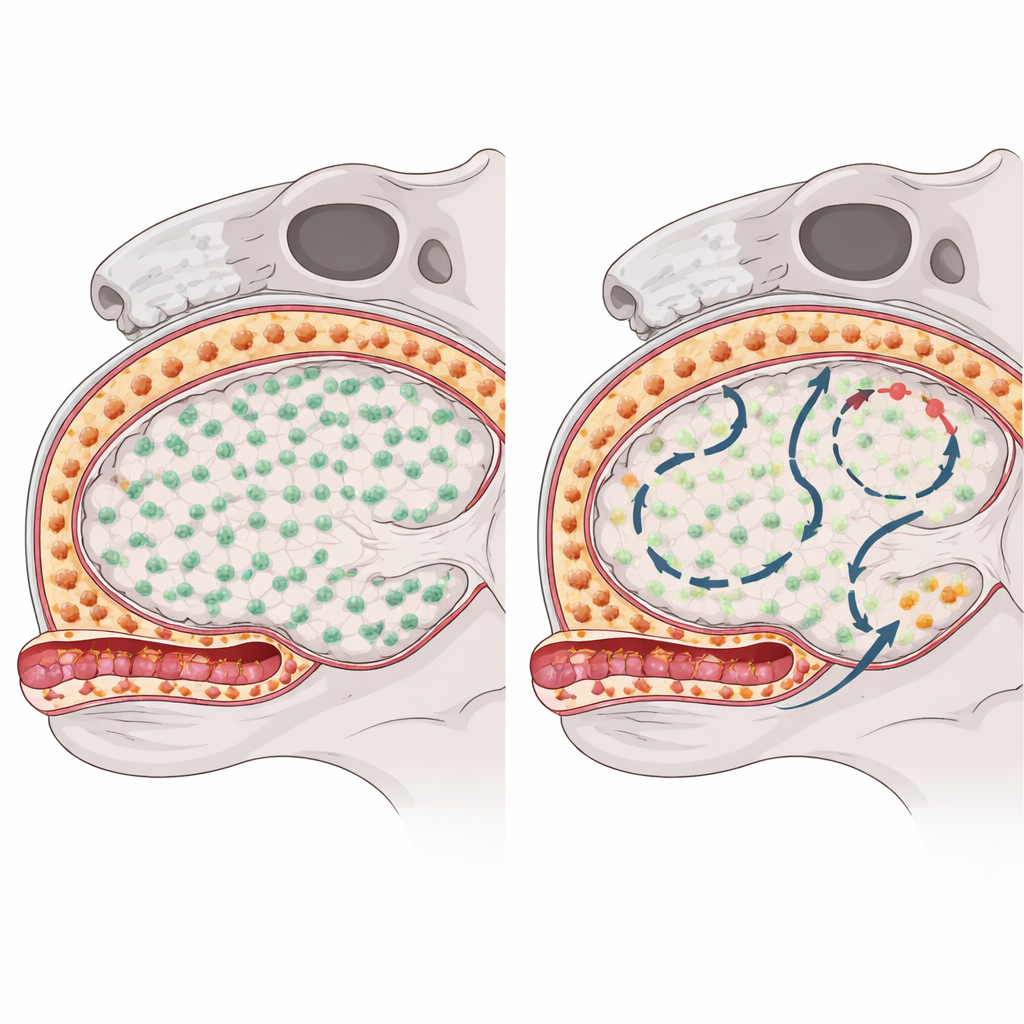
عندما تتحرك خلايا الدم وتستقر
أظهرت تجارب تتبع المصير أنه، على عكس الخلايا النجمية الصغيرة، أعادت البلاعم تحت الجافية ملء مواطنها جزئياً باستخدام الوحيدات النواة قصيرة العمر المتداولة في الدم. بعد النضوب، خلقت إشارات من الخلايا الوعائية والخلايا البينية نافذة مؤقتة مكنت هذه الوحيدات من الالتصاق بجدران الأوعية المُنشطة، والزحف عبرها بمساعدة جزيئات التصاق مثل ICAM‑1 وVCAM‑1، والاستقرار في المواضع المحيطة بالأوعية وعلى السطح. أدى حجب هذه المسارات الالتصاقية إلى تقليل عدد الخلايا الداخلة، مما أكد أهميتها. ومتى ما استوطنت، لم تُقلّد البلاعم الحدودية المشتقة من الوحيدات النواة ببساطة الخلايا المولودة في الجنين: احتفظت بنمط تعبيري جيني ونمط كروماتيني مميز، وازدانت بجزيئات متورطة في عرض المستضدات والتصاق الخلايا، وظلت جزءاً ثابتاً من التجمع لفترة طويلة بعد شفاء الإصابة الظاهرية.
إعادة تشكيل دائمة للمناعة الحدّية
كشف التسلسل الخلوي المفرد والتسلسل الشامل أن الخلايا النجمية الصغيرة استعادت إلى حد كبير ملفها الجزيئي الأصلي بعد إعادة التجدد، مع تغيّرات طويلة الأمد طفيفة. أما البلاعم تحت الجافية فقد انقلبت بشكل دائم نحو صنف أكثر «يقظة» يعبر عن مستويات أعلى من جينات التفعيل المناعي. من خلال فصل الخلايا المولودة في الجنين وتلك المشتقة من الوحيدات النواة باستخدام وسوم جينية، أظهر الفريق أن الأصل التطوري شكل بقوة نشاط الجينات والمناطق DNA القابلة للوصول في هذه الخلايا. حملت البلاعم الحدّية المشتقة من الوحيدات علامات إبجينية نمطية للخلايا الدموية حديثة التمايز وبدت أكثر انفتاحاً على الجينات المشاركة في استشعار الممرضات والتفاعل مع خلايا مناعية أخرى. وعندما تعرضت الحيوانات لمكونات بكتيرية، أبدت هذه الخلايا القادمة استجابات التهابية وإجهادية أقوى من جيرانها المولودين في الجنين، بينما كانت تفاعلات الخلايا النجمية الصغيرة وبلاعم الجافية أقل تغيراً بكثير. 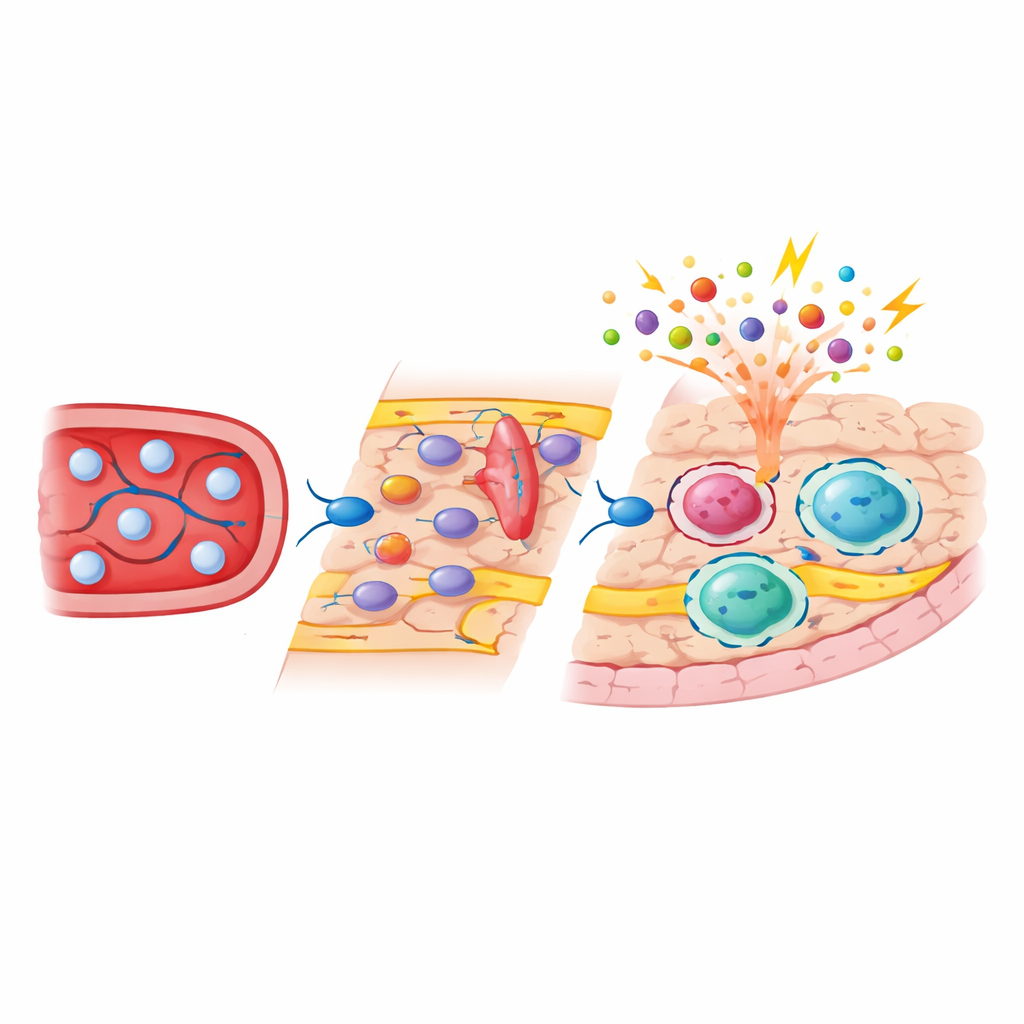
عواقب على السكتة وصحة الدماغ
سأل المؤلفون بعد ذلك ما إذا كان هذا إعادة التشكيل الخفية لبلاعم الحدود يؤثر في المرض. في نموذج للسكتة الإقفارية، أدت إعادة تجدد البلاعم تحت الجافية إلى أداء سلوكي أسوأ لدى الفئران، رغم أن حجم الآفة وإعادة فتح الأوعية الدموية كانت متشابهة مع الضوابط. أظهر تحليل النسيج الكامل وبلاعم الحدود المعزولة تحفيزاً أقوى لجينات مرتبطة بالالتهاب، والأنواع التفاعلية من الأكسجين، واضطراب الحاجز الدماغي الوعائي في الحيوانات المعاد تجددها. كانت الخلايا الحدّية المشتقة من الوحيدات النواة شديدة التفاعل على نحو خاص، منتجة مزيداً من الكيماكائن وعلامات التفعيل بعد السكتة. وأكد تصوير تنشيط الأوعية الدموية إشارة أعلى لـ P‑selectin، وهو مؤشر على التهاب وعائي مكثف، والذي ارتبط بتعافٍ حركي أسوأ.
ماذا يعني هذا للعلاجات المستقبلية
تُظهر هذه الدراسة أن ليس كل البلاعم الدماغية متساوية، وأن استبدالها لا يعيد النظام ببساطة إلى حالته الأصلية. تستطيع الخلايا النجمية الصغيرة إعادة بناء نفسها بهدوء من الخلايا الناجية والعودة إلى العمل كالمعتاد. بالمقابل، تتحول بلاعم حدود الدماغ السطحية إلى مزيج دائم من خلايا مولودة في الجنين ووصلات جديدة من الدم، وهذا التجمع المختلط يستجيب بشكل أكثر عدوانية للالتهاب الجهازي والسكتة. وبما أن الباحثين طوروا وسيلة لاستبدال هذه الخلايا الحدّية بشكل انتقائي مع الحفاظ على الخلايا النجمية الصغيرة، فإن نتائجهم تشير إلى مستقبل يمكن فيه للعلاجات ضبط حدود مناعة الدماغ بدقة — إما لتهدئة الالتهاب الضار في اضطرابات مثل السكتة والتنكس العصبي أو لتعزيز الاستجابات الوقائية — دون تعطيل الشبكة المناعية الداخلية للدماغ بشكل عام.
الاستشهاد: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
الكلمات المفتاحية: بلاعم حدود الدماغ, إعادة تجدد الخلايا النجمية الصغيرة, زراعة الوحيدات النواة, الالتهاب العصبي, السكتة الإقفارية