Clear Sky Science · nl
Verschillende oorsprongen en niches bepalen de cellulaire reactievermogen van CNS‑macrofagen na herbevolking
Waarom bewakers aan de hersenranden ertoe doen
Onze hersenen bestaan niet alleen uit zenuwcellen. Ze worden ook gepatrouilleerd door immuuncellen die óf diep in het weefsel zitten óf op de randen, waar de hersenen de beschermende membranen en bloedvaten ontmoeten. Deze studie onderzoekt hoe verschillende groepen van deze immuunwachters verdwijnen en daarna teruggroeien, en laat zien dat de manier waarop ze worden vervangen invloed kan hebben op hoe de hersenen reageren op ontsteking en beroerte. Inzicht in dit herstelproces opent de deur naar therapieën die de grensimmuuncellen bijsturen zonder de rest van de hersenen te verstoren.
Verschillende buurten, verschillende bewakers
Immuuncellen die macrofagen worden genoemd, bevolken uiteenlopende “buurten” in het centraal zenuwstelsel. Microglia leven in het hersenweefsel zelf, terwijl zogenaamde grensmacrofagen langs de oppervlakten van de hersenen en rond bloedvaten zitten. Binnen deze grenspopulaties liggen subdurale macrofagen net boven het hersenweefsel en omarmen ze het oppervlak en perivasculaire ruimten, terwijl een andere groep de stevige buitenste membraan, de dura, bewoont. Hoewel al deze populaties helpen bij het controleren en vormen van immuunreacties in de hersenen, verschillen ze in oorsprong en levensduur, en eerder werk suggereerde dat microglia zichzelf lokaal kunnen onderhouden zonder hulp van in het bloed circulerende cellen.
Het systeem resetten en het teruggroeien volgen
Om te zien hoe elke macrofaaggroep herstelt nadat ze zijn gewist, gebruikten de onderzoekers een geneesmiddel dat een belangrijke overlevingssignaalblokkeert en deze cellen tijdelijk uitputte bij muizen. Ze volgden vervolgens hoe en waar de cellen terugkwamen met een combinatie van genetische “barcode”‑muizen, single‑cell RNA‑sequencing, chromatineprofilering en hogeresolutiemicroscopie. Microglia in het hersenweefsel kwamen snel en vrijwel volledig terug door te delen vanuit de zeldzame overlevenden die de uitputting ontsnapten, en er was geen aanwijzing dat circulerende immuuncellen naar binnen trokken om hen te vervangen. Daarentegen herbevolkten subdurale macrofagen aan het hersenoppervlak langzaam en ongelijkmatig tussen gebieden, wat suggereert dat ze aanvullende bronnen aanboorden buiten de oorspronkelijke residentiële cellen. 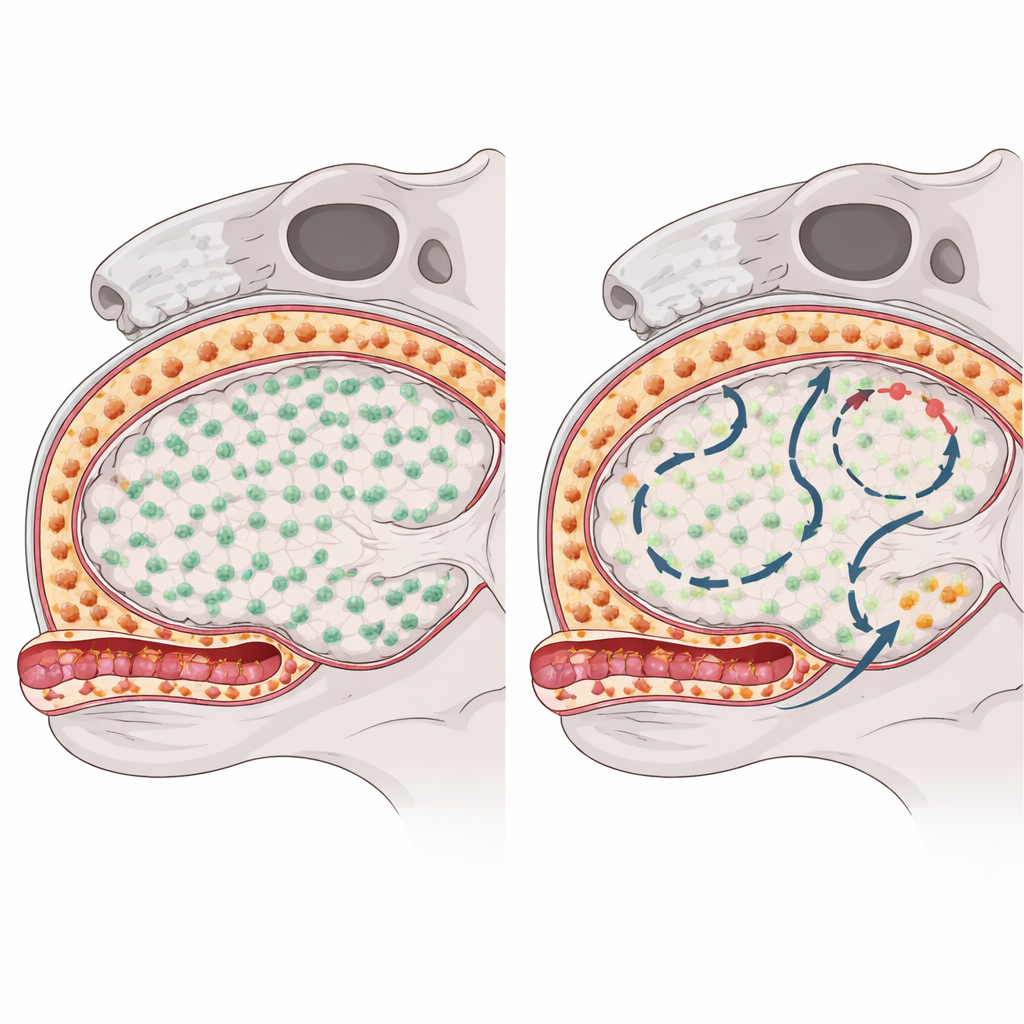
Wanneer bloedcellen binnendringen en blijven
Fate‑mappingexperimenten toonden aan dat, in tegenstelling tot microglia, subdurale macrofagen hun niches gedeeltelijk aanvulden met kortlevende monocyten die in het bloed circuleren. Na uitputting creëerden signalen van bloedvat- en stromale cellen een tijdelijke venster waarin deze monocyten zich aan geactiveerde vaatwanden konden hechten, eroverheen konden kruipen met behulp van adhesiemoleculen zoals ICAM‑1 en VCAM‑1, en zich nestelden in perivasculaire en oppervlakte‑niches. Het blokkeren van deze adhesieroutes verminderde het aantal binnenkomende cellen, wat hun belang bevestigde. Eenmaal ingegroeid imiteerden monocyten‑afgeleide grensmacrofagen niet simpelweg de oorspronkelijke embryo‑afgeleide cellen: ze behielden een onderscheidend genexpressie‑ en chromatinepatroon, waren verrijkt voor moleculen die betrokken zijn bij antigeenpresentatie en cel‑adhesie, en bleven een stabiel deel van de populatie lang nadat de initiële schade schijnbaar was genezen.
Blijvende herschakeling van grensimmuniteit
Single‑cell en bulksequencing toonden aan dat microglia grotendeels hun oorspronkelijke moleculaire profiel herwonnen na herbevolking, met minimale lange termijn veranderingen. Subdurale macrofagen daarentegen waren duurzaam verschoven naar een meer “alert” subtype dat hogere niveaus van immuunactivatiegenen tot expressie bracht. Door embryo‑afgeleide en monocyten‑afgeleide cellen te scheiden met genetische labels, kon het team aantonen dat de ontwikkelingsoorsprong sterk zowel de genactiviteit als de toegankelijke DNA‑regio’s in deze cellen bepaalde. Monocyten‑afgeleide grensmacrofagen droegen epigenetische kenmerken die typisch zijn voor recent gedifferentieerde bloedcellen en toonden toegenomen toegankelijkheid bij genen die betrokken zijn bij het waarnemen van pathogenen en interactie met andere immuuncellen. Wanneer de dieren werden uitgedaagd met bacteriële componenten, gaven deze nieuwkomers sterkere ontstekings‑ en stressreacties dan hun embryo‑afgeleide buren, terwijl de reacties van microglia en durale macrofagen veel minder veranderd waren. 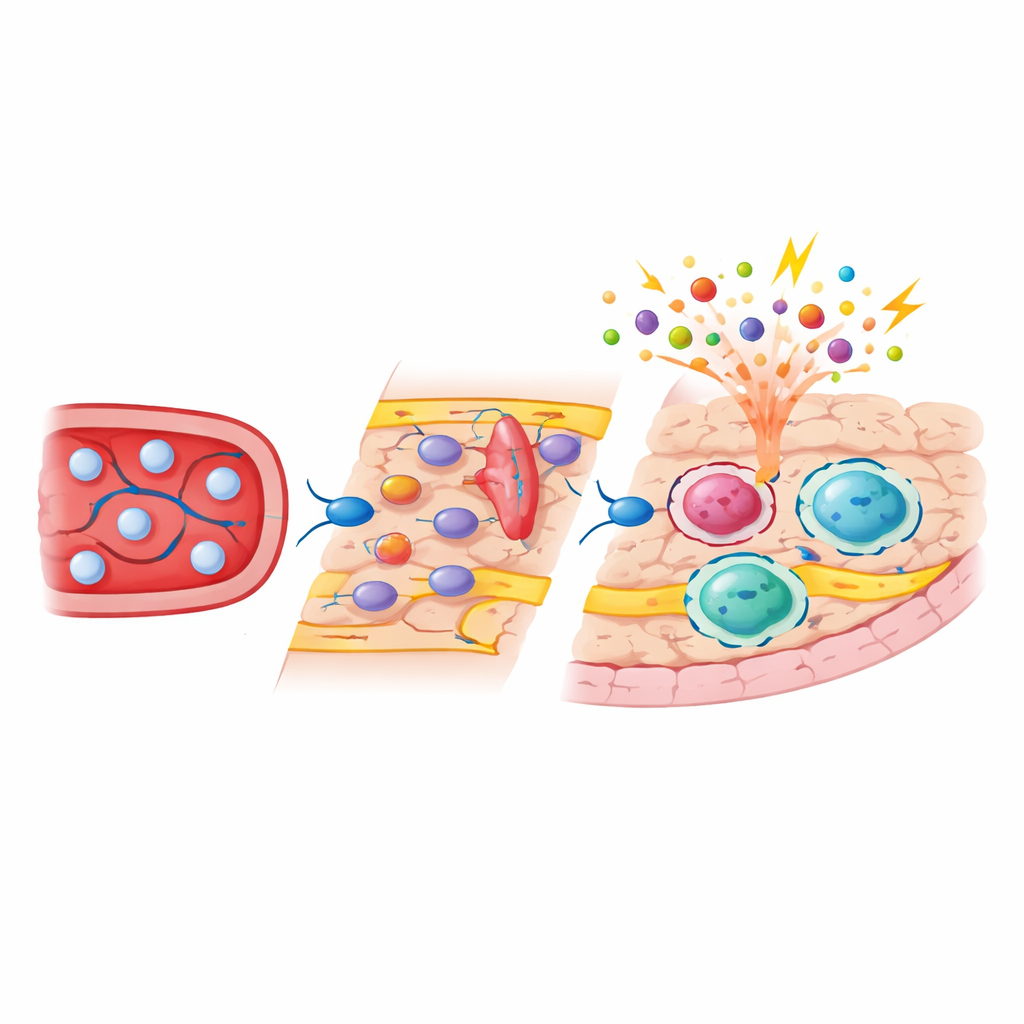
Gevolgen voor beroerte en hersengezondheid
De auteurs vroegen zich vervolgens af of deze verborgen herinrichting van grensmacrofagen ziekte beïnvloedt. In een model van ischemische beroerte presteerden muizen waarvan de subdurale macrofagen waren herbevolkt slechter in gedragstests, hoewel de laesiegrootte en het opnieuw open gaan van bloedvaten vergelijkbaar waren met controles. Analyse van geheel weefsel en geïsoleerde grensmacrofagen toonde sterkere inductie van genen die gekoppeld zijn aan ontsteking, reactieve zuurstofsoorten en verstoring van de bloed‑hersenbarrière in herbevolkte dieren. Monocyten‑afgeleide grenscellen waren bijzonder reactief en produceerden na beroerte meer chemokinen en activatiemarkers. Beeldvorming van vaatactivatie bevestigde een hoger signaal voor P‑selectine, een teken van intense vasculaire ontsteking, wat correleerde met slechter herstel van motorische functies.
Wat dit betekent voor toekomstige behandelingen
Dit werk laat zien dat niet alle hersenmacrofagen gelijk zijn, en dat hun vervanging het systeem niet simpelweg reset. Microglia kunnen zichzelf stilletjes herbouwen vanuit de overlevende cellen en terugkeren naar de normale toestand. Daarentegen worden grensmacrofagen aan het hersenoppervlak een blijvende mix van oorspronkelijke, embryo‑afgeleide cellen en nieuwkomers uit het bloed, en deze gemengde populatie reageert agressiever op systemische ontsteking en beroerte. Omdat de onderzoekers een manier ontwikkelden om deze grenscellen selectief te vervangen terwijl microglia spaard blijven, wijzen hun bevindingen op een toekomst waarin therapieën de immuungrenzen van de hersenen fijn kunnen afstemmen — ofwel door schadelijke ontsteking bij aandoeningen zoals beroerte en neurodegeneratie te dempen, of door beschermende reacties te versterken — zonder het interne immuunsysteem van de hersenen globaal te verstoren.
Bronvermelding: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Trefwoorden: macrofagen aan de rand van de hersenen, microglia‑herbevolking, monocyt‑engraftment, neuro‑inflammatie, ischemische beroerte