Clear Sky Science · pt
Origens e nichos distintos determinam a responsividade celular dos macrófagos do SNC após repovoamento
Por que os guardiões das bordas cerebrais importam
Nossos cérebros não são feitos apenas de neurônios. Eles também são patrulhados por células imunes que se alojam tanto no interior do tecido quanto em suas bordas, onde o cérebro encontra suas membranas protetoras e vasos sanguíneos. Este estudo investiga como diferentes grupos desses sentinelas imunes desaparecem e depois se regeneram, e mostra que a forma como são substituídos pode alterar a resposta do cérebro à inflamação e ao AVC. Compreender essa regeneração abre caminho para terapias que ajustem as células imunes das bordas sem perturbar o restante do cérebro.
Bairros diferentes, sentinelas cerebrais diferentes
Células imunes chamadas macrófagos ocupam “bairros” distintos no sistema nervoso central. As microglias vivem dentro do próprio tecido cerebral, enquanto os chamados macrófagos de borda ficam ao longo das superfícies do cérebro e ao redor dos vasos sanguíneos. Entre essas células de borda, os macrófagos subdurais situam‑se logo acima do tecido cerebral, abraçando a superfície e os espaços perivascular, enquanto outro grupo popula a membrana externa resistente chamada dura. Embora todas essas populações ajudem a monitorar e moldar respostas imunes no cérebro, elas têm origens e tempos de vida diferentes, e trabalhos anteriores sugeriram que as microglias podem se manter localmente sem a ajuda de células provenientes do sangue.
Resetando o sistema e observando a regeneração
Para ver como cada grupo de macrófagos se recupera após ser eliminado, os pesquisadores usaram um fármaco que bloqueia um sinal de sobrevivência chave e esgota temporariamente essas células em camundongos. Em seguida acompanharam como e de onde as células retornavam usando uma combinação de camundongos com “códigos de barras” genéticos, sequenciamento de RNA de célula única, perfilamento de cromatina e microscopia de alta resolução. As microglias no tecido cerebral se recuperaram rapidamente e quase por completo, dividindo‑se a partir dos raros sobreviventes que escaparam da depleção, sem evidência de que células circulantes do sangue tenham entrado para substituí‑las. Em contraste, os macrófagos subdurais na superfície cerebral repovoaram de forma lenta e desigual entre as regiões, indicando que recorriam a fontes adicionais além das células residentes originais. 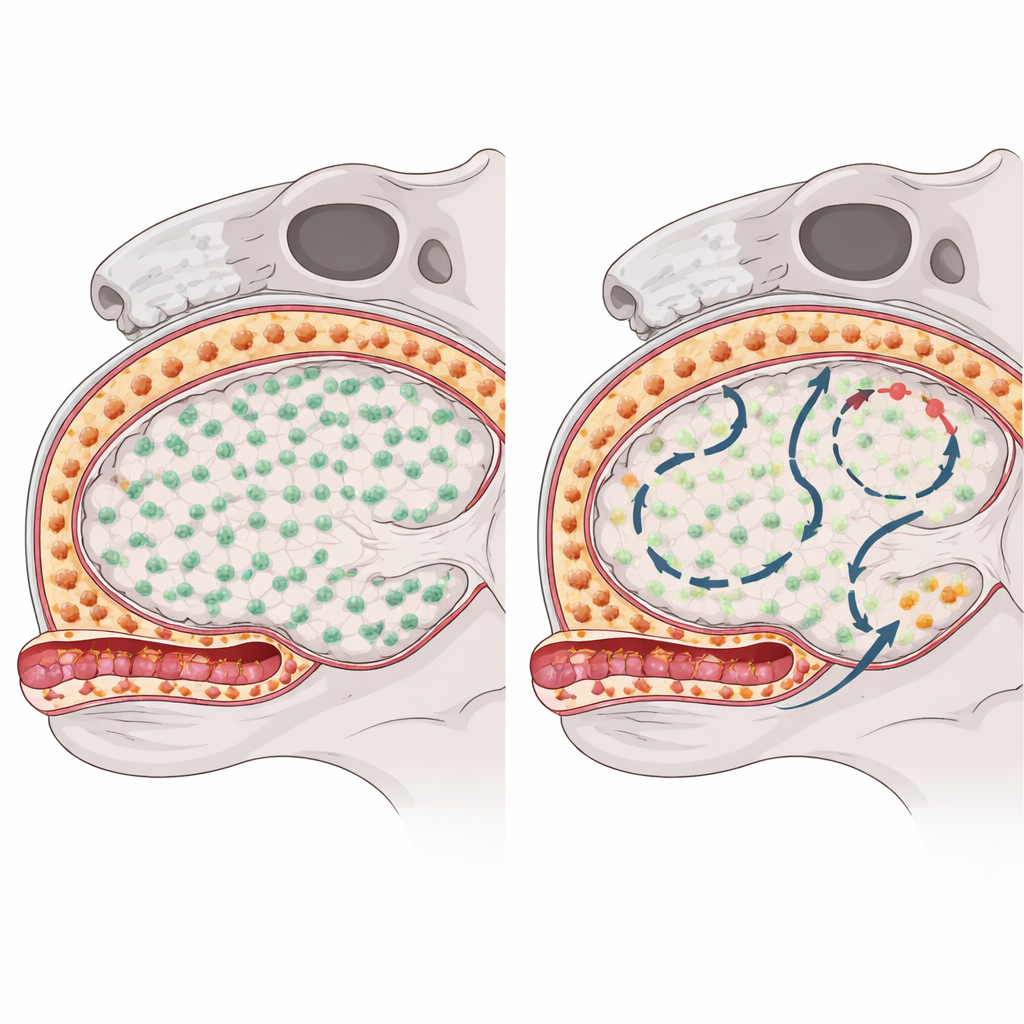
Quando células sanguíneas entram e permanecem
Experimentos de mapeamento de destino mostraram que, diferentemente das microglias, os macrófagos subdurais reocuparam parcialmente seus nichos usando monócitos de vida curta que circulam no sangue. Após a depleção, sinais vindos de células vasculares e estromais criaram uma janela temporária na qual esses monócitos puderam aderir às paredes vasculares ativadas, transitar por elas com a ajuda de moléculas de adesão como ICAM‑1 e VCAM‑1, e se instalar em nichos perivasculares e superficiais. Bloquear essas vias de adesão reduziu o número de células entrantes, confirmando sua importância. Uma vez engraftadas, os macrófagos de borda derivados de monócitos não imitavam simplesmente as células originadas no embrião: mantiveram padrões distintos de expressão gênica e de cromatina, apresentaram enriquecimento em moléculas envolvidas em apresentação de antígeno e adesão celular, e permaneceram como parte estável da população muito tempo depois de a lesão inicial aparentemente ter cicatrizado.
Reconfiguração duradoura da imunidade de borda
Sequenciamento de célula única e em massa revelou que as microglias em grande parte recuperaram seu perfil molecular original após o repovoamento, com mudanças de longo prazo mínimas. Os macrófagos subdurais, no entanto, foram duravelmente reequilibrados para um subtipo mais “alerta” que expressava níveis mais altos de genes de ativação imune. Ao separar células derivadas do embrião e derivadas de monócitos usando marcas genéticas, a equipe mostrou que a origem do desenvolvimento moldou fortemente tanto a atividade gênica quanto as regiões de DNA acessíveis nessas células. Os macrófagos de borda derivados de monócitos carregavam marcas epigenéticas típicas de células sanguíneas recém‑diferenciadas e exibiam maior acessibilidade em genes envolvidos na detecção de patógenos e na interação com outras células imunes. Quando os animais foram desafiados com componentes bacterianos, essas células recém‑chegadas montaram respostas inflamatórias e de estresse mais intensas do que suas vizinhas de origem embrionária, enquanto as reações das microglias e dos macrófagos da dura foram muito menos alteradas. 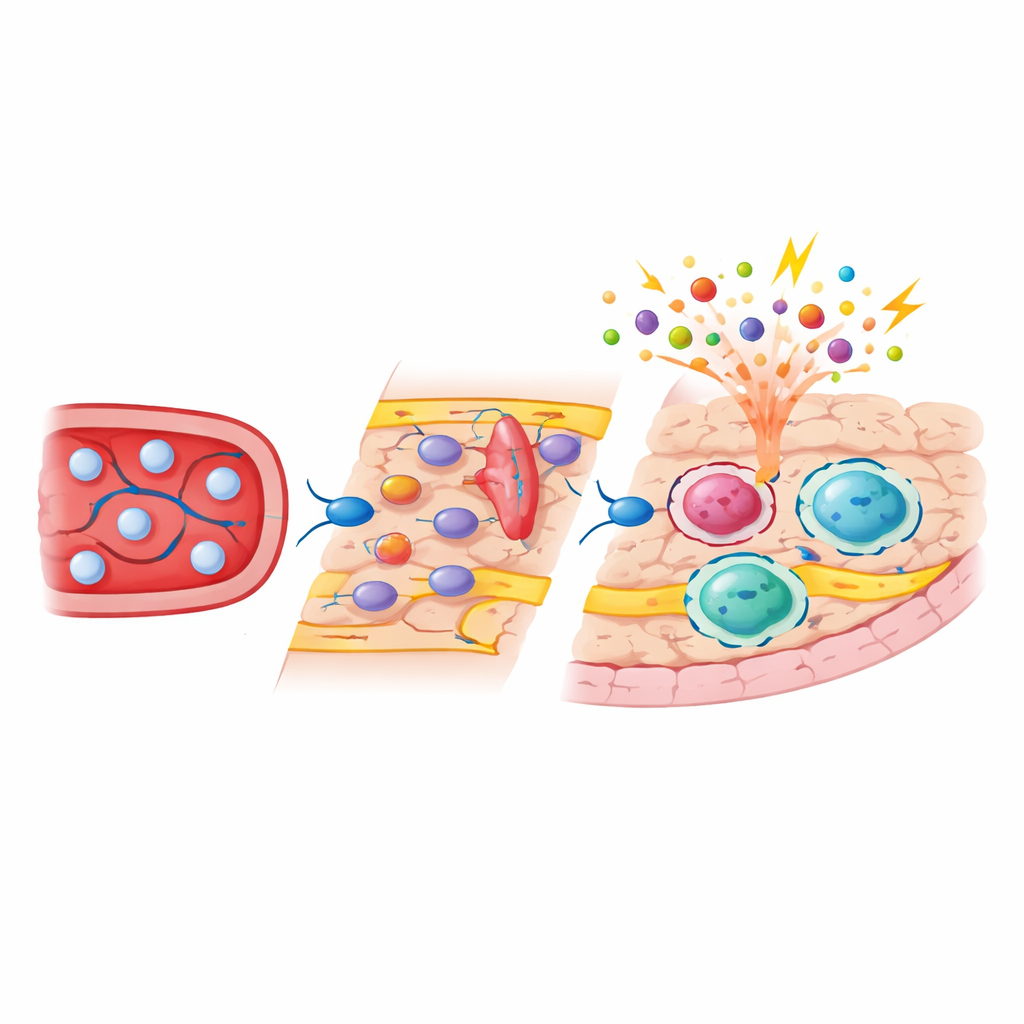
Consequências para AVC e saúde cerebral
Os autores então perguntaram se essa remodelação oculta dos macrófagos de borda afeta a doença. Em um modelo de AVC isquêmico, camundongos cujos macrófagos subdurais haviam sido repovoados apresentaram desempenho pior em testes comportamentais, embora o tamanho da lesão e a reabertura dos vasos fossem semelhantes aos controles. Análises de tecido inteiro e de macrófagos de borda isolados mostraram indução mais forte de genes ligados à inflamação, espécies reativas de oxigênio e ruptura da barreira hematoencefálica nos animais repovoados. As células de borda derivadas de monócitos foram especialmente reativas, produzindo mais quimiocinas e marcadores de ativação após o AVC. Imageamento da ativação vascular confirmou sinal mais alto de P‑selectina, um marcador de inflamação vascular intensa, que se correlacionou com recuperação motora pior.
O que isso significa para tratamentos futuros
Este trabalho mostra que nem todos os macrófagos cerebrais são iguais, e que substituí‑los não simplesmente reinicia o sistema. As microglias podem reconstruir‑se silenciosamente a partir de células sobreviventes e voltar às atividades normais. Em contraste, os macrófagos de borda na superfície cerebral tornam‑se uma mistura permanente de células originais de origem embrionária e novos arrivantes do sangue, e essa população mista responde de forma mais agressiva à inflamação sistêmica e ao AVC. Como os pesquisadores desenvolveram um modo de trocar seletivamente essas células de borda poupando as microglias, suas descobertas apontam para um futuro em que terapias poderiam ajustar finamente as fronteiras imunes do cérebro — seja atenuando inflamações prejudiciais em doenças como AVC e neurodegeneração, seja potencializando respostas protetoras — sem interromper globalmente a rede imune interna do cérebro.
Citação: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Palavras-chave: macrófagos das bordas cerebrais, repovoamento de microglia, engraftamento de monócitos, neuroinflamação, acidente vascular isquêmico