Clear Sky Science · it
Origini e nicchie distinte determinano la reattività cellulare dei macrofagi del SNC dopo la ripopolazione
Perché i guardiani delle frontiere cerebrali sono importanti
I nostri cervelli non sono costituiti solo da cellule nervose. Sono anche pattugliati da cellule immunitarie che risiedono tanto all’interno del tessuto quanto alle sue frontiere, dove il cervello incontra le meningi e i vasi sanguigni. Questo studio esplora come diversi gruppi di questi sentinelle immunitari scompaiono e poi ritornano, e mostra che il modo in cui vengono rimpiazzati può modificare la risposta del cervello all’infiammazione e all’ictus. Comprendere questa ricrescita apre la strada a terapie che modulano le cellule immunitarie di confine senza perturbare il resto del cervello.
Quartieri diversi, sentinelle diverse
Cellule immunitarie chiamate macrofagi occupano “quartieri” distinti nel sistema nervoso centrale. La microglia vive all’interno del tessuto cerebrale, mentre i cosiddetti macrofagi di confine si trovano lungo le superfici cerebrali e intorno ai vasi sanguigni. Tra queste cellule di confine, i macrofagi subdurali giacciono appena sopra il tessuto cerebrale, aderendo alla superficie e agli spazi perivascolari, mentre un altro gruppo popola la dura madre, la robusta membrana esterna. Sebbene tutte queste popolazioni contribuiscano a monitorare e modellare le risposte immunitarie nel cervello, hanno origini e longevità differenti, e lavori precedenti suggerivano che la microglia possa mantenersi localmente senza l’aiuto di cellule provenienti dal sangue.
Azzerare il sistema e osservare la ricrescita
Per vedere come ogni gruppo di macrofagi si riprende dopo essere stato eliminato, i ricercatori hanno usato un farmaco che blocca un segnale chiave per la sopravvivenza e depleta temporaneamente queste cellule nei topi. Hanno poi tracciato come e da dove le cellule ricomparivano usando una combinazione di topi con “codici a barre” genetici, sequenziamento dell’RNA a singola cellula, profilazione della cromatina e microscopia ad alta risoluzione. La microglia nel tessuto cerebrale è tornata rapidamente e quasi completamente dividendosi a partire dai rari sopravvissuti che avevano eluso la deplezione, senza segni di sostituzione da parte di cellule circolanti. Al contrario, i macrofagi subdurali sulla superficie cerebrale si sono ripopolati lentamente e in modo non uniforme tra le regioni, suggerendo che si rifornissero anche da fonti aggiuntive oltre alle cellule residenti originarie. 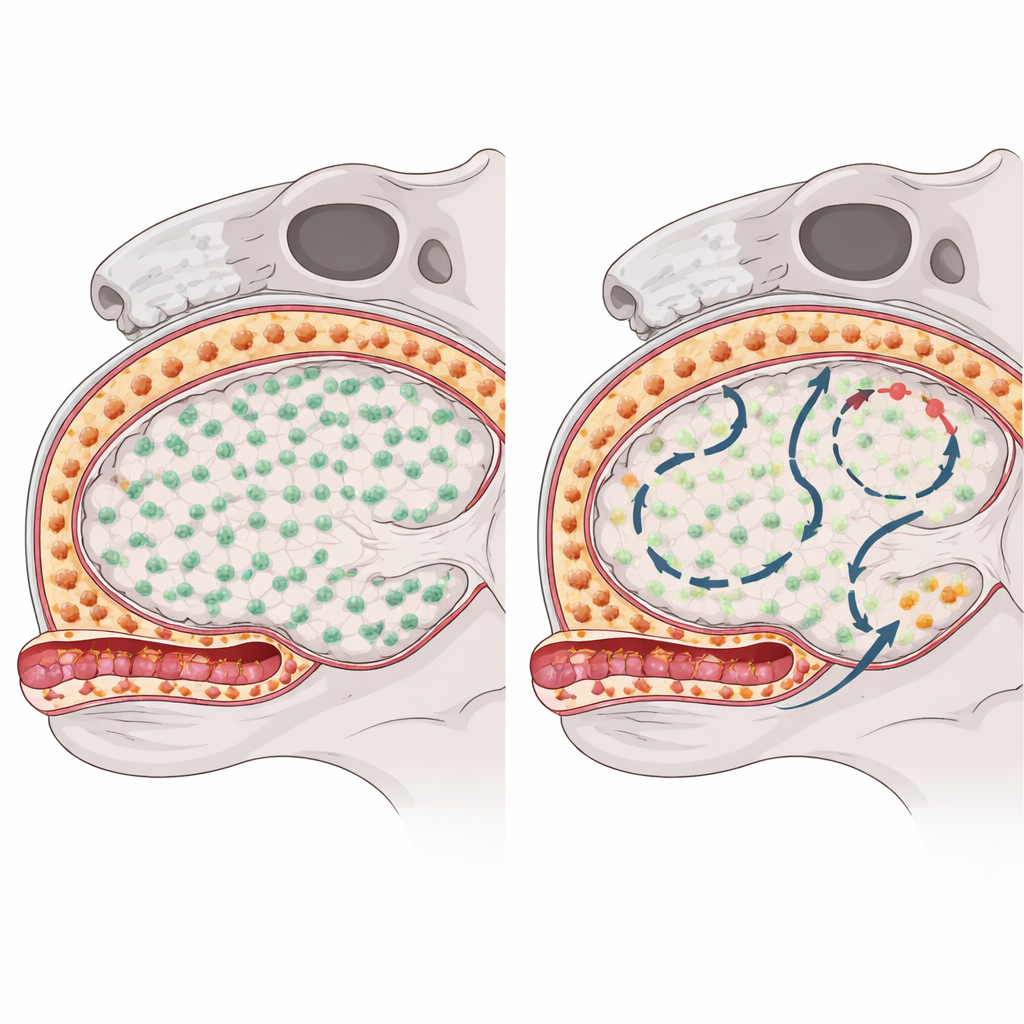
Quando le cellule del sangue entrano e restano
Esperimenti di fate‑mapping hanno mostrato che, a differenza della microglia, i macrofagi subdurali hanno parzialmente reintegrato le loro nicchie usando monociti a breve vita che circolano nel sangue. Dopo la deplezione, segnali provenienti dalle cellule vascolari e stromali hanno creato una finestra temporanea in cui questi monociti potevano aderire alle pareti vascolari attivate, spostarsi su di esse con l’aiuto di molecole di adesione come ICAM‑1 e VCAM‑1, e insediarsi in nicchie perivascolari e superficiali. Il blocco di queste vie di adesione ha ridotto il numero di cellule in ingresso, confermandone l’importanza. Una volta engrafted, i macrofagi di confine derivati dai monociti non si sono limitati a imitare le cellule originarie di derivazione embrionale: hanno mantenuto un profilo di espressione genica e di cromatina distinto, erano arricchiti per molecole coinvolte nella presentazione di antigeni e nell’adesione cellulare, e sono rimasti come parte stabile della popolazione molto tempo dopo che il danno iniziale sembrava essersi risolto.
Rimodellamento duraturo dell’immunità di confine
Sequenziamenti a singola cellula e bulk hanno rivelato che la microglia ha in gran parte riacquistato il suo profilo molecolare originale dopo la ripopolazione, con cambiamenti a lungo termine minimi. I macrofagi subdurali, invece, sono stati stabilmente riequilibrati verso un sottotipo più “allertato” che esprimeva livelli più elevati di geni di attivazione immunitaria. Separando le cellule di derivazione embrionale da quelle derivate dai monociti tramite etichette genetiche, il gruppo ha dimostrato che l’origine di sviluppo ha plasmato in modo marcato sia l’attività genica sia le regioni di DNA accessibili in queste cellule. I macrofagi di confine derivati dai monociti portavano marchi epigenetici tipici di cellule ematiche recentemente differenziate e mostravano una maggiore accessibilità in geni coinvolti nel riconoscere patogeni e nell’interagire con altre cellule immunitarie. Quando gli animali sono stati sfidati con componenti batterici, queste cellule neospecate hanno montato risposte infiammatorie e di stress più forti rispetto ai loro vicini di derivazione embrionale, mentre le reazioni di microglia e macrofagi durali sono risultate molto meno alterate. 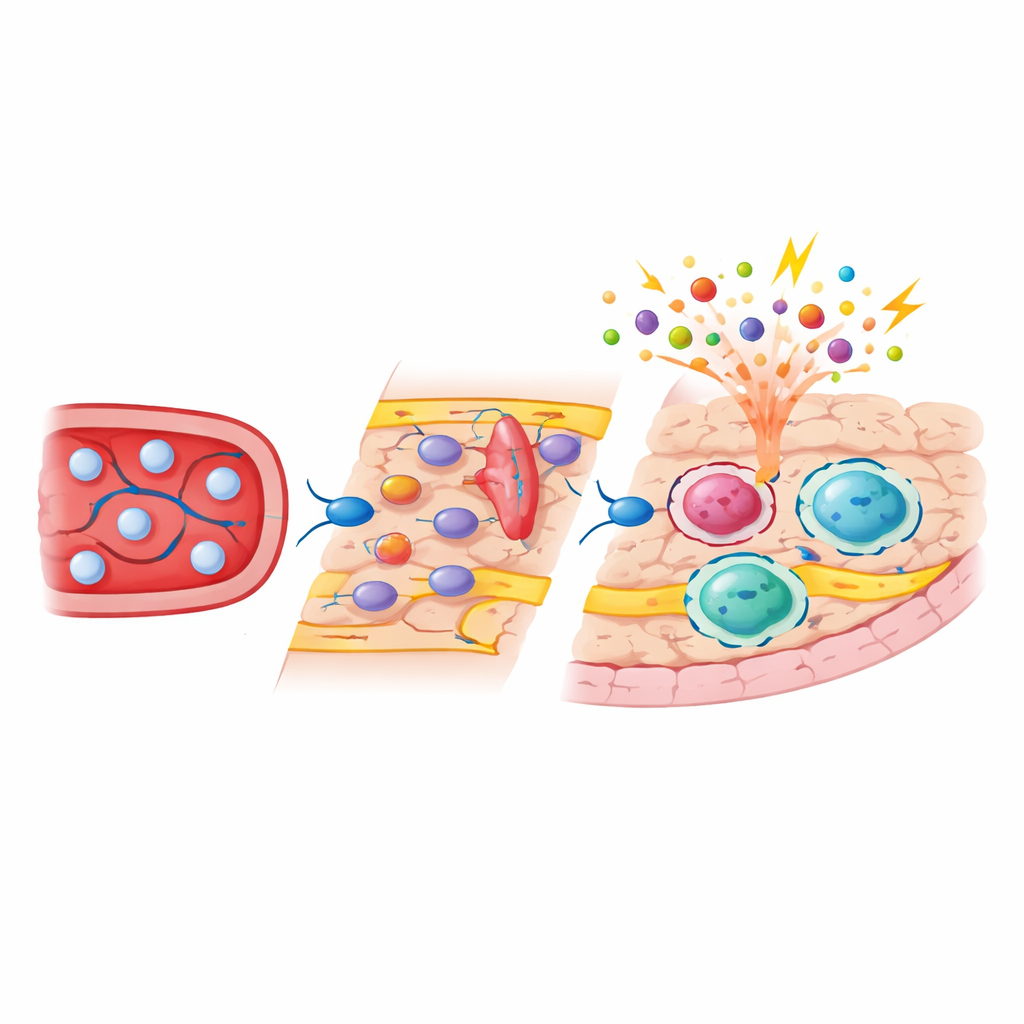
Conseguenze per l’ictus e la salute cerebrale
Gli autori si sono poi chiesti se questo rimodellamento nascosto dei macrofagi di confine influenzi la malattia. In un modello di ictus ischemico, i topi i cui macrofagi subdurali erano stati ripopolati hanno mostrato prestazioni peggiori nei test comportamentali, sebbene la dimensione della lesione e la riapertura dei vasi fossero simili ai controlli. L’analisi del tessuto intero e dei macrofagi di confine isolati ha mostrato una più forte induzione di geni legati all’infiammazione, alla produzione di specie reattive dell’ossigeno e alla compromissione della barriera emato‑encefalica negli animali ripopolati. Le cellule di confine derivate dai monociti sono risultate particolarmente reattive, producendo più chemochine e marcatori di attivazione dopo l’ictus. L’imaging dell’attivazione vascolare ha confermato un segnale più alto per la P‑selectina, un marcatore di intensa infiammazione vascolare, che correlava con un recupero motorio peggiore.
Cosa significa per le terapie future
Questo lavoro dimostra che non tutti i macrofagi cerebrali sono uguali e che rimpiazzarli non equivale a riportare il sistema allo stato iniziale. La microglia può ricostituirsi silenziosamente a partire dalle cellule sopravvissute e tornare alle funzioni consuete. Al contrario, i macrofagi di confine sulla superficie cerebrale diventano un mix permanente di cellule originarie di derivazione embrionale e di nuove arrivate dal sangue, e questa popolazione mista risponde in modo più aggressivo all’infiammazione sistemica e all’ictus. Poiché i ricercatori hanno sviluppato un metodo per scambiare selettivamente queste cellule di confine preservando la microglia, i loro risultati indicano un futuro in cui le terapie potrebbero modulare finemente le frontiere immunitarie del cervello — riducendo l’infiammazione dannosa in patologie come l’ictus e le neurodegenerazioni o potenziando risposte protettive — senza perturbare globalmente la rete immunitaria interna del cervello.
Citazione: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Parole chiave: macrofagi delle frontiere cerebrali, ripopolazione della microglia, inglobamento dei monociti, neuroinfiammazione, ictus ischemico