Clear Sky Science · fr
Origines distinctes et niches déterminent la réactivité cellulaire des macrophages du SNC après repopulation
Pourquoi les gardiens des frontières cérébrales comptent
Nos cerveaux ne sont pas composés uniquement de neurones. Ils sont aussi patrouillés par des cellules immunitaires qui se trouvent soit profondément dans le tissu soit à ses frontières, là où le cerveau rencontre ses membranes protectrices et les vaisseaux sanguins. Cette étude examine comment différents groupes de ces sentinelles immunitaires disparaissent puis repoussent, et montre que la manière dont ils sont remplacés peut modifier la réponse du cerveau à l’inflammation et à l’AVC. Comprendre cette régénération ouvre la voie à des thérapies qui moduleraient les cellules immunitaires frontières sans perturber le reste du cerveau.
Quartiers différents, sentinelles différentes
Des cellules immunitaires appelées macrophages occupent des « quartiers » distincts du système nerveux central. Les microglies vivent au sein même du tissu cérébral, tandis que les macrophages de frontière siègent le long des surfaces du cerveau et autour des vaisseaux sanguins. Parmi ces cellules de frontière, les macrophages sous-duraux se situent juste au‑dessus du tissu cérébral, épousant la surface et les espaces périvasculaires, alors qu’un autre groupe peuple la membrane externe résistante appelée dure-mère. Bien que ces populations contribuent toutes à surveiller et façonner les réponses immunitaires dans le cerveau, elles ont des origines et des durées de vie différentes, et des travaux antérieurs suggéraient que les microglies peuvent s’auto-entretenir localement sans apport de cellules circulantes.
Réinitialiser le système et observer la repousse
Pour voir comment chaque groupe de macrophages se rétablit après élimination, les chercheurs ont utilisé un médicament bloquant un signal de survie clé et déplétant temporairement ces cellules chez la souris. Ils ont ensuite suivi d’où et comment les cellules revenaient en utilisant une combinaison de souris génétiquement « barcodées », de séquençage ARN unicellulaire, de profilage de la chromatine et de microscopie haute résolution. Les microglies dans le tissu cérébral ont rebondi rapidement et presque complètement en se divisant à partir des rares survivantes ayant échappé à la déplétion, et il n’y avait aucune trace d’un remplacement par des cellules immunitaires circulantes. En revanche, les macrophages sous-duraux à la surface cérébrale se sont repeuplés lentement et de manière inégale selon les régions, ce qui suggère qu’ils puisaient des sources supplémentaires au-delà des cellules résidentes d’origine. 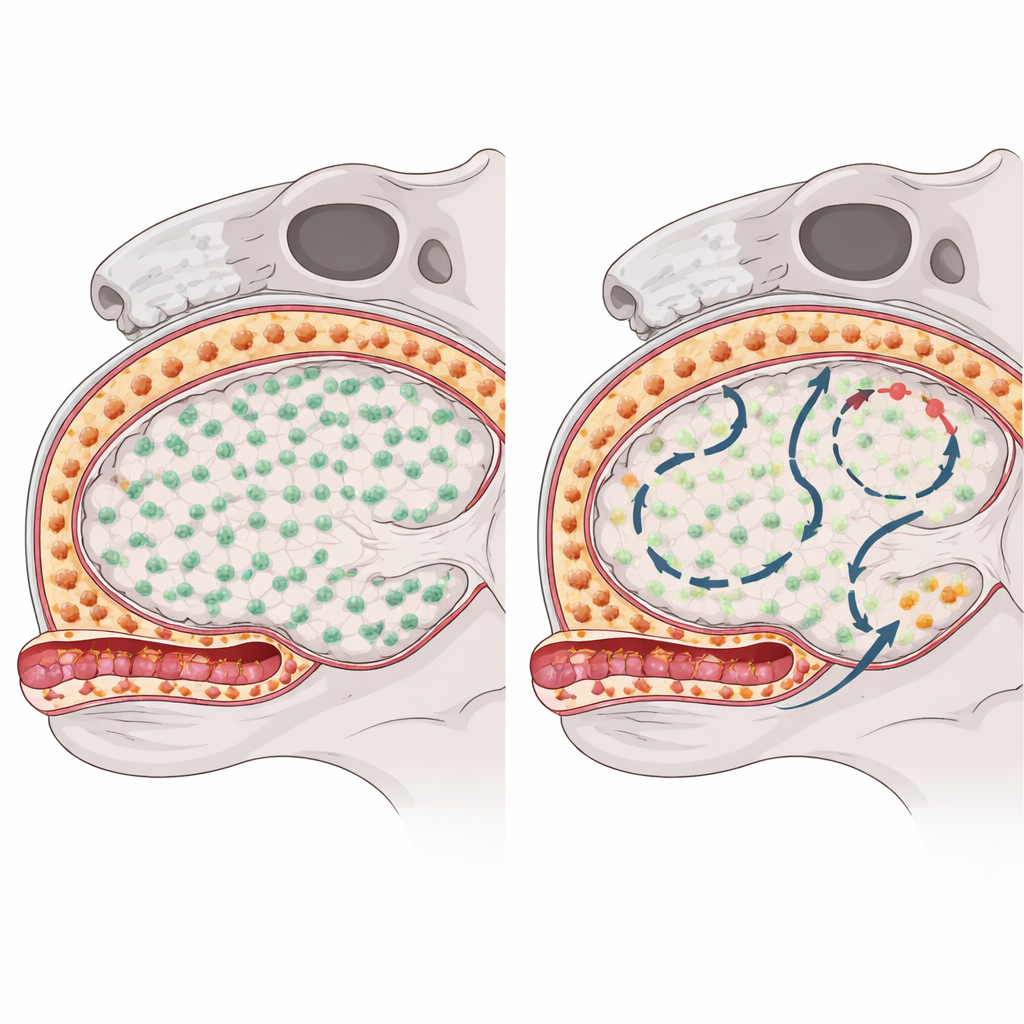
Quand les cellules sanguines s’installent et restent
Des expériences de traçage de destinée ont montré que, contrairement aux microglies, les macrophages sous-duraux ont partiellement reconstitué leurs niches en utilisant des monocytes à courte durée de vie circulant dans le sang. Après déplétion, des signaux provenant des cellules vasculaires et stromales ont créé une fenêtre temporaire permettant à ces monocytes d’adhérer aux parois vasculaires activées, de les traverser en ramifiant avec l’aide de molécules d’adhésion telles que ICAM‑1 et VCAM‑1, et de s’installer dans les niches périvasculaires et de surface. Le blocage de ces voies d’adhésion a réduit le nombre de cellules entrantes, confirmant leur importance. Une fois greffés, les macrophages border dérivés des monocytes n’imitaient pas simplement les cellules d’origine embryonnaire : ils conservaient un profil d’expression génique et de chromatine distinct, étaient enrichis en molécules impliquées dans la présentation d’antigènes et l’adhésion cellulaire, et restaient une partie stable de la population longtemps après que la lésion initiale semblait cicatrisée.
Réorganisation durable de l’immunité frontalière
Le séquençage unicellulaire et en masse a révélé que les microglies retrouvaient en grande partie leur profil moléculaire d’origine après repeuplement, avec des changements à long terme minimes. Les macrophages sous-duraux, en revanche, ont été durablement réorientés vers un sous-type plus « en alerte » exprimant des niveaux supérieurs de gènes d’activation immunitaire. En séparant les cellules d’origine embryonnaire et celles dérivées des monocytes par des marqueurs génétiques, l’équipe a montré que l’origine développementale façonnait fortement à la fois l’activité génique et les régions d’ADN accessibles chez ces cellules. Les macrophages border dérivés des monocytes portaient des marques épigénétiques typiques de cellules sanguines récemment différenciées et présentaient une accessibilité augmentée aux gènes impliqués dans la détection de pathogènes et les interactions avec d’autres cellules immunitaires. Lorsque les animaux étaient exposés à des composants bactériens, ces cellules nouvellement arrivées déclenchaient des réponses inflammatoires et de stress plus intenses que leurs voisines d’origine embryonnaire, tandis que les réactions des microglies et des macrophages duraux étaient beaucoup moins modifiées. 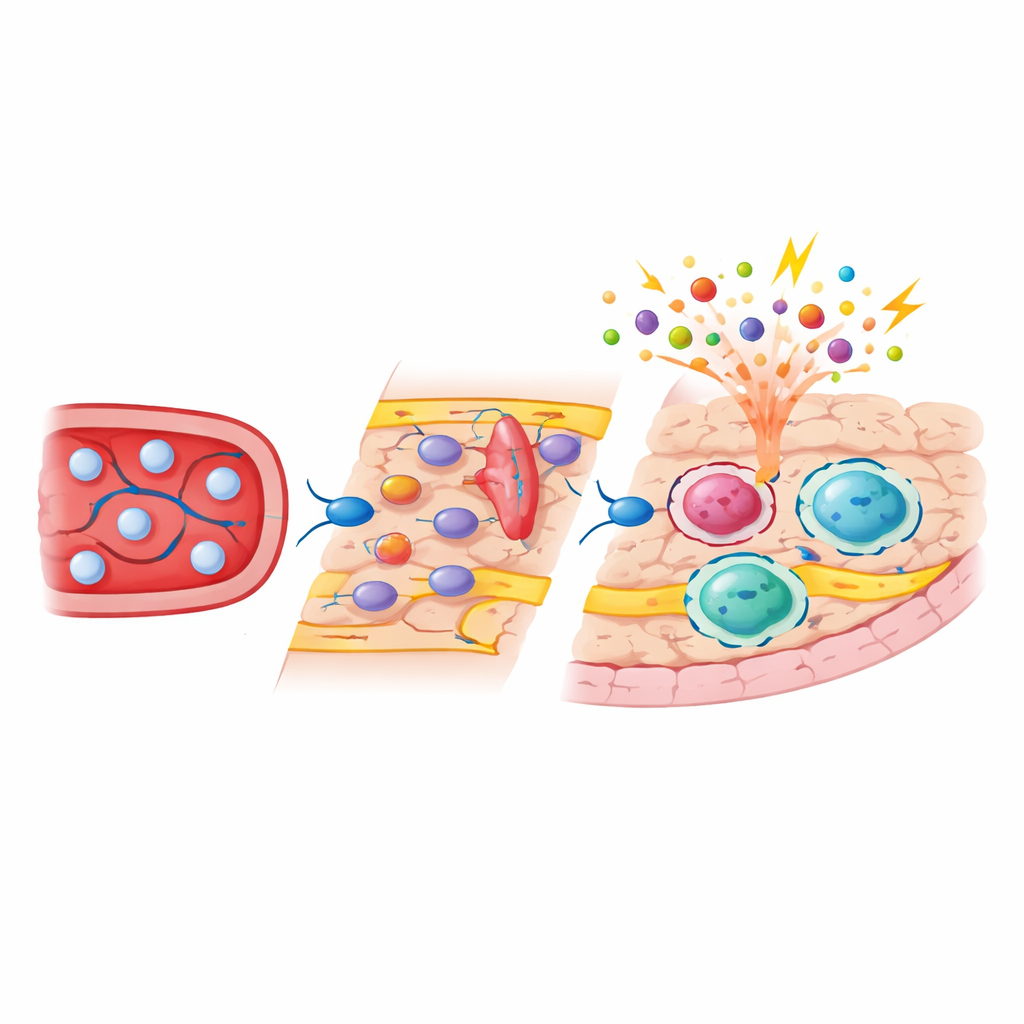
Conséquences pour l’AVC et la santé cérébrale
Les auteurs se sont ensuite demandé si ce remodelage discret des macrophages frontières affectait la maladie. Dans un modèle d’accident vasculaire ischémique, les souris dont les macrophages sous-duraux avaient été repeuplés ont présenté de moins bonnes performances aux tests comportementaux, même si la taille des lésions et la réouverture vasculaire étaient similaires à celles des témoins. L’analyse du tissu entier et des macrophages frontière isolés a montré une induction plus marquée de gènes liés à l’inflammation, aux espèces réactives de l’oxygène et à la perturbation de la barrière hémato‑encéphalique chez les animaux repeuplés. Les cellules frontières dérivées des monocytes étaient particulièrement réactives, produisant davantage de chimiokines et de marqueurs d’activation après l’AVC. L’imagerie de l’activation vasculaire a confirmé un signal plus élevé pour la P‑sélectine, un marqueur d’inflammation vasculaire intense, corrélant avec une récupération motrice plus faible.
Ce que cela signifie pour les traitements futurs
Ce travail montre que tous les macrophages cérébraux ne se valent pas, et que les remplacer ne réinitialise pas simplement le système. Les microglies peuvent se reconstruire discrètement à partir des cellules survivantes et reprendre leurs fonctions habituelles. En revanche, les macrophages de frontière à la surface cérébrale deviennent un mélange permanent de cellules d’origine embryonnaire et de nouveaux arrivants sanguins, et cette population mixte répond de façon plus agressive à l’inflammation systémique et à l’AVC. Parce que les chercheurs ont développé une méthode permettant d’échanger sélectivement ces cellules frontières tout en épargnant les microglies, leurs résultats ouvrent la perspective de thérapies qui ajusteraient finement les frontières immunitaires du cerveau — soit en atténuant l’inflammation délétère dans des maladies comme l’AVC et la neurodégénérescence, soit en renforçant des réponses protectrices — sans perturber globalement le réseau immunitaire interne du cerveau.
Citation: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Mots-clés: macrophages des frontières cérébrales, repeuplement des microglies, engraftement des monocytes, neuroinflammation, accident vasculaire ischémique