Clear Sky Science · es
Orígenes y nichos distintos determinan la capacidad de respuesta celular de los macrófagos del SNC tras la repoblación
Por qué importan los guardianes de las fronteras cerebrales
Nuestros cerebros no solo están formados por neuronas. También los vigilan células inmunitarias que residen bien en el interior del tejido o en sus fronteras, donde el cerebro se encuentra con sus membranas protectoras y los vasos sanguíneos. Este estudio explora cómo distintos grupos de estos centinelas inmunitarios desaparecen y después vuelven a crecer, y muestra que la forma en que se reemplazan puede alterar la respuesta del cerebro a la inflamación y al ictus. Comprender este reingreso abre la puerta a terapias que modifiquen las células inmunitarias de la frontera sin perturbar el resto del cerebro.
Diferentes barrios, distintos centinelas cerebrales
Las células inmunitarias llamadas macrófagos ocupan “barrios” distintos en el sistema nervioso central. Las microglías viven dentro del propio tejido cerebral, mientras que los llamados macrófagos de frontera se sitúan a lo largo de las superficies del cerebro y alrededor de los vasos sanguíneos. Entre estas células de frontera, los macrófagos subdurales yacen justo por encima del tejido cerebral, abrazando la superficie y los espacios perivasculares, mientras que otro grupo puebla la membrana externa resistente llamada duramadre. Aunque estas poblaciones ayudan a supervisar y moldear las respuestas inmunitarias en el cerebro, tienen orígenes y longevidades diferentes, y trabajos previos sugirieron que la microglía puede mantenerse localmente sin ayuda de células procedentes de la sangre.
Resetear el sistema y observar cómo vuelve a crecer
Para ver cómo se recupera cada grupo de macrófagos tras ser eliminado, los investigadores usaron un fármaco que bloquea una señal de supervivencia clave y agota temporalmente estas células en ratones. A continuación siguieron cómo y de dónde regresaban las células empleando una combinación de ratones con “código de barras” genético, secuenciación de ARN a célula única, perfilado de cromatina y microscopía de alta resolución. Las microglías en el tejido cerebral se recuperaron rápidamente y casi por completo mediante la división de los supervivientes raros que escaparon a la depleción, y no hubo indicios de que células inmunitarias circulantes entraran a reemplazarlas. En contraste, los macrófagos subdurales en la superficie cerebral se repoblaron de forma lenta y desigual según la región, lo que sugiere que recurrían a fuentes adicionales más allá de las células residentes originales. 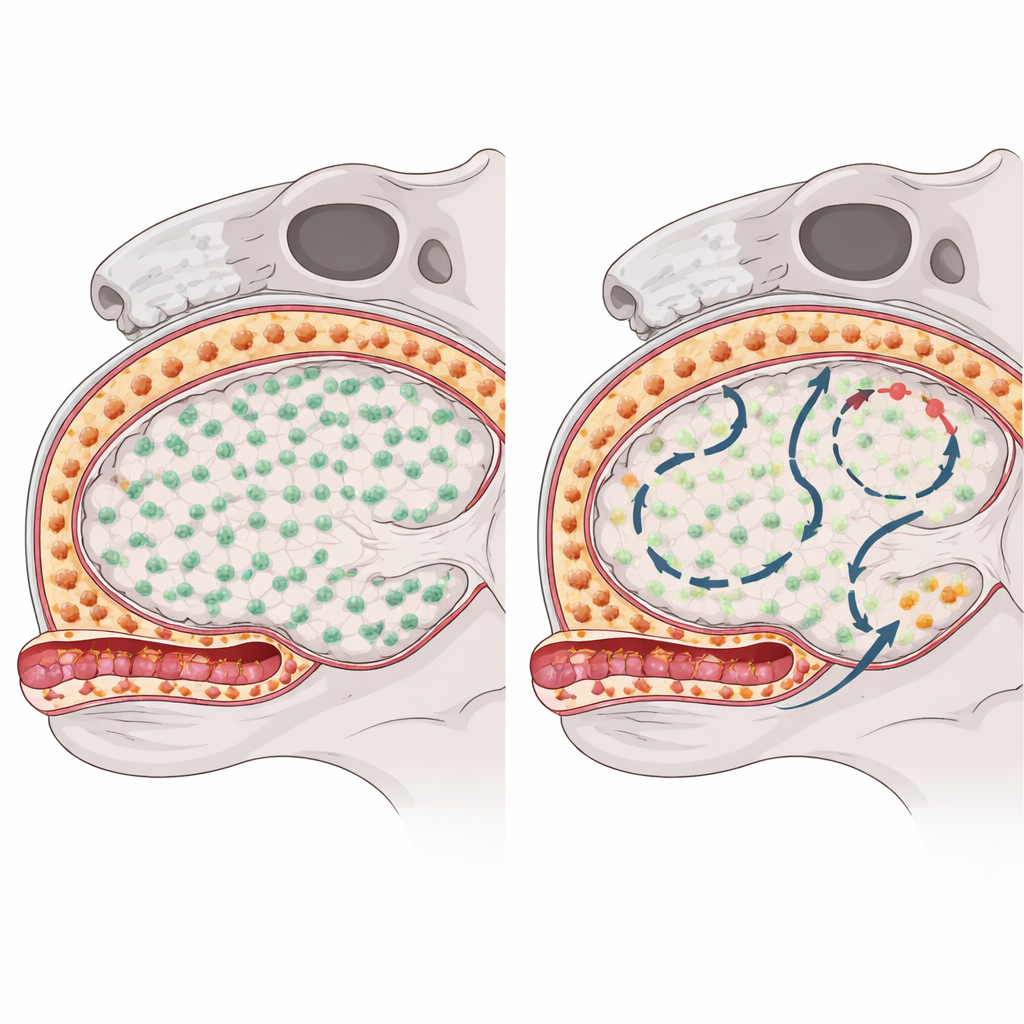
Cuando las células sanguíneas entran y permanecen
Experimentos de mapeo de destino mostraron que, a diferencia de la microglía, los macrófagos subdurales rellenaron parcialmente sus nichos usando monocitos de vida corta que circulan en la sangre. Tras la depleción, señales procedentes de células vasculares y del estroma crearon una ventana temporal en la que estos monocitos pudieron adherirse a las paredes vasculares activadas, desplazarse por ellas con la ayuda de moléculas de adhesión como ICAM‑1 y VCAM‑1, y asentarse en nichos perivasculares y superficiales. Bloquear estas vías de adhesión redujo el número de células entrantes, confirmando su importancia. Una vez implantados, los macrófagos de frontera derivados de monocitos no simplemente imitaban a las células de origen embrionario: conservaron un patrón distinto de expresión génica y de cromatina, estaban enriquecidos en moléculas implicadas en la presentación de antígenos y la adhesión celular, y permanecieron como una parte estable de la población mucho tiempo después de que la lesión inicial pareciera haberse resuelto.
Reconfiguración duradera de la inmunidad de frontera
La secuenciación a célula única y a granel reveló que la microglía recuperó en gran medida su perfil molecular original tras la repoblación, con cambios mínimos a largo plazo. Los macrófagos subdurales, sin embargo, se reequilibraron de forma duradera hacia un subtipo más “alerta” que expresaba niveles más altos de genes de activación inmunitaria. Al separar las células derivadas del embrión y las derivadas de monocitos mediante marcas genéticas, el equipo mostró que el origen durante el desarrollo condiciona fuertemente tanto la actividad génica como las regiones de ADN accesibles en estas células. Los macrófagos de frontera derivados de monocitos presentaban marcas epigenéticas típicas de células sanguíneas recientemente diferenciadas y mostraban mayor accesibilidad en genes implicados en la detección de patógenos e interacción con otras células inmunitarias. Cuando los animales fueron desafiados con componentes bacterianos, estas células recién llegadas desencadenaron respuestas inflamatorias y de estrés más intensas que sus vecinas de origen embrionario, mientras que las reacciones de la microglía y los macrófagos durales se vieron mucho menos alteradas. 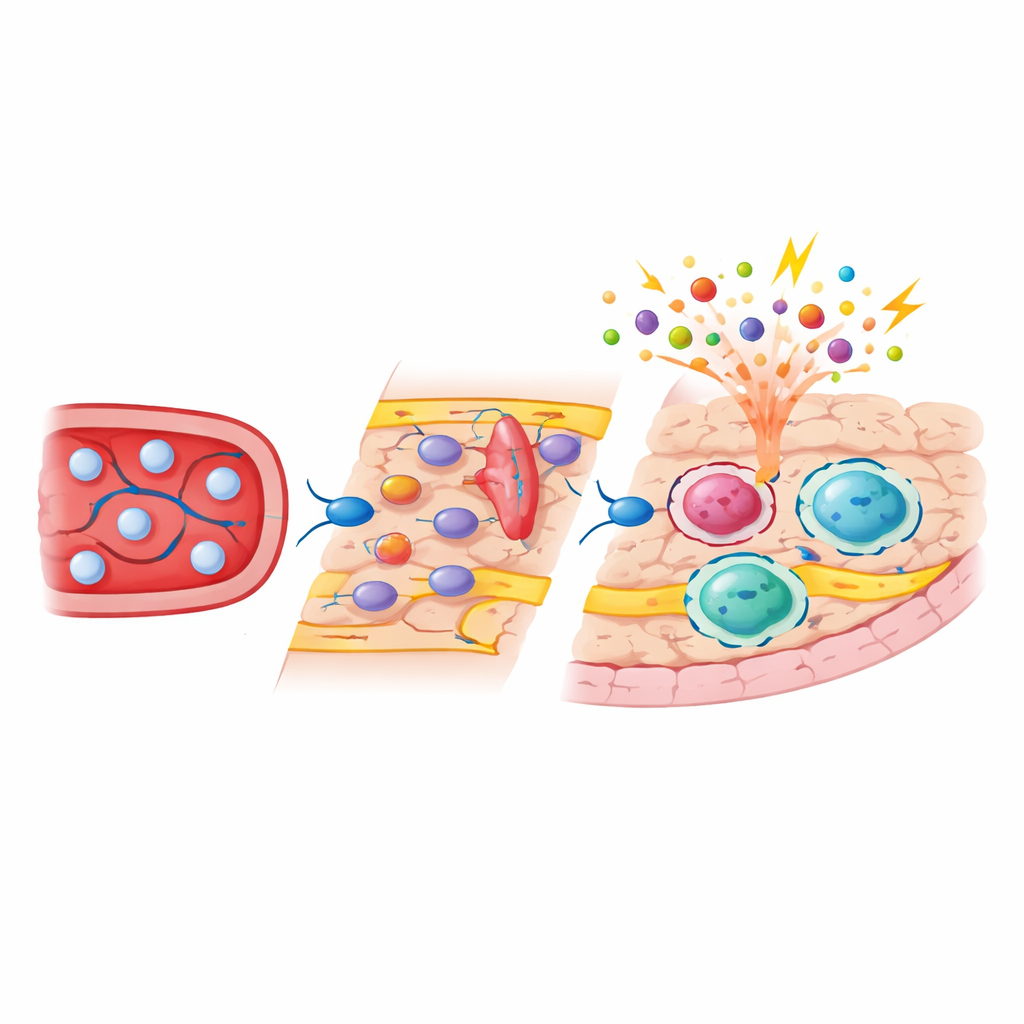
Consecuencias para el ictus y la salud cerebral
Los autores preguntaron después si esta remodelación oculta de los macrófagos de frontera afecta a la enfermedad. En un modelo de ictus isquémico, los ratones cuyos macrófagos subdurales habían sido repoblados se comportaron peor en pruebas de comportamiento, aunque el tamaño de la lesión y la reperfusión vascular fueron similares a los controles. El análisis de tejido completo y de macrófagos de frontera aislados mostró una inducción más intensa de genes vinculados a la inflamación, especies reactivas del oxígeno y disrupción de la barrera hematoencefálica en los animales repoblados. Las células de frontera derivadas de monocitos fueron especialmente reactivas, produciendo más quimiocinas y marcadores de activación tras el ictus. La imagen de la activación vascular confirmó una señal más alta de P‑selectina, un marcador de inflamación vascular intensa, que se correlacionó con una peor recuperación motora.
Qué significa esto para futuros tratamientos
Este trabajo muestra que no todos los macrófagos cerebrales son iguales y que reemplazarlos no equivale simplemente a reiniciar el sistema. La microglía puede reconstruirse silenciosamente a partir de las células supervivientes y volver a su actividad habitual. En cambio, los macrófagos de frontera en la superficie cerebral se convierten en una mezcla permanente de células originales de origen embrionario y nuevas llegadas desde la sangre, y esta población mixta responde con mayor agresividad a la inflamación sistémica y al ictus. Como los investigadores desarrollaron una forma de intercambiar selectivamente estas células de frontera sin afectar a la microglía, sus hallazgos apuntan a un futuro en el que las terapias podrían afinar las fronteras inmunitarias del cerebro —ya sea atenuando la inflamación nociva en trastornos como el ictus y la neurodegeneración o potenciando respuestas protectoras— sin alterar de forma global la red inmunitaria interna del cerebro.
Cita: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Palabras clave: macrófagos de las fronteras cerebrales, repoblación de microglía, implantación de monocitos, neuroinflamación, ictus isquémico