Clear Sky Science · ru
Различное происхождение и ниши определяют реактивность макрофагов ЦНС после репопуляции
Почему стражи на границе мозга важны
Наш мозг состоит не только из нервных клеток. Его также патрулируют иммунные клетки, которые располагаются либо глубоко в ткани, либо на её границах — там, где мозг встречается со своими защитными оболочками и кровеносными сосудами. В этом исследовании изучают, как разные группы этих иммунных стражей исчезают и затем восстанавливаются, и показывают, что способ их замены может изменить реакцию мозга на воспаление и инсульт. Понимание этого восстановления открывает путь к терапиям, которые тонко регулируют пограничные иммунные клетки, не нарушая остальную часть мозга.
Разные районы — разные стражи мозга
Иммунные клетки, называемые макрофагами, занимают отдельные «районы» в центральной нервной системе. Микроглия живёт внутри самой мозговой ткани, в то время как так называемые пограничные макрофаги располагаются вдоль поверхностей мозга и вокруг сосудов. Среди этих пограничных клеток субдуральные макрофаги лежат сразу над тканью мозга, прилегая к поверхности и периваскулярным пространствам, тогда как другая группа населяет плотную наружную оболочку — дуру. Хотя все эти популяции помогают контролировать и формировать иммунные ответы в мозге, у них разное происхождение и срок жизни, и предыдущие исследования указывали на то, что микроглия может поддерживать себя локально без помощи циркулирующих клеток крови.
Сброс системы и наблюдение за восстановлением
Чтобы увидеть, как каждая группа макрофагов восстанавливается после истребления, исследователи использовали препарат, блокирующий ключевой сигнал выживания и временно истощающий эти клетки у мышей. Затем они отслеживали, откуда и как клетки возвращаются, используя комбинацию генетических «штрих-кодов» у мышей, одноядерный РНК‑секвенсинг, профилирование хроматина и высокоразрешающую микроскопию. Микроглия в ткани мозга быстро восстановилась почти полностью за счёт деления редких выживших клеток, избежавших истощения, и не было признаков того, что циркулирующие иммунные клетки проникали в их ниши для замены. Напротив, субдуральные макрофаги на поверхности мозга репопулировали медленно и неравномерно по регионам, что намекало на привлечение дополнительных источников помимо исходных резидентных клеток. 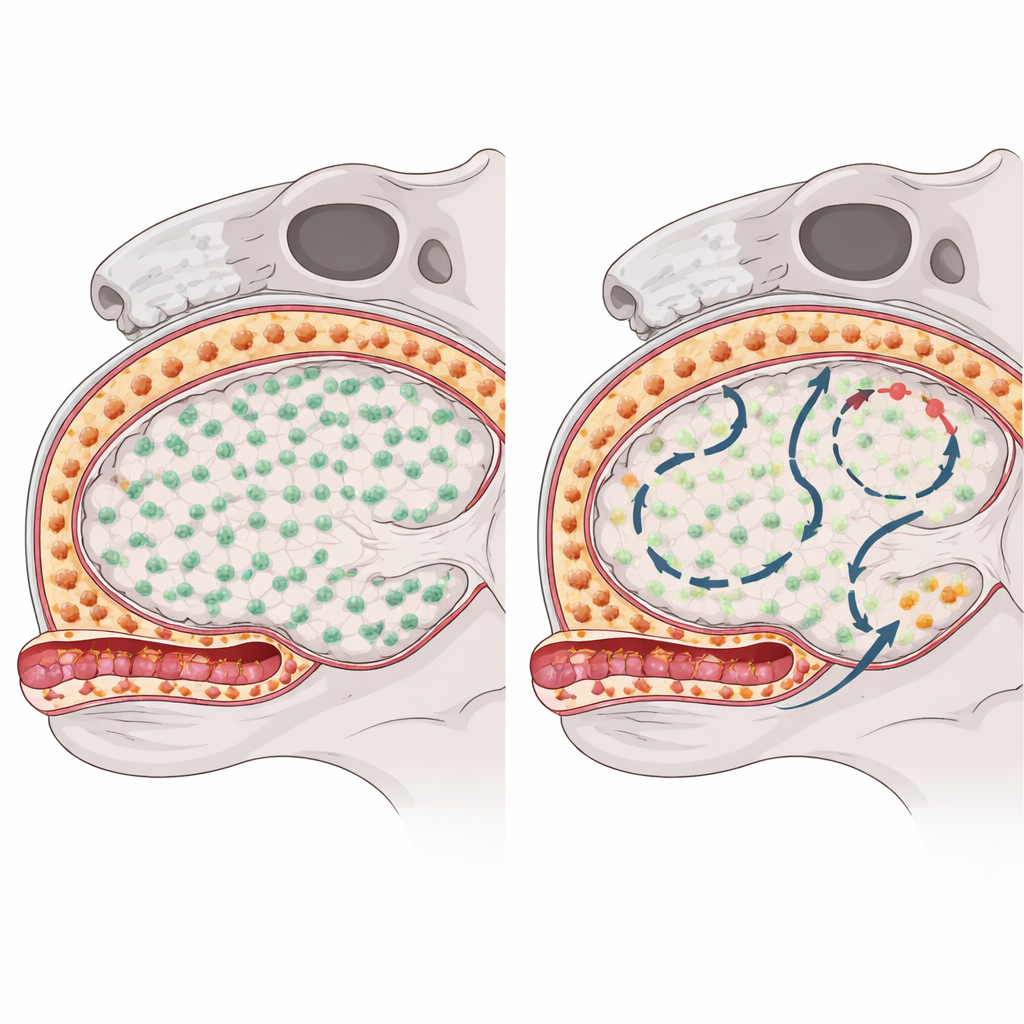
Когда клеток крови пускают внутрь и они остаются
Эксперименты по трассировке судьбы показали, что в отличие от микроглии, субдуральные макрофаги частично заполняют свои ниши за счёт короткоживущих моноцитов, циркулирующих в крови. После истощения сигналы от сосудистых и стромальных клеток создавали временное окно, в котором эти моноциты могли прилипать к активированным стенкам сосудов, переползать по ним с участием адгезивных молекул, таких как ICAM‑1 и VCAM‑1, и оседать в периваскулярных и поверхностных нишах. Блокирование этих адгезивных путей уменьшало количество входящих клеток, подтверждая их важность. После приживания макрофаги, происходящие от моноцитов, не просто клонировали исходные эмбрионально‑порожденные клетки: они сохраняли отличающийся профиль экспрессии генов и паттерн хроматина, были обогащены молекулами, участвующими в презентации антигена и клеточной адгезии, и оставались стабильной частью популяции долгое время после кажущегося заживления первоначальной травмы.
Длительная перенастройка пограничного иммунитета
Одноклеточные и массовые секвенирования показали, что микроглия в основном возвращала свой исходный молекулярный профиль после репопуляции с минимальными долгосрочными изменениями. Субдуральные макрофаги, однако, устойчиво сдвигались в сторону более «бдительного» подтипа, который экспрессировал более высокие уровни генов иммунной активации. Разделив эмбрионально‑порожденные и моноцитарно‑производные клетки с помощью генетических меток, команда показала, что развитие играет решающую роль в формировании и активности генов и доступных областей ДНК в этих клетках. Макрофаги пограничной зоны, происходящие от моноцитов, несут эпигенетические метки, типичные для недавно дифференцированных клеток крови, и демонстрируют повышенную доступность в генах, вовлечённых в распознавание патогенов и взаимодействие с другими иммунными клетками. При стимуляции бактериальными компонентами новоприбывшие клетки вызывали более сильные воспалительные и стрессовые ответы по сравнению с их эмбрионально‑порожденными соседями, тогда как реакции микроглии и дуральных макрофагов изменялись значительно меньше. 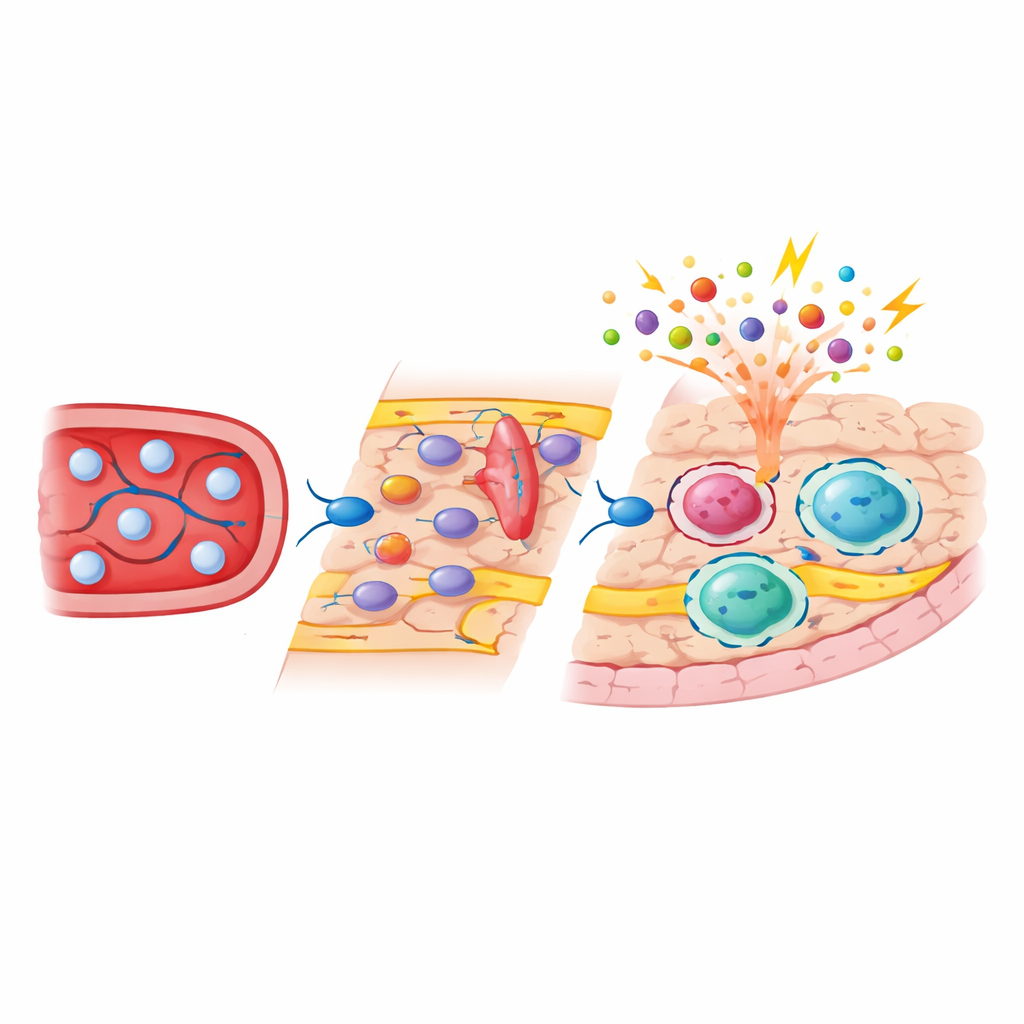
Последствия для инсульта и здоровья мозга
Затем авторы задали вопрос, влияет ли эта скрытая перестройка пограничных макрофагов на развитие болезни. В модели ишемического инсульта мыши с репопулированными субдуральными макрофагами показали худшую работу в поведенческих тестах, хотя размер очага и восстановление проходимости сосудов были сопоставимы с контролем. Анализ целой ткани и изолированных пограничных макрофагов выявил более сильную индукцию генов, связанных с воспалением, реактивными формами кислорода и нарушением гематоэнцефалического барьера у репопулированных животных. Макрофаги пограничной зоны, происходящие от моноцитов, были особенно реактивны, продуцируя больше хемокинов и маркеров активации после инсульта. Визуализация активации сосудов подтвердили более высокий сигнал для P‑селектина — маркёра интенсивного сосудистого воспаления, — который коррелировал с худшим восстановлением моторики.
Что это значит для будущих лечений
Эта работа показывает, что не все макрофаги мозга одинаковы, и что их замена не просто сбрасывает систему. Микроглия может тихо восстановиться из выживших клеток и вернуться к привычной работе. Напротив, пограничные макрофаги на поверхности мозга становятся постоянной смесью исходных эмбрионально‑порожденных клеток и новых пришельцев из крови, и эта смешанная популяция реагирует более агрессивно на системное воспаление и инсульт. Поскольку исследователи разработали способ избирательно обменивать эти пограничные клетки, не затрагивая микроглию, их результаты указывают на будущее, в котором терапии смогут точно настраивать иммунные границы мозга — либо снижая вредное воспаление при таких состояниях, как инсульт и нейродегенерация, либо усиливая защитные ответы — без глобального нарушения внутренней иммунной сети мозга.
Цитирование: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Ключевые слова: макрофаги пограничных областей мозга, репопуляция микроглии, приживание моноцитов, нейровоспаление, ишемический инсульт