Clear Sky Science · de
Unterschiedliche Herkunft und Nischen bestimmen die zelluläre Reaktionsfähigkeit von ZNS‑Makrophagen nach der Repopulation
Warum Wächter an den Hirnflächen wichtig sind
Unser Gehirn besteht nicht nur aus Nervenzellen. Es wird auch von Immunzellen überwacht, die entweder tief im Gewebe sitzen oder an seinen Grenzen, dort wo das Gehirn auf die schützenden Membranen und Blutgefäße trifft. Diese Studie untersucht, wie verschiedene Gruppen dieser immunologischen Wächter verschwinden und anschließend wieder nachwachsen, und zeigt, dass die Art ihrer Ersetzung verändern kann, wie das Gehirn auf Entzündungen und Schlaganfall reagiert. Das Verständnis dieses Nachwachsens eröffnet Wege zu Therapien, die Grenzimmunzellen gezielt beeinflussen, ohne den Rest des Gehirns zu stören.
Unterschiedliche Nachbarschaften, unterschiedliche Hirnwächter
Immunzellen, sogenannte Makrophagen, besetzen verschiedene „Nachbarschaften“ im zentralen Nervensystem. Mikroglia leben im eigentlichen Hirngewebe, während sogenannte Border‑Makrophagen entlang der Hirnoberflächen und um Blutgefäße herum sitzen. Unter diesen Grenzzellen liegen subdurale Makrophagen direkt über dem Hirngewebe und schmiegen sich an die Oberfläche und perivaskulären Räume, während eine andere Gruppe die harte Außenschicht, die Dura, besiedelt. Obwohl alle diese Populationen dazu beitragen, Immunantworten im Gehirn zu überwachen und zu formen, unterscheiden sie sich in Herkunft und Lebensdauer; frühere Arbeiten zeigten, dass Mikroglia sich lokal selbst erhalten können, ohne Hilfe blutgetragener Zellen.
Das System zurücksetzen und sein Nachwachsen beobachten
Um zu sehen, wie jede Makrophagen‑Gruppe sich nach einer Auslöschung erholt, setzten die Forschenden ein Medikament ein, das ein zentrales Überlebenssignal blockiert und diese Zellen bei Mäusen vorübergehend dezimiert. Anschließend verfolgten sie mit einer Kombination aus genetischen „Barcode“‑Mäusen, Einzelzell‑RNA‑Sequenzierung, Chromatinprofilierung und hochauflösender Mikroskopie, wie und wo die Zellen zurückkehrten. Mikroglia im Hirngewebe erholten sich schnell und nahezu vollständig durch Teilung der wenigen Überlebenden, die der Dezimierung entgangen waren; es gab keinen Hinweis darauf, dass zirkulierende Immunzellen sie ersetzten. Im Gegensatz dazu repopulierten subdurale Makrophagen an der Hirnoberfläche langsam und regional ungleichmäßig, was darauf hindeutet, dass sie zusätzliche Quellen jenseits der ursprünglich ansässigen Zellen anzapften. 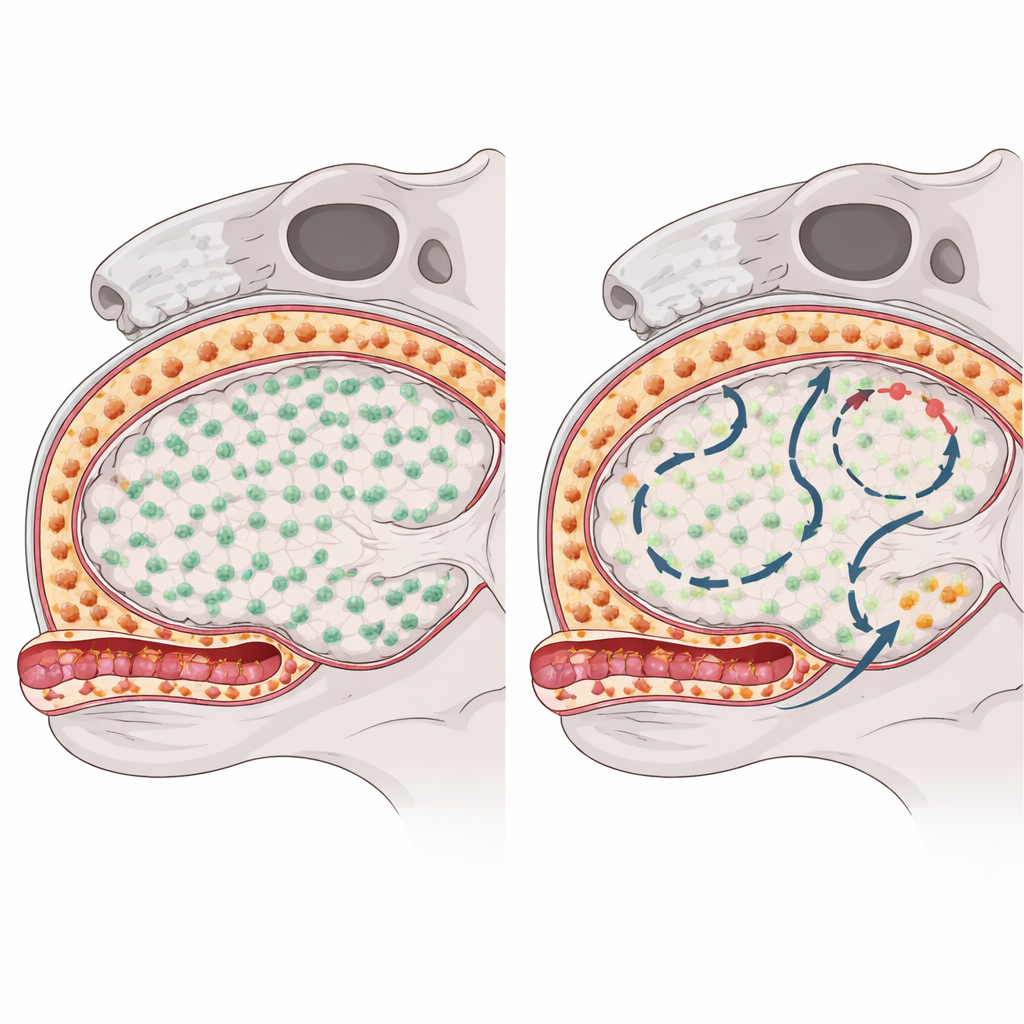
Wenn Blutzellen einwandern und bleiben
Fate‑Mapping‑Experimente zeigten, dass sich subdurale Makrophagen, im Gegensatz zu Mikroglia, teilweise aus kurzlebigen Monozyten auffüllten, die im Blut zirkulieren. Nach der Dezimierung schufen Signale aus Gefäß‑ und Stroma‑Zellen ein vorübergehendes Zeitfenster, in dem sich diese Monozyten an aktivierten Gefäßwänden anheften, mit Hilfe von Adhäsionsmolekülen wie ICAM‑1 und VCAM‑1 darüber hinwegkriechen und sich in perivaskuläre und oberflächennahe Nischen ansiedeln konnten. Die Blockade dieser Adhäsionswege verringerte die Zahl der einwandernden Zellen und bestätigte so deren Bedeutung. Einmal eingegliedert, imitierten monozyten‑abgeleitete Border‑Makrophagen nicht einfach die ursprünglichen, während der Embryonalentwicklung entstandenen Zellen: Sie behielten ein eigenständiges Genexpressions‑ und Chromatinmuster, wiesen eine Anreicherung von Molekülen für Antigenpräsentation und Zelladhäsion auf und blieben lange nach scheinbarer Heilung als stabiler Bestandteil der Population erhalten.
Lang anhaltende Umprogrammierung der Grenzimmunität
Einzelzell‑ und Bulk‑Sequenzierungen zeigten, dass Mikroglia nach der Repopulation weitgehend ihr ursprüngliches molekulares Profil wiedererlangten, mit nur minimalen langfristigen Veränderungen. Subdurale Makrophagen jedoch verschoben sich dauerhaft zugunsten eines eher „alarmierten“ Subtyps, der höhere Spiegel von Genen für Immunaktivierung exprimierte. Durch die Trennung von embryonal‑ und monozyten‑abgeleiteten Zellen mittels genetischer Marker demonstrierte das Team, dass die entwicklungsbedingte Herkunft sowohl die Genaktivität als auch die zugänglichen DNA‑Regionen in diesen Zellen stark prägte. Monozyten‑abgeleitete Border‑Makrophagen trugen epigenetische Kennzeichen, die typisch für kürzlich differenzierte Blutzellen sind, und zeigten eine erhöhte Zugänglichkeit an Genen, die an der Erkennung von Krankheitserregern und an Interaktionen mit anderen Immunzellen beteiligt sind. Als die Tiere mit bakteriellen Komponenten herausgefordert wurden, reagierten diese Neuankömmlinge mit stärkeren entzündlichen und Stress‑Antworten als ihre embryonal‑abgeleiteten Nachbarn, während die Reaktionen von Mikroglia und duralen Makrophagen deutlich weniger verändert waren. 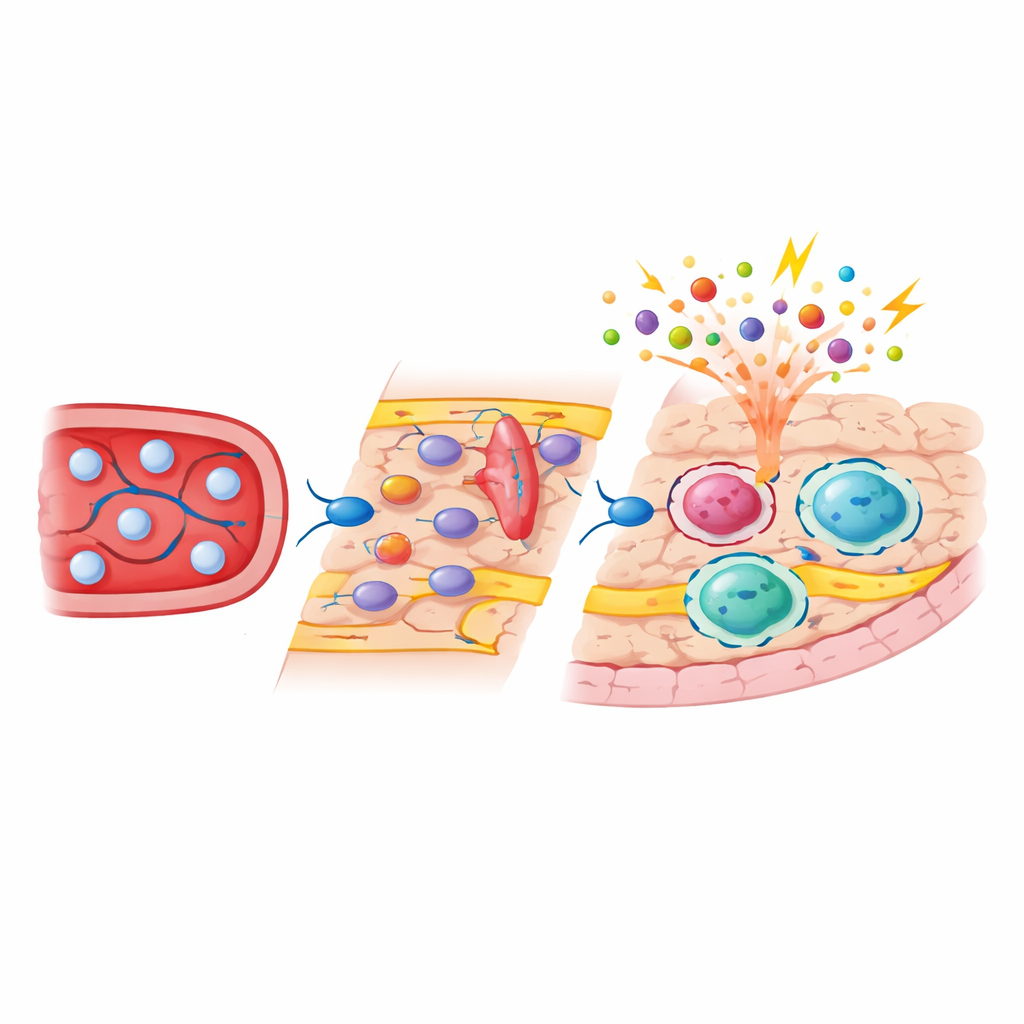
Folgen für Schlaganfall und Gehirngesundheit
Die Autorinnen und Autoren untersuchten dann, ob diese versteckte Umgestaltung der Border‑Makrophagen Krankheiten beeinflusst. In einem Modell des ischämischen Schlaganfalls schnitten Mäuse, deren subdurale Makrophagen repopuliert worden waren, in Verhaltensprüfungen schlechter ab, obwohl die Läsionsgröße und das Wiederöffnen der Gefäße den Kontrollen ähnlich waren. Analysen von Ganzgewebe und isolierten Border‑Makrophagen zeigten eine stärkere Induktion von Genen, die mit Entzündung, reaktiven Sauerstoffspezies und der Störung der Blut‑Hirn‑Schranke verknüpft sind, in repopulierten Tieren. Monozyten‑abgeleitete Border‑Zellen waren besonders reaktiv und produzierten nach dem Schlaganfall mehr Chemokine und Aktivierungsmarker. Bildgebende Untersuchungen der Gefäßaktivierung bestätigten ein stärkeres Signal für P‑Selectin, einen Marker intensiver vaskulärer Entzündung, das mit einer schlechteren motorischen Erholung korrelierte.
Was das für künftige Behandlungen bedeutet
Diese Arbeit zeigt, dass nicht alle Hirnmakrophagen gleich sind und dass ihre Ersetzung das System nicht einfach zurücksetzt. Mikroglia können sich still aus überlebenden Zellen neu aufbauen und zum gewohnten Zustand zurückkehren. Im Gegensatz dazu werden Border‑Makrophagen an der Hirnoberfläche zu einer dauerhaften Mischung aus ursprünglichen, embryonal‑abgeleiteten Zellen und Neuzugängen aus dem Blut, und diese gemischte Population reagiert aggressiver auf systemische Entzündungen und Schlaganfall. Da die Forschenden eine Methode entwickelten, um diese Border‑Zellen selektiv auszutauschen, während Mikroglia verschont blieben, weisen ihre Ergebnisse auf eine Zukunft hin, in der Therapien die immunologischen Grenzen des Gehirns feinjustieren könnten — entweder um schädliche Entzündungen bei Erkrankungen wie Schlaganfall und Neurodegeneration zu dämpfen oder um schützende Reaktionen zu verstärken — ohne das interne Immunnetzwerk des Gehirns global zu stören.
Zitation: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Schlüsselwörter: Makrophagen an Hirnbegrenzungen, Repopulation von Mikroglia, Monozyten‑Eingliederung, Neuroinflammation, ischämischer Schlaganfall