Clear Sky Science · pl
Różne pochodzenie i nisze determinują komórkową responsywność makrofagów OUN po odbudowie
Dlaczego strażnicy granic mózgu mają znaczenie
Nasze mózgi to nie tylko neurony. Patrolują je także komórki układu odpornościowego, które osiedlają się głęboko w tkance albo na jej granicach, tam gdzie mózg styka się z osłonkami i naczyniami krwionośnymi. Badanie to analizuje, jak różne grupy tych immunologicznych strażników znikają, a potem odrastają, i pokazuje, że sposób ich wymiany może zmieniać reakcję mózgu na zapalenie i udar. Zrozumienie tego odrastania otwiera drogę do terapii, które modulują komórki przygraniczne, nie naruszając pozostałej części mózgu.
Różne dzielnice, różni strażnicy mózgu
Komórki odpornościowe zwane makrofagami zajmują odmienne „dzielnice” w ośrodkowym układzie nerwowym. Mikroglej żyje wewnątrz tkanki mózgowej, podczas gdy tak zwane makrofagi przygraniczne osiedlają się wzdłuż powierzchni mózgu i wokół naczyń krwionośnych. Wśród tych przygranicznych komórek makrofagi podtwardówkowe leżą tuż nad tkanką mózgową, przylegając do powierzchni i przestrzeni okołonaczyniowych, podczas gdy inna grupa zasiedla twardą, zewnętrzną oponę zwaną durą. Chociaż wszystkie te populacje pomagają monitorować i kształtować odpowiedzi immunologiczne w mózgu, różnią się pochodzeniem i długością życia, a wcześniejsze badania sugerowały, że mikroglej potrafi utrzymać się lokalnie bez wsparcia komórek krążących we krwi.
Reset systemu i obserwacja odrostu
Aby zobaczyć, jak każda grupa makrofagów odbudowuje się po usunięciu, badacze użyli leku blokującego kluczowy sygnał przetrwania, co tymczasowo wyczerpało te komórki u myszy. Następnie śledzili, jak i skąd komórki się pojawiają, stosując kombinację genetycznych „kodów kreskowych”, sekwencjonowania RNA pojedynczych komórek, profilowania chromatyny oraz mikroskopii o wysokiej rozdzielczości. Mikroglej w tkance mózgowej odrósł szybko i niemal całkowicie dzięki podziałom rzadkich ocalałych komórek, które wymknęły się deplecji, i nie zaobserwowano przesiedlania komórek krążących z krwi. W przeciwieństwie do tego makrofagi podtwardówkowe na powierzchni mózgu odbudowywały się powoli i nierównomiernie między regionami, co sugeruje, że sięgały po dodatkowe źródła poza pierwotnymi rezydentami. 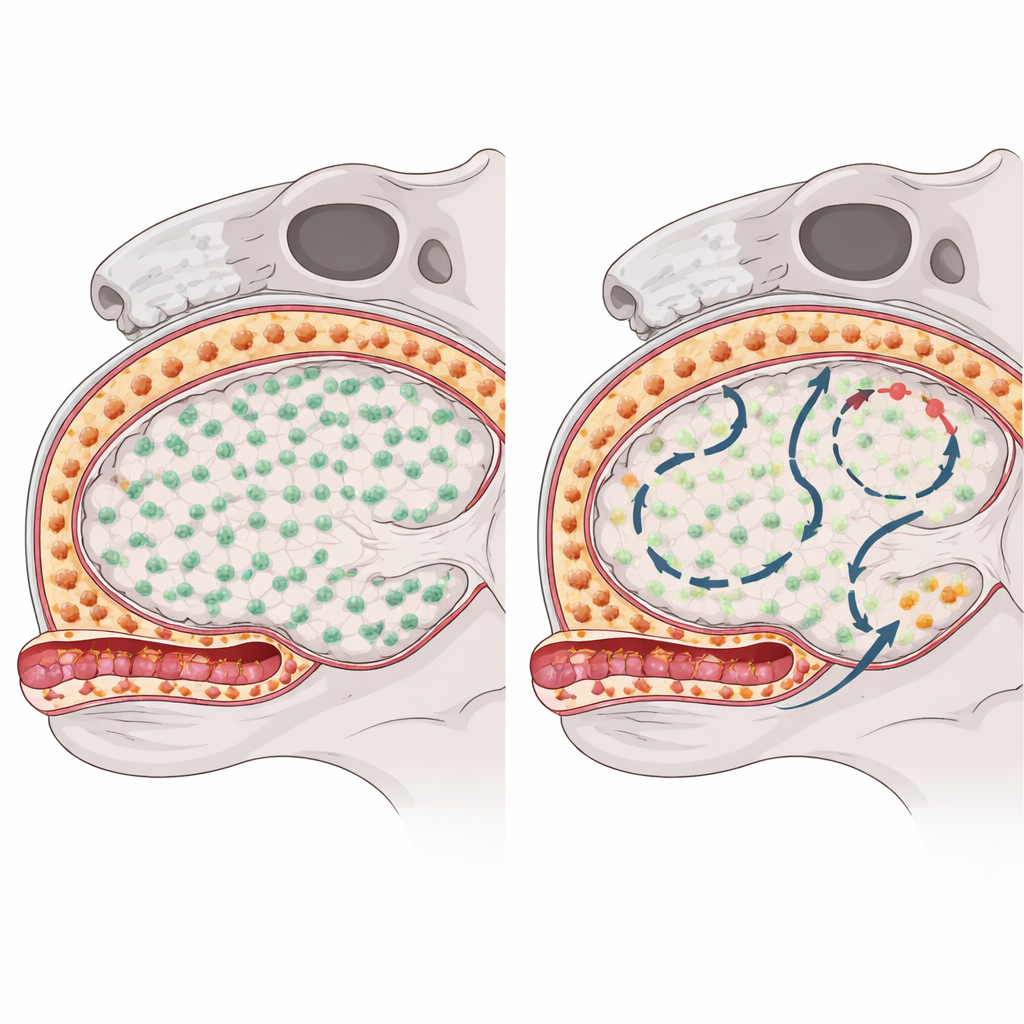
Gdy komórki krwi wkraczają i zostają
Eksperymenty mapowania losów wykazały, że w odróżnieniu od mikrogleju, makrofagi podtwardówkowe częściowo uzupełniały swoje nisze przy pomocy krótkotrwałych monocytów krążących we krwi. Po deplecji sygnały ze śródbłonka naczyń i komórek zrębu stworzyły tymczasowe okno, w którym te monocyty mogły przyczepiać się do aktywowanych ścian naczyń, przemieszczać się po nich z udziałem cząsteczek adhezji takich jak ICAM‑1 i VCAM‑1 i osiedlać w niszach okołonaczyniowych i powierzchniowych. Blokada tych dróg adhezyjnych zmniejszała liczbę napływających komórek, potwierdzając ich rolę. Po zasiedleniu makrofagi pochodzenia monocytarnego nie naśladowały po prostu dawnych komórek pochodzenia embrionalnego: zachowywały odmienny profil ekspresji genów i chromatyny, były wzbogacone w cząsteczki zaangażowane w prezentację antygenów i adhezję komórek oraz pozostały stabilną częścią populacji długo po ustąpieniu urazu.
Trwałe przestawienie odporności przygranicznej
Analizy pojedynczych komórek i sekwencjonowanie materiału z całej tkanki wykazały, że mikroglej w dużej mierze odzyskał swój pierwotny profil molekularny po odbudowie, z minimalnymi długotrwałymi zmianami. Makrofagi podtwardówkowe natomiast zostały trwale przesunięte w kierunku bardziej „czujnego” podtypu, który wykazywał wyższe poziomy genów związanych z aktywacją immunologiczną. Rozdzielając komórki pochodzenia embrionalnego i monocytarnego za pomocą etykiet genetycznych, zespół pokazał, że pochodzenie rozwojowe silnie kształtowało zarówno aktywność genów, jak i dostępne regiony DNA w tych komórkach. Makrofagi przygraniczne pochodzenia monocytarnego nosiły epigenetyczne ślady typowe dla niedawno zróżnicowanych komórek krwi i wykazywały zwiększoną dostępność przy genach zaangażowanych w wykrywanie patogenów oraz interakcje z innymi komórkami odpornościowymi. Gdy zwierzęta wystawiono na działanie bakterijnych składników, nowoprzybyłe komórki generowały silniejsze odpowiedzi zapalne i stresowe niż ich sąsiedzi pochodzenia embrionalnego, podczas gdy reakcje mikrogleju i makrofagów duralnych uległy znacznie mniejszym zmianom. 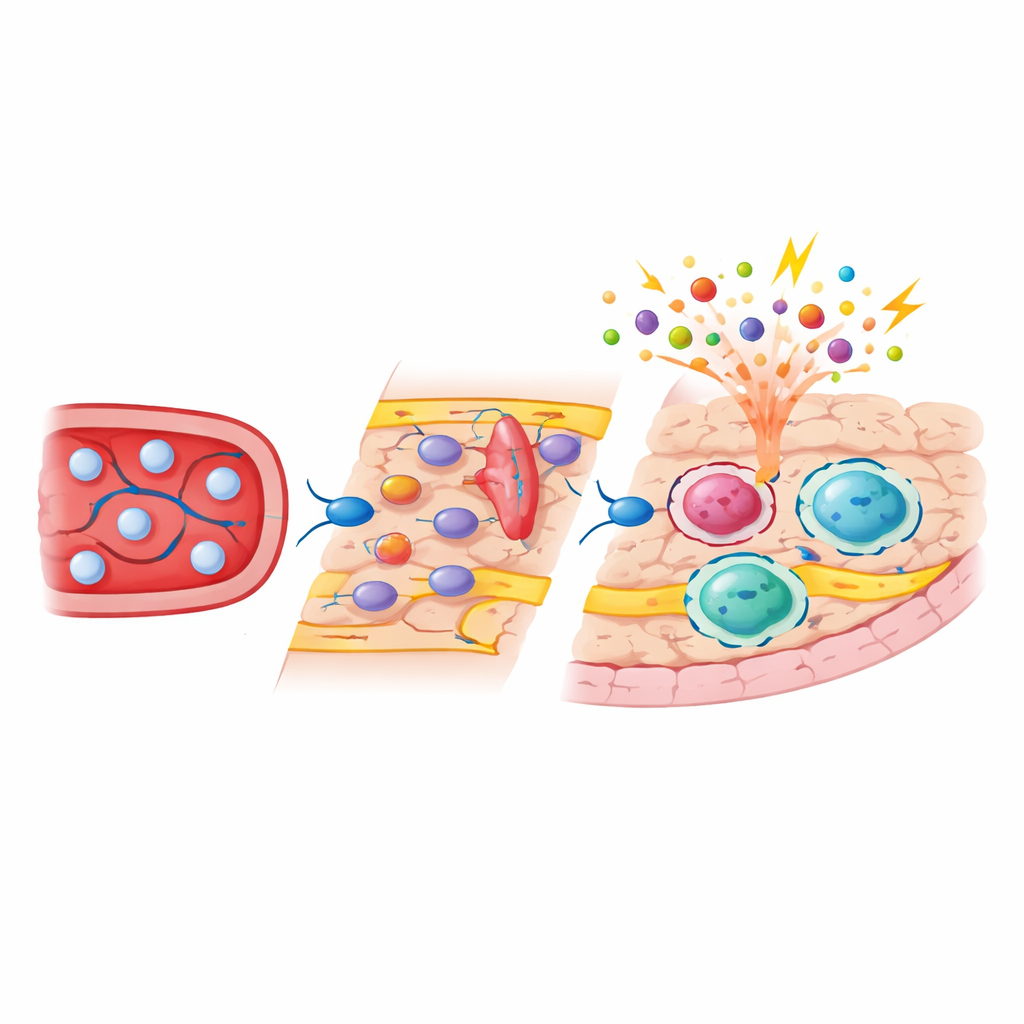
Konsekwencje dla udaru i zdrowia mózgu
Następnie autorzy zapytali, czy to ukryte przekształcenie makrofagów przygranicznych wpływa na chorobę. W modelu udaru niedokrwiennego myszy, których makrofagi podtwardówkowe zostały odbudowane, wypadły gorzej w testach behawioralnych, mimo że rozmiar ogniska uszkodzenia i przywrócenie przepływu w naczyniach były podobne do kontroli. Analiza całej tkanki i wyizolowanych makrofagów przygranicznych wykazała silniejszą indukcję genów powiązanych z zapaleniem, reaktywnymi formami tlenu i zaburzeniem bariery krew–mózg u zwierząt po repopulacji. Komórki przygraniczne pochodzenia monocytarnego były szczególnie reaktywne, produkując więcej chemokin i markerów aktywacji po udarze. Obrazowanie aktywacji naczyń potwierdziło wyższy sygnał dla P‑selektyny, markera intensywnego zapalenia naczyniowego, który korelował z gorszym powrotem sprawności ruchowej.
Co to oznacza dla przyszłych terapii
Ta praca pokazuje, że nie wszystkie makrofagi mózgu są takie same i że ich wymiana nie oznacza prostego zresetowania systemu. Mikroglej potrafi cicho odbudować się z ocalałych komórek i wrócić do poprzedniej funkcji. Natomiast makrofagi przygraniczne na powierzchni mózgu stają się stałą mieszaniną oryginalnych komórek pochodzenia embrionalnego i nowych przybyszów z krwi, a ta mieszana populacja reaguje bardziej agresywnie na zapalenie ogólnoustrojowe i udar. Ponieważ badacze opracowali sposób selektywnej wymiany tych przygranicznych komórek przy oszczędzeniu mikrogleju, ich wyniki wskazują na przyszłość, w której terapie będą mogły precyzyjnie regulować immunologiczną granicę mózgu — albo tłumiąc szkodliwe zapalenie w chorobach takich jak udar i neurodegeneracja, albo wzmacniając odpowiedzi ochronne — bez globalnego zakłócania wewnętrznej sieci odpornościowej mózgu.
Cytowanie: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Słowa kluczowe: makrofagi przygraniczne mózgu, odtwarzanie mikrogleju, zasiedlanie przez monocyty, neurozapalenie, udar niedokrwienny