Clear Sky Science · sv
Olika ursprung och nischer bestämmer CNS-makrofagers cellära respons efter återbefolkning
Varför hjärnans gränsvakter spelar roll
Våra hjärnor består inte endast av nervceller. De patrulleras också av immunceller som antingen sitter djupt inne i vävnaden eller vid dess gränser, där hjärnan möter sina skyddande hinnor och blodkärl. Denna studie undersöker hur olika grupper av dessa immunsensorer försvinner och sedan återväxer, och visar att sättet de ersätts på kan förändra hur hjärnan svarar på inflammation och stroke. Att förstå denna återväxt öppnar dörren för terapier som finjusterar gränsimmuniteten utan att rubba resten av hjärnan.
Olika kvarter, olika hjärnvakter
Immunceller som kallas makrofager uppehåller sig i skilda ”kvarter” i centrala nervsystemet. Mikroglia lever inne i hjärnvävnaden, medan så kallade gränsmakrofager sitter längs hjärnans ytor och runt blodkärl. Bland dessa gränsceller ligger subdurala makrofager precis ovanför hjärnvävnaden, anslutna till ytan och perivaskulära utrymmen, medan en annan grupp befolkar den hårda ytterhinnan som kallas dura. Trots att dessa populationer alla bidrar till att övervaka och forma immunsvar i hjärnan, har de olika ursprung och livslängd, och tidigare arbete antydde att mikroglia kan underhålla sig själva lokalt utan hjälp från blodburna celler.
Återställ systemet och följ återväxten
För att se hur varje makrofaggrupp återhämtar sig efter att ha raderats, använde forskarna ett läkemedel som blockerar en viktig överlevnadssignal och temporärt tömde dessa celler hos möss. De följde sedan hur och var cellerna återkom genom en kombination av genetiska ”streckkod”‑möss, single‑cell RNA‑sekvensering, kromatinprofilering och högupplöst mikroskopi. Mikroglia i hjärnvävnaden återhämtade sig snabbt och nästan helt genom delning från de få överlevare som undkom uttömningen, och det fanns inga tecken på att cirkulerande immunceller flyttade in för att ersätta dem. Tvärtom repopulerade subdurala makrofager på hjärnytan långsamt och ojämnt över regioner, vilket antyder att de drog nytta av ytterligare källor utöver de ursprungliga boende cellerna. 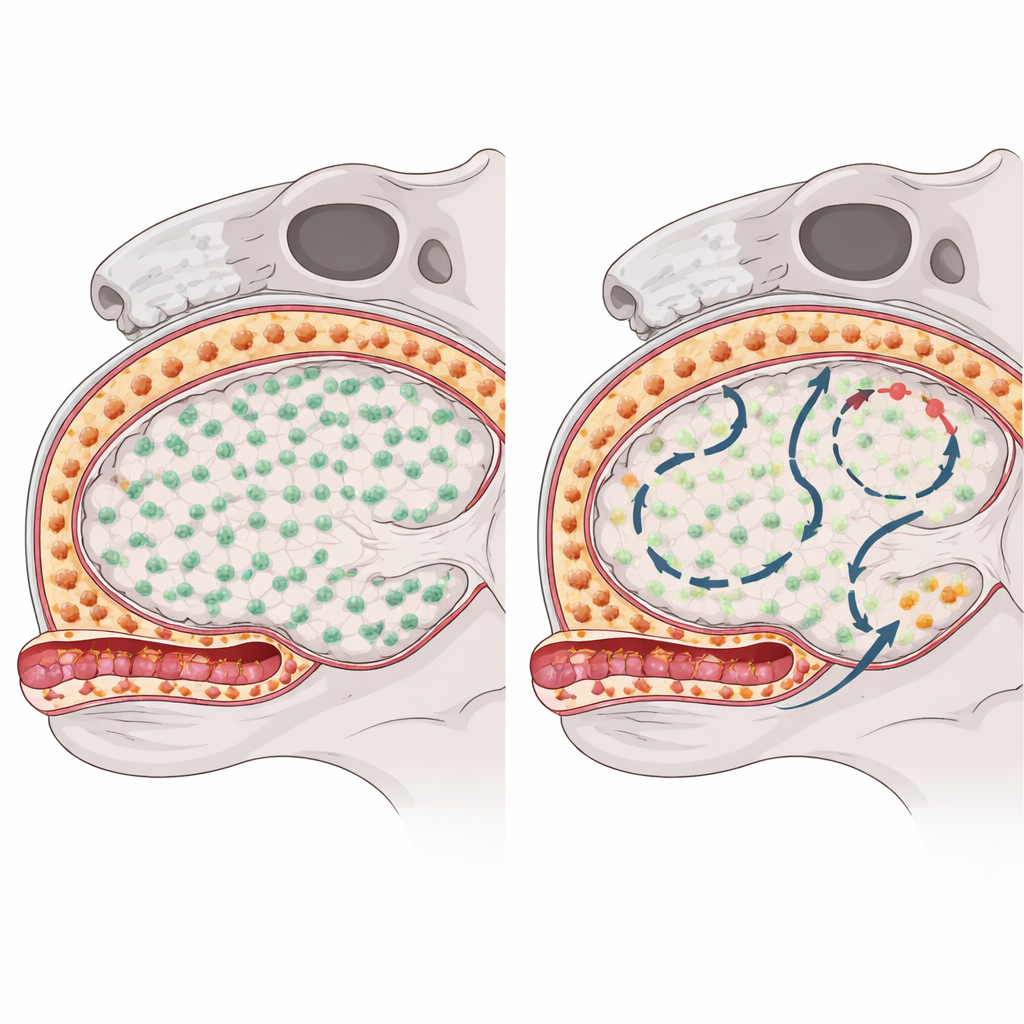
När blodceller flyttar in och stannar
SkicksMappings (fate‑mapping) visade att, till skillnad från mikroglia, fyllde subdurala makrofager delvis sina nischer med kortlivade monocyter som cirkulerar i blodet. Efter uttömningen skapade signaler från blodkärl och stromaceller ett temporärt fönster där dessa monocyter kunde fästa vid aktiverade kärlväggar, krypa över dem med hjälp av adhesionsmolekyler såsom ICAM‑1 och VCAM‑1 och slå sig ner i perivaskulära och ytliggande nischer. Blockering av dessa adhesionsvägar minskade antalet inkommande celler, vilket bekräftar deras betydelse. När de väl etablerat sig eftergick monocyt‑deriverade gränsmakrofager inte bara som kopior av de ursprungliga embryonalt härledda cellerna: de behöll ett distinkt genuttryck- och kromatinmönster, var berikade för molekyler som är involverade i antigenpresentation och celladhesion, och förblev en stabil del av populationen långt efter att den inledande skadan till synes läkt.
Varaktig omkoppling av gränsimmuniteten
Single‑cell och bulksekvensering visade att mikroglia till stor del återfick sin ursprungliga molekylära profil efter återbefolkning, med minimala långsiktiga förändringar. Subdurala makrofager däremot ombalanserades varaktigt mot en mer ”alert” undergrupp som uttryckte högre nivåer av immuaktiveringsgener. Genom att separera embryonalt härledda och monocyt‑deriverade celler med genetiska etiketter visade teamet att utvecklingsursprung starkt formade både genaktivitet och tillgängliga DNA‑regioner i dessa celler. Monocyt‑deriverade gränsmakrofager bar epigenetiska märkningar typiska för nyligen differentierade blodceller och visade ökad tillgänglighet vid gener som är involverade i att upptäcka patogener och interagera med andra immunceller. När djuren utmanades med bakteriella komponenter svarade dessa nykomna celler med starkare inflammatoriska och stressrelaterade reaktioner än sina embryonalt härledda grannar, medan mikroglia och durala makrofagers reaktioner var mycket mindre förändrade. 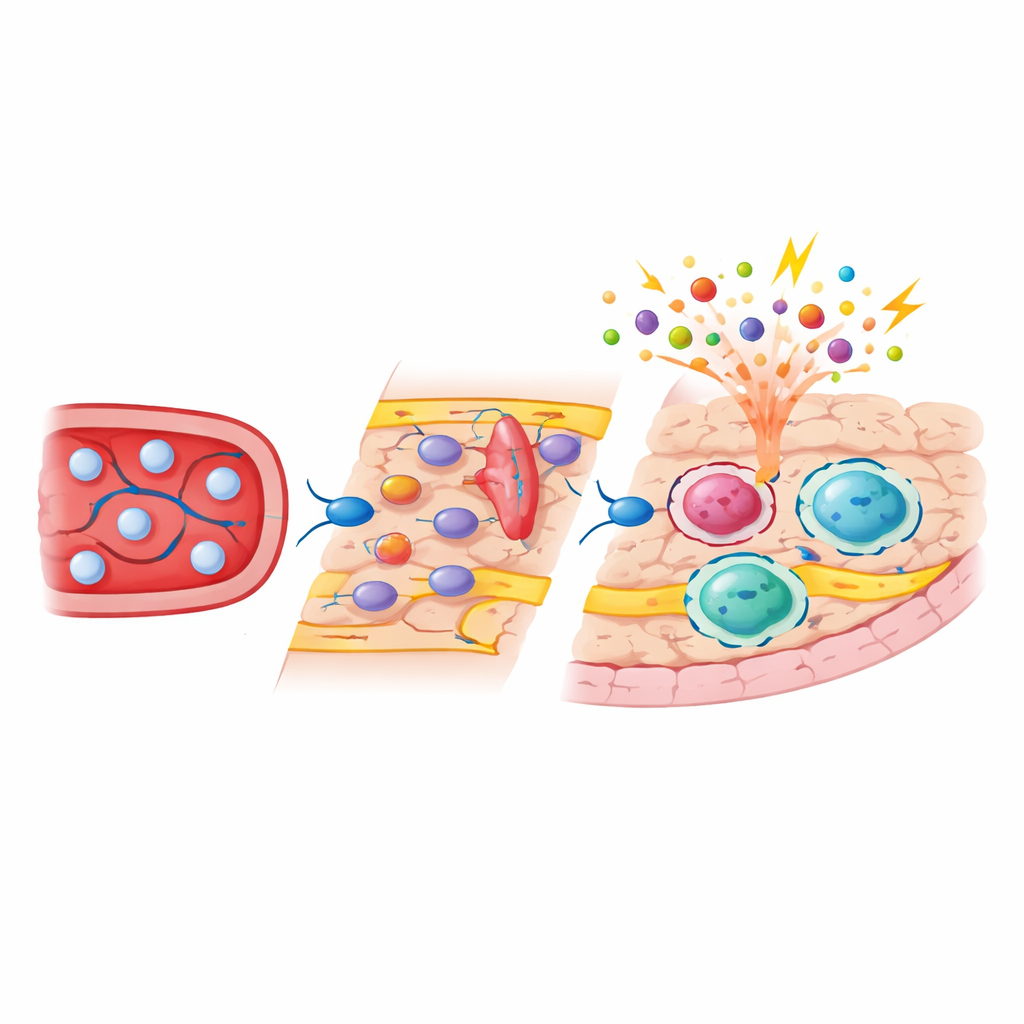
Konsekvenser för stroke och hjärnhälsa
Författarna frågade därefter om denna dolda omformning av gränsmakrofager påverkar sjukdom. I en modell för ischemisk stroke presterade möss vars subdurala makrofager hade återbefolkats sämre i beteendetester, trots att lesionstorlek och reperfusion av kärl var liknande kontroller. Analys av hel vävnad och isolerade gränsmakrofager visade starkare induktion av gener kopplade till inflammation, reaktiva syreradikaler och störning av blod‑hjärnbarriären hos återbefolkade djur. Monocyt‑deriverade gränsceller var särskilt reaktiva och producerade fler kemokiner och aktiveringsmarkörer efter stroke. Avbildning av kärlaktivering bekräftade en starkare signal för P‑selectin, en markör för intensiv vaskulär inflammation, vilket korrelerade med sämre motorisk återhämtning.
Vad detta innebär för framtida behandlingar
Detta arbete visar att inte alla hjärnmakrofager är likadana och att att ersätta dem inte bara återställer systemet. Mikroglia kan tyst återbygga sig från överlevande celler och återgå till sitt vanliga tillstånd. Däremot blir gränsmakrofager vid hjärnytan en permanent blandning av ursprungliga, embryonalt härledda celler och nya tillskott från blodet, och denna blandade population svarar mer aggressivt på systemisk inflammation och stroke. Eftersom forskarna utvecklade ett sätt att selektivt byta ut dessa gränsceller samtidigt som mikroglia sparades, pekar deras fynd mot en framtid där terapier kan finkalibrera hjärnans immungsgränser — antingen dämpa skadlig inflammation vid tillstånd som stroke och neurodegeneration eller förstärka skyddande svar — utan att globalt rubba hjärnans interna immunsystem.
Citering: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
Nyckelord: hjärnans gränsmakrofager, mikrogliaåterbefolkning, monocytengraftning, neuroinflammation, ischemisk stroke