Clear Sky Science · zh
断奶驱动通过微生物组介导的表观遗传调控以塑造小鼠的免疫记忆
为何首批固体食物至关重要
当婴儿——无论是小鼠还是人类——从母乳转向固体食物时,肠道会迎来更为丰富的微生物群落。这个新群落不仅帮助消化食物;它还发出信号,能够塑造机体长期的防御能力。这项在小鼠中的研究表明,断奶前后那段短暂时期像一个免疫“训练营”,肠道细菌通过在 DNA 上留下微妙化学痕迹来永久性地调整肠道细胞。若在此窗口期被打断,例如早期使用抗生素,可能削弱肠道防御,并增加日后肠道炎症和癌症的风险。
肠道微生物的变化历程
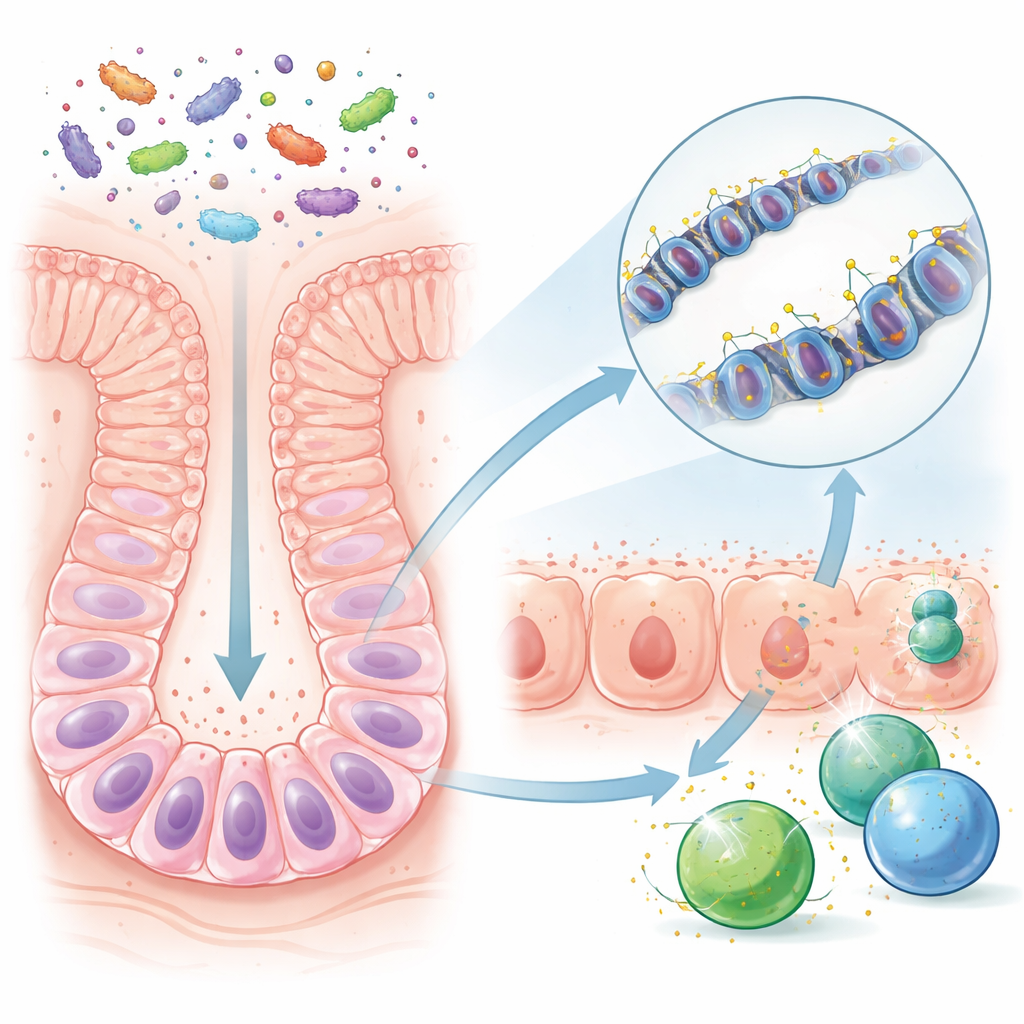
在断奶前,幼鼠的肠道相对简单,以母乳和有限的微生物群为营养来源。断奶后,新食物带来更多细菌种类和微生物代谢产物。研究者将在常规、微生物丰富环境中饲养的老鼠与无菌环境中饲养的老鼠进行了比较。他们关注寿命长的肠道干细胞,这些细胞不断再生肠道上皮。尽管这些细胞的总体 DNA 化学特征在有无微生物间看起来相似,但某些特定的 DNA 片段——作为邻近基因“音量旋钮”的调控区——在有微生物存在时明显不同。其中许多调控区位于参与识别和应答微生物的基因附近。

微生物如何在 DNA 上留下持久印记
研究团队发现,断奶后干细胞中某些 DNA 调控区失去了名为甲基的小化学标签。这种“去甲基化”尤其发生在调控用于向免疫细胞呈递微生物片段的基因的位点。一旦这些调控区被去除甲基标签,这种改变就在干细胞分裂并分化为日常肠上皮细胞的过程中被传递下去。因此,暴露于微生物的成年肠上皮细胞被预设为能更快地激活防御基因,即便在最初的断奶期过去很久之后也是如此。相比之下,无菌小鼠或仅在生命后期被定植的鼠,未能在同等程度上形成这种持久的预设状态。
短暂信号的长期影响
是什么驱动了这些 DNA 变化?在断奶期间,扩展的微生物群会激发一波短暂的炎性信使,包括一种叫做干扰素-γ的分子。作者在断奶后不久阻断了这种信号,发现关键的去甲基化和基因预设大多消失;而在成年时阻断则几乎无影响。在体外培养的小型肠道“类器官”中,暴露于低剂量的干扰素-γ就足以触发快速去甲基化并长期维持关键基因的准备状态。经过这种处理后,类器官对随后挑战的反应更快更强,甚至对不同类型的信号也表现出增强响应——这类似于肠上皮的训练记忆行为。
抗生素、缺失的微生物与脆弱的肠道
研究还测试了当这一早期节律被抗生素干扰时会发生什么。从产前到断奶期给予低剂量青霉素的鼠总体仍保留许多微生物,但失去了特定的革兰氏阳性细菌群体,这些细菌是干扰素-γ的强烈刺激者并产生有助于 DNA 去甲基化的代谢物。这些小鼠在关键调控区显示出更高的 DNA 甲基化、肠上皮中抗原呈递基因的表达降低,以及产生干扰素-γ的免疫细胞减少。在后来暴露于诱导结肠炎的化学物质时,它们发展出更严重、更持久的疾病,并且更容易形成结肠肿瘤。
这对终生肠道健康意味着什么
综合来看,这项工作将断奶后时期描绘为一个狭窄但强有力的窗口期,在此期间由饮食驱动的肠道微生物变化在肠道干细胞上留下持久的印记。这些表观遗传标记并不会持续性地让免疫基因过度活跃;相反,它们使系统保持警觉,随时准备对未来威胁做出迅速且平衡的应答。通过延迟定植或广谱使用抗生素干扰这种早期微生物训练,可能破坏这种内在记忆,使肠道更容易发生慢性炎症和癌变。尽管该研究在小鼠中进行,但它提出了关于婴儿喂养选择、以微生物为目标的疗法以及早期抗生素暴露如何在数十年内影响人类肠道健康的重要问题。
引用: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
关键词: 肠道微生物组, 断奶, 表观遗传记忆, 肠道免疫, 早期抗生素