Clear Sky Science · ar
الفطام يدفع تنظيمًا إبجينيتكيًا بوساطة الميكروبيوم لتشكيل ذاكرة مناعية لدى الفئران
لماذا تهم الوجبات الصلبة الأولى
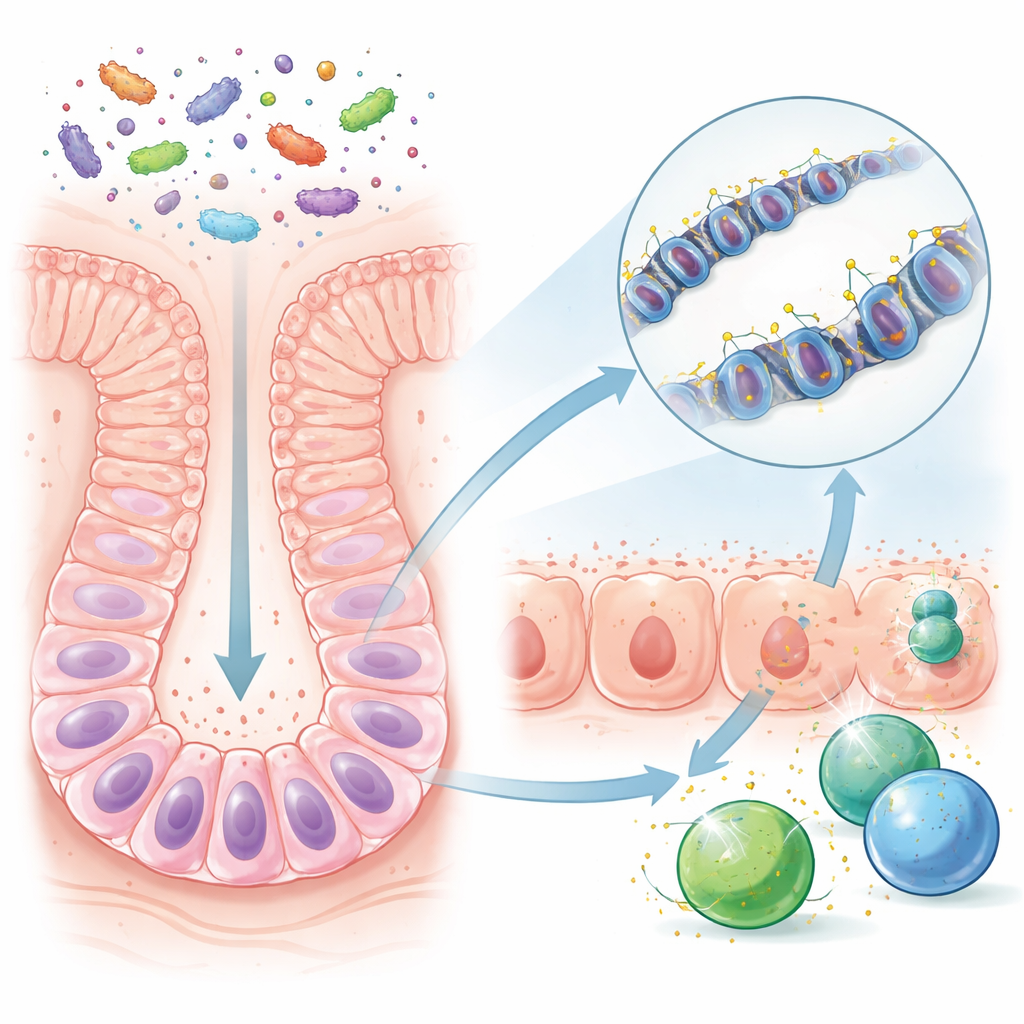
عندما ينتقل رضيع—فأر أو إنسان—من الحليب إلى الغذاء الصلب، تصبح أمعاؤه موطناً لمجتمع ميكروبي أكثر ثراءً. هذا المجتمع الجديد لا يساعد فقط في هضم الطعام؛ بل يرسل إشارات تستطيع أن تشكّل دفاعات الجسم مدى الحياة. تظهر هذه الدراسة على الفئران أن الفترة القصيرة المحيطة بالفطام تعمل مثل «معسكر تدريب» مناعي، حيث تضبط البكتيريا المعوية خلايا الأمعاء بشكل دائم عبر علامات كيميائية دقيقة على الحمض النووي. إفساد هذه النافذة، مثلاً بواسطة المضادات الحيوية المبكرة، يمكن أن يضعف دفاعات الأمعاء ويزيد خطر الالتهاب المعوي والسرطان لاحقًا.
حياة الميكروبات المتغيرة
قبل الفطام، يكون جهاز أمعاء الفأر الصغير بسيطًا إلى حد ما، تغذيه لبن الأم ومجموعة محدودة من الميكروبات. بعد الفطام، تجلب الأطعمة الجديدة أعدادًا أكبر من أنواع البكتيريا ومنتجات ميكروبية متنوعة. قارن الباحثون فئرانًا تربت في ظروف عادية غنية بالميكروبات مع فئرانٍ خالية من الجراثيم. ركزوا على خلايا جذعية معوية طويلة العمر، تعيد تجديد بطانة الأمعاء باستمرار. على الرغم من أن الكيمياء العامة للحمض النووي في هذه الخلايا بدت متشابهة بوجود الميكروبات أو بدونها، فإن مقاطع محددة من الحمض النووي—مناطق ضابطة تعمل كمفاتيح تحكم للجينات المجاورة—كانت مختلفة بوضوح عند وجود الميكروبات. وجدت العديد من هذه المناطق قرب جينات مشاركة في التعرف على الميكروبات والاستجابة لها.

كيف تكتب الميكروبات ملاحظات دائمة على الحمض النووي
وجد الفريق أنه بعد الفطام، فقدت مناطق ضبطٍ معينة في الحمض النووي داخل الخلايا الجذعية علامات كيميائية صغيرة تسمى مجموعات الميثيل. حدث هذا «إزالة الميثلة» خصوصًا في مواضع تنظم جينات تستخدم لعرض شظايا ميكروبية على الخلايا المناعية. ومتى ما جُرِّدت هذه المناطق من علامات الميثيل، انتقلت التغييرات مع انقسام الخلايا الجذعية ونضوجها إلى الخلايا الاعتيادية التي تبطن الأمعاء. نتيجة لذلك، كانت خلايا الأمعاء البالغة في الفئران المعرضة للميكروبات متهيِّئة لتفعيل جينات الدفاع بسرعة، حتى بعد مرور وقت طويل على فترة الفطام. بالمقابل، فشلت الفئران الخالية من الجراثيم، أو التي استعمرت أمعاؤها في وقت لاحق من الحياة، في تطوير هذا التأهب الدائم إلى نفس الدرجة.
دفعة إشارات قصيرة الأمد ذات تأثير طويل الأمد
ما الذي يدفع هذه التغيرات في الحمض النووي؟ خلال الفطام، تثير الميكروبيوم المتوسعة موجة قصيرة المدى من الرسائل الالتهابية، بما في ذلك جزيء يُدعى إنترفيرون-غاما. حجب المؤلفون هذا الإشارة في فئران صغيرة مباشرة بعد الفطام فوجدوا أن إزالة الميثلة الحيوية والتأهب الجيني الحاسم اختفت إلى حد كبير؛ أما حجبها في البالغين فكان له تأثير ضئيل. في «أورغانويدات» معوية صغيرة نمت في أطباق، كان التعرض لمستويات منخفضة من إنترفيرون-غاما كافيًا لتحفيز إزالة ميثلة سريعة واستعداد طويل الأمد للجينات الرئيسية. بعد هذا المعالجة، استجابت الأورغانويدات بشكل أسرع وأقوى للتحديات اللاحقة، حتى لإشارات من أنواع مختلفة—سلوك شبيه بالذاكرة المدربة في بطانة الأمعاء.
المضادات الحيوية، الميكروبات المفقودة، وأمعاء عرضة للخطر
اختبرت الدراسة أيضًا ما يحدث عندما يتعطل هذا التنسيق المبكر بواسطة المضادات الحيوية. الفئران التي أعطيت جرعة منخفضة من البنسيلين من قبل الولادة وحتى الفطام احتفظت بالعديد من الميكروبات عمومًا لكنها فقدت مجموعات محددة من البكتيريا موجبة الغرام التي تعد محفزات قوية لإنترفيرون-غاما ومنتجة لمستقلبات تساعد على إزالة ميثلة الحمض النووي. أظهرت هذه الفئران مستويات ميثلة أعلى في مناطق الضبط الحاسمة، وتعبيرًا أضعف لجينات عرض المستضد في بطانة الأمعاء، وعددًا أقل من الخلايا المناعية المنتجة لإنترفيرون-غاما. عند تعرضها لاحقًا لمادة كيميائية تحفز التهاب القولون، طورت أمراضًا أكثر شدة واستمرارًا، وكانت أكثر عُرضة لأورام القولون.
ماذا يعني هذا لصحة الأمعاء مدى الحياة
من خلال تجميع النتائج، تصوّر الدراسة فترة ما بعد الفطام كنافذة ضيقة لكنها قوية، تترك فيها التغيرات الغذائية في الميكروبيوم علامات دائمة على الخلايا الجذعية المعوية. هذه العلامات الإبجينية لا تدفع باستمرار جينات المناعة إلى الإفراط في النشاط؛ بل تبقي النظام على أهبة الاستعداد، جاهزًا لتقديم استجابة سريعة ومتوازنة للتهديدات المستقبلية. يمكن أن يضعف التدخل في هذا التدريب الميكروبي المبكر—من خلال استعمار متأخر أو استخدام واسع للمضادات الحيوية—هذه الذاكرة المدمجة ويجعل الأمعاء أكثر عرضة للالتهاب المزمن والسرطان. على الرغم من أن الدراسة أُجريت على الفئران، فإنها تثير أسئلة مهمة حول كيف يمكن لخيارات تغذية الرضع، والعلاجات المستهدفة للميكروبيوم، والتعرض المبكر للمضادات الحيوية أن تشكّل صحة الأمعاء البشرية لعقود.
الاستشهاد: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
الكلمات المفتاحية: ميكروبيوم الأمعاء, الفطام, الذاكرة الإبجينية, المناعة المعوية, المضادات الحيوية في مرحلة الحياة المبكرة