Clear Sky Science · ja
離乳が腸内微生物を介したエピジェネティック制御を駆動し、マウスの免疫記憶を形成する
最初の固形食が重要な理由
母乳から固形食へ移行するとき、マウスでも人間でも腸内ははるかに多様な微生物の住処になります。この新しいコミュニティは食事の消化を助けるだけでなく、生涯にわたって身体の防御機構を形作るシグナルを送ります。本研究はマウスで、離乳前後の短い時期が免疫の「訓練場」のように働き、腸内細菌がDNA上の微細な化学的印(エピジェネティックマーク)を通じて腸の細胞を恒久的に調整することを示しています。この窓を、例えば早期の抗生物質で妨げると、腸の防御が弱まり、のちの炎症性腸疾患やがんのリスクが高まる可能性があります。
変わる腸内微生物の暮らし
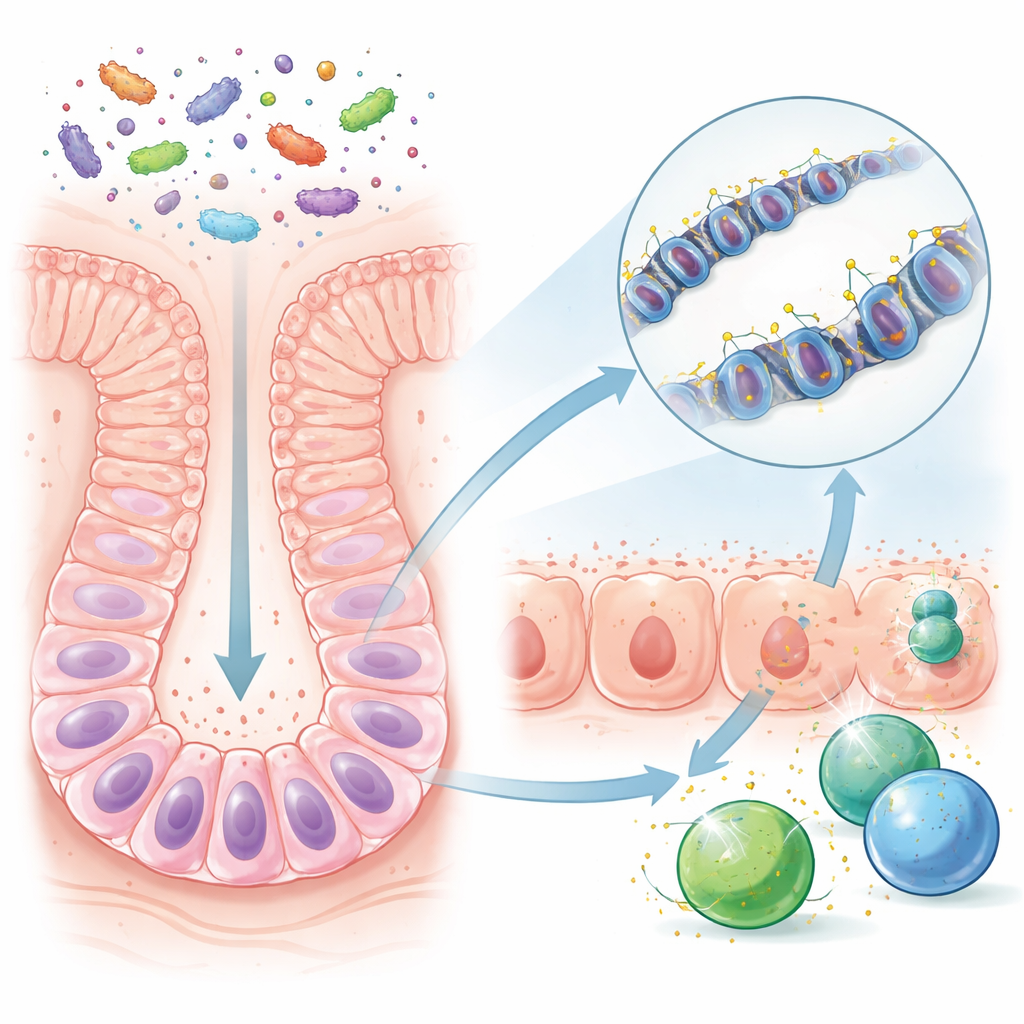
離乳前の幼いマウスの腸は比較的単純で、母乳と限られた微生物群に支えられています。離乳後、新しい食物が多くの細菌種や微生物産物をもたらします。研究者たちは通常の微生物に富んだ条件で育てたマウスと無菌で育てたマウスを比較しました。注目したのは腸の上皮を継続的に再生する長寿命の腸幹細胞です。これらの細胞全体のDNA化学(メチル化など)は微生物の有無で大きく変わらないように見えましたが、特定のDNA領域――近傍の遺伝子の「音量つまみ」のように機能する制御領域――は微生物が存在する場合に目に見えて異なっていました。これらの多くは微生物を認識し応答する遺伝子の近傍に位置していました。

微生物がDNAに残す持続的な記録の仕組み
研究チームは、離乳後に幹細胞の特定のDNA制御領域が小さな化学タグであるメチル基を失うことを発見しました。この「脱メチル化」は、微生物断片を免疫細胞に提示するために使われる遺伝子を制御する部位で特に顕著でした。一度これらの領域からメチルタグが除かれると、その変化は幹細胞が分裂して腸の常在細胞へと成熟する過程で受け継がれます。その結果、微生物暴露を受けた成体の腸細胞は、防御遺伝子を迅速に立ち上げるように準備され、離乳期が過ぎても長期間にわたり速やかな応答が可能になります。対照的に、無菌マウスや生後に腸が後から植え付けられたマウスは、このような持続的な準備状態を同程度には形成できませんでした。
短期の信号が長期に影響を残す
これらのDNA変化を引き起こすのは何でしょうか。離乳期には、拡大するマイクロバイオームが短期間の炎症性メッセンジャーの波を引き起こし、その中にインターフェロンγという分子が含まれます。著者らが離乳直後の若いマウスでこのシグナルを遮断すると、重要な脱メチル化と遺伝子の準備状態はほとんど消失しましたが、成人で遮断してもほとんど影響はありませんでした。培養皿内で育てたミニ腸「オルガノイド」では、低濃度のインターフェロンγに曝露するだけで急速な脱メチル化と主要遺伝子の長期にわたる準備状態が誘導されました。こうした処置を受けたオルガノイドは、後の刺激に対して、たとえ種類の異なるシグナルでも、より速く強く反応するようになり、腸上皮の訓練された記憶に似た振る舞いを示しました。
抗生物質、欠けた微生物、脆弱な腸
研究ではまた、この幼少期の協調的変化が抗生物質で乱されたときに何が起きるかも調べました。出生前から離乳まで低用量ペニシリンを与えたマウスは全体として多くの微生物を保持したものの、インターフェロンγの強力な刺激因子であり、DNA脱メチル化を助ける代謝物を産生するグラム陽性菌の特定の群を失いました。これらのマウスは重要な制御領域でDNAメチル化が高く、腸上皮における抗原提示関連遺伝子の発現が弱く、インターフェロンγを産生する免疫細胞も少なくなっていました。その後、結腸炎を誘導する化学物質に曝露すると、より重篤で長引く病態を示し、結腸腫瘍を生じやすくなっていました。
生涯にわたる腸の健康にとっての意味
総じて、この研究は離乳後の時期を狭くも強力な窓として描き、食事による腸内微生物の変化が腸幹細胞に持続的な刻印を残すことを示しています。これらのエピジェネティックな刻印は免疫遺伝子を常時過剰に駆動するわけではなく、むしろ将来の脅威に対して迅速かつバランスの取れた応答を行えるようにシステムを警戒状態に保ちます。定着の遅延や広範な抗生物質使用によってこの早期の微生物による訓練が妨げられると、この組み込みの記憶が損なわれ、慢性炎症やがんに対する感受性が高まる可能性があります。本研究はマウスで行われたものですが、乳児の授乳選択、マイクロバイオームを標的とした治療、早期の抗生物質曝露が人間の腸の健康を何十年も先まで形作るかもしれないという重要な問題を提起します。
引用: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
キーワード: 腸内マイクロバイオーム, 離乳, エピジェネティック記憶, 腸の免疫, 幼少期の抗生物質