Clear Sky Science · sv
Avvänjning driver mikrobiombaserad epigenetisk reglering för att forma immunminnet hos möss
Varför de första fasta måltiderna spelar roll
När en unge—mus eller människa—går från mjölk till fast föda blir tarmen hem för ett mycket rikare samhälle av mikrober. Detta nya samhälle hjälper inte bara till att smälta maten; det skickar signaler som kan forma kroppens försvar för livet. Studien i möss visar att den korta period som omger avvänjningen fungerar som ett immunologiskt ”träningsläger”, där tarmbakterier permanent ställer in tarmceller genom subtila kemiska markörer på DNA. Att störa detta fönster, till exempel med tidiga antibiotikabehandlingar, kan försvaga tarmförsvaret och öka risken för inflammation i tarmen och cancer senare i livet.
Tarmmikrobernas föränderliga liv
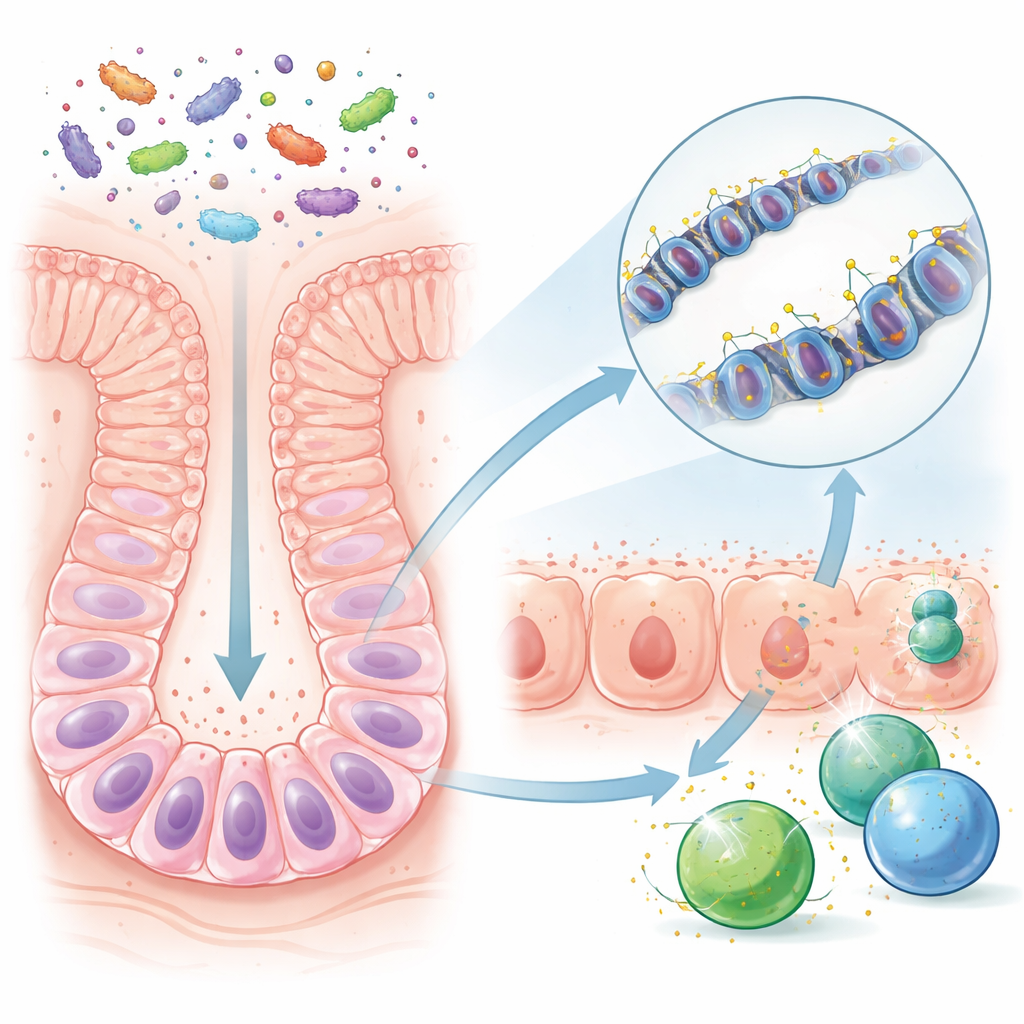
Före avvänjning är en ung mus tarm relativt enkel, försörjd av moderns mjölk och en begränsad uppsättning mikrober. Efter avvänjning för med sig ny mat många fler bakteriearter och mikrobprodukter. Forskarna jämförde möss uppvuxna i normala, mikroborika miljöer med möss som hölls germfria. De fokuserade på långlivade intestinella stamceller som kontinuerligt regenererar tarmens slemhinna. Även om den övergripande DNA-kemin i dessa celler såg liknande ut med eller utan mikrober, var specifika DNA-sträckor—reglerande regioner som fungerar som volymknappar för närliggande gener—tydligt annorlunda när mikrober fanns närvarande. Många av dessa regioner låg nära gener som är involverade i att känna igen och svara på mikrober.

Hur mikrober skriver bestående anteckningar på DNA
Teamet fann att efter avvänjning förlorade vissa DNA-regions i stamceller små kemiska markörer kallade metylgrupper. Denna ”demetylering” skedde särskilt vid platser som reglerar gener som används för att presentera mikrobfragment för immunceller. När dessa regioner avkläddes metylmärken nedärvdes förändringen när stamceller delade sig och mognade till de dagliga cellerna som bekläder tarmen. Som ett resultat var vuxna tarmceller hos mikrobeexponerade möss förberedda att snabbt slå på försvarsgener, även långt efter att den initiala avvänjningsperioden hade passerat. I kontrast utvecklade germfria möss, eller möss vars tarmar koloniserades först senare i livet, inte denna hållbara förberedelse i samma utsträckning.
En kort signalvåg med långsiktig påverkan
Vad driver dessa DNA-förändringar? Under avvänjningen utlöser det expanderande mikrobiomet en kortvarig våg av inflammatoriska budbärare, inklusive en som kallas interferon-gamma. Författarna blockerade denna signal i unga möss strax efter avvänjningen och fann att den kritiska demetyleringen och genförberedelsen i stort sett försvann; att blockera den hos vuxna hade liten effekt. I miniatyr-tarmorger odlas i skålar var exponering för låga nivåer av interferon-gamma tillräckligt för att utlösa snabb demetylering och långvarig beredskap hos nyckelgener. Efter denna behandling svarade organoiderna snabbare och starkare på senare utmaningar, även på olika typer av signaler—ett beteende som liknar ett inlärt minne i tarmens epitel.
Antibiotika, saknade mikrober och en sårbar tarm
Studien testade också vad som händer när denna tidiga samspel rubbas av antibiotika. Möss som gavs lågdospenicillin från före födseln fram till avvänjning behöll många mikrober generellt men förlorade specifika grupper av grampositiva bakterier som är starka stimulatorer av interferon-gamma och producenter av metaboliter som underlättar DNA-demetylering. Dessa möss visade högre DNA-metylation vid de avgörande kontrollregionerna, svagare uttryck av antigenpresenterande gener i tarmens slemhinna och färre immunceller som producerar interferon-gamma. När de senare utsattes för en kemikalie som inducerar kolit utvecklade de en mer allvarlig och långvarig sjukdom, och de var mer benägna att få tumörer i tjocktarmen.
Vad detta betyder för livslång tarmsundhet
Samlade innebär arbetet att perioden efter avvänjning är ett smalt men kraftfullt fönster under vilket kostdrivna förändringar i tarmmikrober lämnar bestående spår på intestinella stamceller. Dessa epigenetiska markörer pressar inte konstant immungenerna i övervarv; istället håller de systemet på alerten, redo att ge ett snabbt, balanserat svar på framtida hot. Att störa denna tidiga mikrobiella träning—genom försenad kolonisation eller bred antibiotikaanvändning—kan kompromettera detta inbyggda minne och göra tarmen mer mottaglig för kronisk inflammation och cancer. Även om studien gjordes i möss väcker den viktiga frågor om hur val i spädbarnsmatning, microbiomriktade terapier och tidig antibiotikaexponering kan forma människans tarmhälsa i årtionden.
Citering: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
Nyckelord: tarmmikrobiom, avvänjning, epigenetiskt minne, intestinalt immunförsvar, antibiotika i tidig ålder