Clear Sky Science · de
Abstillen treibt mikrobiomvermittelte epigenetische Regulation und formt das Immungedächtnis bei Mäusen
Warum die ersten festen Mahlzeiten wichtig sind
Wenn ein Säugling – Maus oder Mensch – von Milch auf feste Nahrung umsteigt, wird der Darm zur Heimat einer deutlich vielfältigeren Mikrobenwelt. Diese neue Gemeinschaft hilft nicht nur bei der Verdauung; sie sendet Signale, die die Abwehrkräfte des Körpers lebenslang prägen können. Die vorliegende Studie an Mäusen zeigt, dass die kurze Phase rund ums Abstillen wie ein Immun-„Trainingslager“ wirkt, in dem Darmbakterien durch feine chemische Markierungen auf der DNA dauerhaft die Zellen des Darms justieren. Wird dieses Zeitfenster gestört, etwa durch frühe Antibiotikagaben, kann das die Darmabwehr schwächen und das Risiko für Entzündungen des Darms und Krebs später im Leben erhöhen.
Das wechselvolle Leben der Darmmikroben
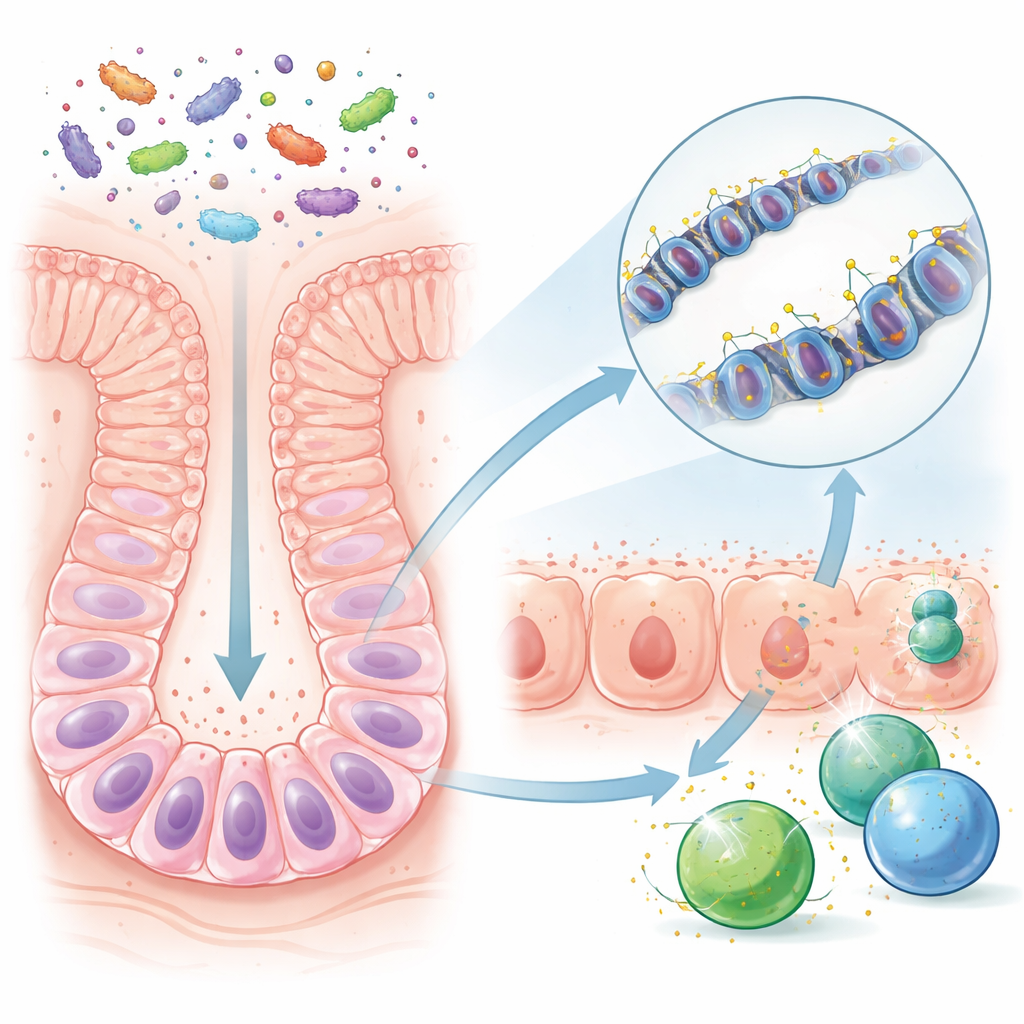
Vor dem Abstillen ist der Darm eines jungen Mausexemplars relativ einfach strukturiert, gespeist von der Muttermilch und einem begrenzten Mikrobiensatz. Nach dem Abstillen bringen neue Nahrungsmittel viele zusätzliche Bakterienarten und mikrobielle Produkte mit sich. Die Forschenden verglichen Mäuse, die unter normalen, mikrobenreichen Bedingungen aufwuchsen, mit keimfreien Tieren. Im Mittelpunkt standen langlebige intestinale Stammzellen, die die Darmoberfläche fortlaufend erneuern. Zwar ähnelte die allgemeine DNA-Chemie dieser Zellen mit und ohne Mikroben weitgehend einander, doch bestimmte DNA-Abschnitte – Kontrollregionen, die wie Lautstärkeregler für nahegelegene Gene wirken – unterschieden sich deutlich, wenn Mikroben vorhanden waren. Viele dieser Regionen lagen in der Nähe von Genen, die an der Erkennung und Reaktion auf Mikroben beteiligt sind.

Wie Mikroben dauerhafte Notizen in der DNA hinterlassen
Das Team stellte fest, dass nach dem Abstillen bestimmte Kontrollregionen in den Stammzellen winzige chemische Markierungen, sogenannte Methylgruppen, verloren. Diese „Demethylierung“ trat besonders an Stellen auf, die Gene regulieren, die mikrobielle Fragmente den Immunzellen präsentieren. Sobald diese Regionen ihrer Methylmarken beraubt waren, wurde die Veränderung beim Teilen und der Reifung der Stammzellen in die normalen Darmzellen weitergegeben. Folglich waren erwachsene Darmschleimhautzellen bei mikrobenexponierten Mäusen darauf vorbereitet, Abwehrgene rasch hochzufahren, selbst lange nach der Abstillphase. Im Gegensatz dazu entwickelten keimfreie Mäuse oder Mäuse, deren Darm erst später besiedelt wurde, diese dauerhafte Prägung nicht im selben Ausmaß.
Ein kurzer Signalschub mit langfristiger Wirkung
Was treibt diese DNA-Veränderungen an? Während des Abstillens löst das sich ausdehnende Mikrobiom eine kurzlebige Welle entzündlicher Botenstoffe aus, darunter Interferon-gamma. Die Autorinnen und Autoren blockierten dieses Signal bei jungen Mäusen unmittelbar nach dem Abstillen und fanden heraus, dass die entscheidende Demethylierung und Genvorbereitung weitgehend ausblieben; eine Blockade bei erwachsenen Tieren hatte kaum Wirkung. In im Labor gezüchteten Mini-Darm-„Organoiden“ reichte die Exposition gegenüber niedrigen Interferon-gamma-Spiegeln aus, um eine schnelle Demethylierung und eine langfristige Bereitschaft zentraler Gene auszulösen. Nach dieser Behandlung reagierten die Organoide später schneller und stärker auf Herausforderungen, sogar auf unterschiedliche Signaltypen – ein Verhalten, das einem trainierten Gedächtnis der Darmschleimhaut ähnelt.
Antibiotika, fehlende Mikroben und ein verwundbarer Darm
Die Studie untersuchte außerdem, was passiert, wenn diese frühe Abstimmung durch Antibiotika gestört wird. Mäuse, die von vor der Geburt bis zum Abstillen niedrig dosiertes Penicillin erhielten, behielten zwar viele Mikroben insgesamt, verloren jedoch bestimmte Gruppen grampositiver Bakterien, die starke Stimulatoren von Interferon-gamma sind und Metabolite produzieren, die bei der DNA-Demethylierung helfen. Diese Mäuse zeigten höhere DNA-Methylierung an den entscheidenden Kontrollregionen, eine schwächere Expression von antigenpräsentierenden Genen in der Darmschleimhaut und weniger interferon-gamma-produzierende Immunzellen. Bei späterer Exposition gegenüber einem chemischen Colitisauslöser entwickelten sie schwerere und länger anhaltende Erkrankungen und waren anfälliger für Tumoren im Dickdarm.
Was das für die lebenslange Darmgesundheit bedeutet
In der Summe zeichnet die Arbeit das Post-Abstillungs-Intervall als ein schmales, aber wirkungsvolles Fenster, in dem durch die Nahrung bedingte Veränderungen des Mikrobioms dauerhafte Spuren in intestinalen Stammzellen hinterlassen. Diese epigenetischen Markierungen treiben Immungene nicht dauerhaft in Überfunktion; vielmehr halten sie das System in Bereitschaft, sodass es auf künftige Bedrohungen schnell und ausgewogen reagieren kann. Eingriffe in dieses frühe mikrobielle Training – durch verzögerte Kolonisierung oder breit eingesetzte Antibiotika – können dieses eingebaute Gedächtnis beeinträchtigen und den Darm anfälliger für chronische Entzündungen und Krebs machen. Obwohl die Studie an Mäusen durchgeführt wurde, wirft sie wichtige Fragen dazu auf, wie Säuglingsernährung, mikrobiomzielgerichtete Therapien und frühe Antibiotikagaben die intestinale Gesundheit von Menschen über Jahrzehnte hinweg prägen könnten.
Zitation: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
Schlüsselwörter: Darmmikrobiom, Abstillen, epigenetisches Gedächtnis, intestinale Immunität, Antibiotika in der frühen Lebensphase