Clear Sky Science · es
El destete impulsa la regulación epigenética mediada por el microbioma para configurar la memoria inmunitaria en ratones
Por qué importan las primeras comidas sólidas
Cuando un bebé—ratón u humano—pasa de la leche a los alimentos sólidos, su intestino se convierte en el hogar de una comunidad microbiana mucho más diversa. Esta nueva comunidad no solo ayuda a digerir la comida; envía señales que pueden moldear las defensas del organismo a lo largo de la vida. Este estudio en ratones muestra que el periodo breve en torno al destete actúa como un “campo de entrenamiento” inmunitario, donde las bacterias intestinales ajustan de forma permanente las células intestinales mediante marcas químicas sutiles en el ADN. Alterar esta ventana, por ejemplo con antibióticos tempranos, puede debilitar las defensas intestinales y aumentar el riesgo de inflamación intestinal y cáncer en etapas posteriores.
La vida cambiante de los microbios intestinales
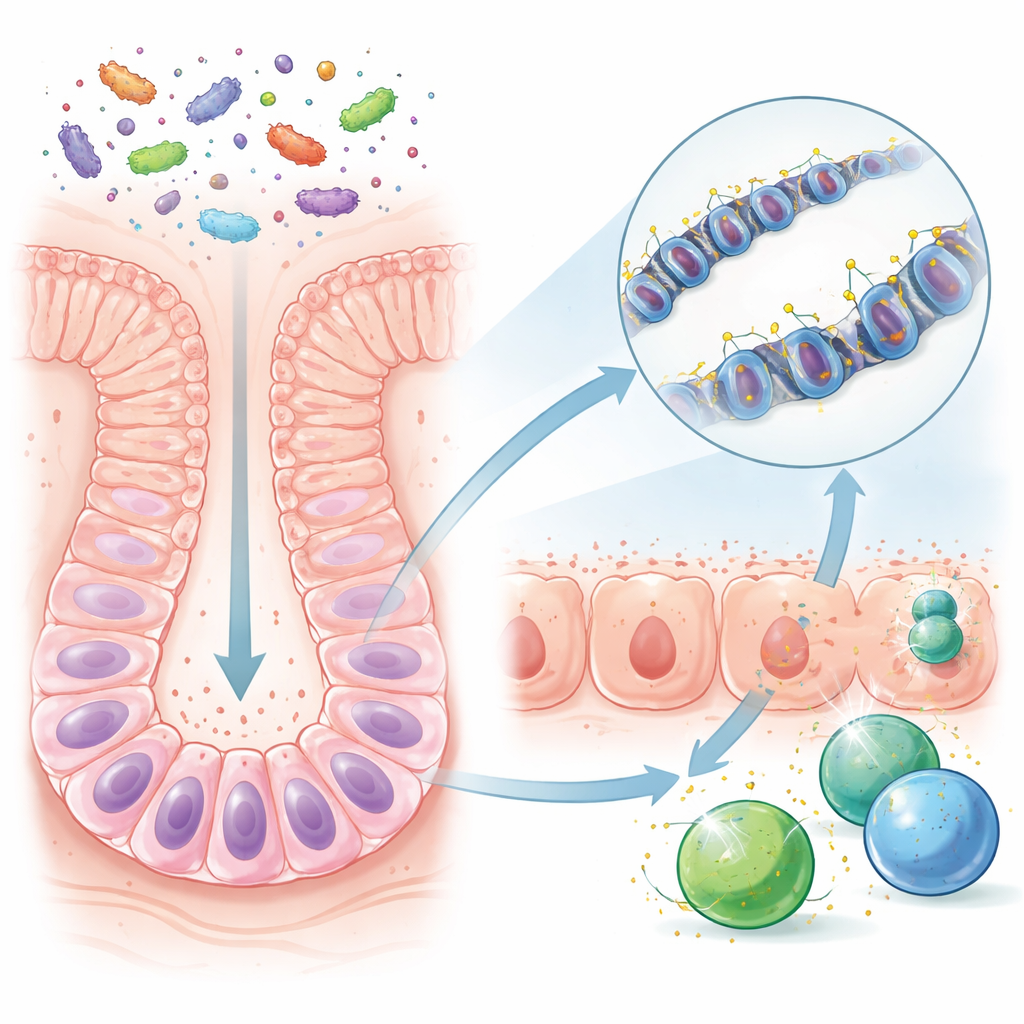
Antes del destete, el intestino de un ratón joven es relativamente sencillo, alimentado por la leche materna y un conjunto limitado de microbios. Tras el destete, los nuevos alimentos introducen muchas más especies bacterianas y productos microbianos. Los investigadores compararon ratones criados en condiciones normales ricas en microbios con ratones mantenidos libres de gérmenes. Se centraron en las células madre intestinales de larga vida, que regeneran continuamente el revestimiento del intestino. Aunque la química general del ADN de estas células era similar con o sin microbios, tramos específicos de ADN—regiones de control que actúan como botones de volumen para genes cercanos—eran claramente distintos cuando había microbios presentes. Muchas de estas regiones se situaban cerca de genes implicados en reconocer y responder a los microbios.

Cómo los microbios escriben notas duraderas en el ADN
El equipo observó que tras el destete, ciertas regiones de control del ADN en las células madre perdían pequeñas etiquetas químicas llamadas grupos metilo. Esta “desmetilación” se producía especialmente en sitios que regulan genes empleados para presentar fragmentos microbianos a las células inmunitarias. Una vez que estas regiones quedaban despojadas de etiquetas metilo, el cambio se transmitía a medida que las células madre se dividían y maduraban en las células que recubren el intestino. Como resultado, las células intestinales adultas en ratones expuestos a microbios estaban predispuestas a activar rápidamente genes de defensa, incluso mucho después de que hubiera pasado el periodo inicial del destete. En contraste, los ratones libres de gérmenes, o aquellos cuyo intestino se colonizó solo más tarde en la vida, no desarrollaron este primado duradero en la misma medida.
Un pulso breve de señales con impacto a largo plazo
¿Qué impulsa estos cambios en el ADN? Durante el destete, el microbioma en expansión desencadena una ola de mensajeros inflamatorios de corta duración, incluido uno llamado interferón gamma. Los autores bloquearon esta señal en ratones jóvenes justo después del destete y observaron que la desmetilación crítica y el primado génico desaparecían en gran medida; bloquearla en adultos tuvo poco efecto. En “organoides” intestinales en miniatura cultivados en placas, la exposición a niveles bajos de interferón gamma fue suficiente para desencadenar una desmetilación rápida y una preparación duradera de genes clave. Tras este tratamiento, los organoides respondieron más rápido y con mayor intensidad a desafíos posteriores, incluso a tipos distintos de señales—un comportamiento similar a una memoria entrenada en el revestimiento intestinal.
Antibióticos, microbios perdidos y un intestino vulnerable
El estudio también evaluó qué ocurre cuando esta coreografía temprana se altera con antibióticos. Ratones tratados con penicilina en dosis bajas desde antes del nacimiento hasta el destete conservaron muchos microbios en general, pero perdieron grupos específicos de bacterias Gram-positivas que son potentes estimuladoras de interferón gamma y productoras de metabolitos que favorecen la desmetilación del ADN. Estos ratones mostraron una mayor metilación del ADN en las regiones de control cruciales, una expresión más débil de genes de presentación de antígenos en el revestimiento intestinal y menos células inmunitarias productoras de interferón gamma. Al exponerse más tarde a un químico que induce colitis, desarrollaron una enfermedad más grave y prolongada, y mostraron mayor propensión a tumores de colon.
Qué significa esto para la salud intestinal a lo largo de la vida
En conjunto, el trabajo describe el periodo posdestete como una ventana estrecha pero potente durante la cual los cambios dietéticos en el microbioma intestinal dejan marcas duraderas en las células madre intestinales. Estas marcas epigenéticas no mantienen los genes inmunitarios en hiperactividad constante; más bien, mantienen el sistema en alerta, listo para montar una respuesta rápida y equilibrada frente a amenazas futuras. Interferir con este entrenamiento microbiano temprano—mediante colonización tardía o el uso amplio de antibióticos—puede comprometer esta memoria incorporada y dejar el intestino más susceptible a inflamación crónica y cáncer. Aunque el estudio se llevó a cabo en ratones, plantea preguntas importantes sobre cómo las elecciones de alimentación infantil, las terapias dirigidas al microbioma y la exposición temprana a antibióticos podrían influir en la salud intestinal humana durante décadas.
Cita: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
Palabras clave: microbioma intestinal, destete, memoria epigenética, inmunidad intestinal, antibióticos en la primera infancia