Clear Sky Science · ru
Отлучение от груди вызывает опосредованную микробиомом эпигенетическую регуляцию, формирующую иммунную память у мышей
Почему важны первые твёрдые прикормы
Когда детёныш — мышь или человек — переходит с молока на твёрдую пищу, его кишечник заселяется гораздо более разнообразной совокупностью микробов. Эта новая сообщества не только помогает переваривать еду; она посылает сигналы, которые могут формировать защитные механизмы организма на всю жизнь. Исследование на мышах показывает, что краткий период вокруг отлучения действует как «учебный лагерь» для иммунитета, где кишечные бактерии навсегда настраивают клетки кишечника с помощью тонких химических меток на ДНК. Нарушение этого окна, например при раннем приёме антибиотиков, может ослабить защиту кишечника и повысить риск воспалительных заболеваний кишечника и рака в дальнейшем.
Как меняется жизнь микробов в кишечнике
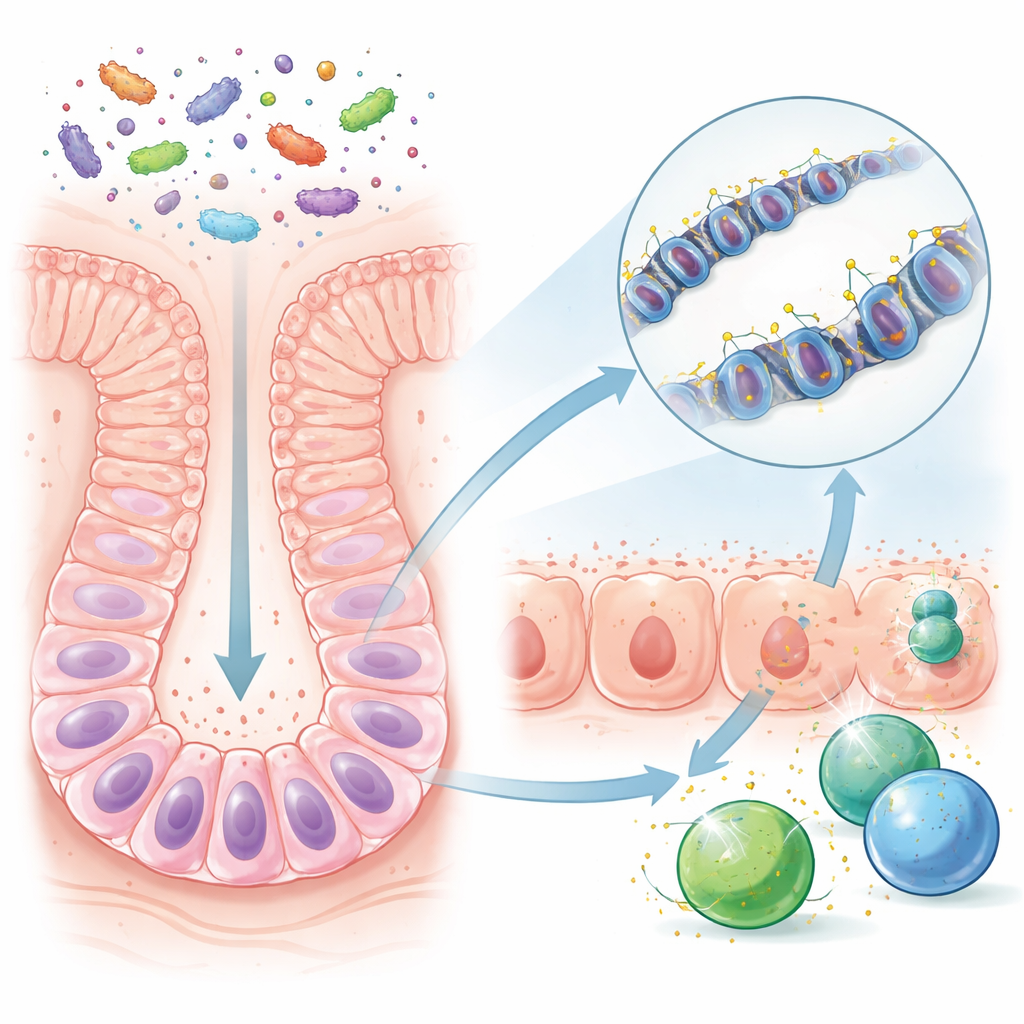
До отлучения кишечник молодой мыши относительно прост: он питается материнским молоком и заселён ограниченным набором микробов. После отлучения новая пища приносит гораздо больше видов бактерий и микробных продуктов. Исследователи сравнивали мышей, выращенных в нормальных условиях с богатой микробиотой, и мышей, содержащихся в условиях без микробов. Они сосредоточились на длительно живущих стволовых клетках кишечника, которые постоянно обновляют эпителий. Хотя общая химия ДНК этих клеток выглядела схожей при наличии или отсутствии микробов, определённые участки ДНК — регуляторные области, действующие как регуляторы громкости для соседних генов — отличались при наличии микробов. Многие из этих областей находились рядом с генами, вовлечёнными в распознавание и ответ на микробы.

Как микробы оставляют долговременные метки на ДНК
Команда обнаружила, что после отлучения некоторые регуляторные области ДНК в стволовых клетках теряли крошечные химические метки, называемые метильными группами. Эта «деметилирование» происходило особенно в тех местах, которые регулируют гены, участвующие в представлении микробных фрагментов иммунным клеткам. После удаления меток это изменение передавалось при делении стволовых клеток и их созревании в повседневные клетки, выстилающие кишечник. В результате у взрослых мышей, подвергшихся воздействию микробов, клетки кишечника были готовы быстро включать гены защиты, даже спустя долгое время после периода отлучения. Напротив, мыши, выращенные в условиях без микробов, или мыши, колонизированные только позднее, не развивали такого стойкого настроя в той же степени.
Краткий всплеск сигналов с долгосрочным эффектом
Что вызывает эти изменения ДНК? В период отлучения расширяющаяся микробиота вызывает короткую волну воспалительных посредников, включая интерферон-гамма. Авторы блокировали этот сигнал у молодых мышей сразу после отлучения и обнаружили, что критическое деметилирование и подготовка генов в значительной степени исчезали; блокирование в зрелом возрасте имело мало эффекта. В миниатюрных «органоидах» кишечника, выращенных в чашках, воздействие низких уровней интерферона-гамма было достаточным, чтобы вызвать быстрое деметилирование и долгосрочную готовность ключевых генов. После такого воздействия органоиды отвечали быстрее и сильнее на последующие вызовы, даже на разные типы сигналов — поведение, сходное с тренировочной памятью слизистой кишечника.
Антибиотики, недостающие микробы и уязвимый кишечник
Исследование также проверяло, что происходит, когда эта ранняя «хореография» нарушается антибиотиками. Мышам, получавшим низкие дозы пенициллина с периода до рождения до отлучения, в целом сохранялась значительная часть микробов, но исчезли определённые группы грамположительных бактерий, которые сильно стимулируют выработку интерферона-гамма и продуцируют метаболиты, способствующие деметилированию ДНК. У этих мышей в ключевых регуляторных областях наблюдалась более высокая метилизация ДНК, слабее выражались гены, отвечающие за представление антигенов в слизистой кишечника, и было меньше иммунных клеток, продуцирующих интерферон-гамма. При последующем воздействии химического вещества, вызывающего колит, у них развивалось более тяжёлое и продолжительное заболевание, и они были более подвержены опухолям ободочной кишки.
Что это означает для здоровья кишечника на всю жизнь
В целом работа рисует пост-отлучительный период как узкое, но мощное окно, в течение которого изменения микробов, вызванные питанием, оставляют долговременные метки на стволовых клетках кишечника. Эти эпигенетические метки не постоянно включают иммунные гены на полную мощность; скорее они держат систему в состоянии готовности, позволяя дать быстрый и сбалансированный ответ на будущие угрозы. Вмешательство в это раннее микробное «обучение» — через отсроченную колонизацию или широкое применение антибиотиков — может ослабить встроенную память и сделать кишечник более уязвимым к хроническому воспалению и раку. Хотя исследование проведено на мышах, оно ставит важные вопросы о том, как выбор питания младенца, терапии, направленные на микробиом, и раннее применение антибиотиков могут формировать здоровье человеческого кишечника на десятилетия вперёд.
Цитирование: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
Ключевые слова: микробиом кишечника, отлучение от груди, эпигенетическая память, кишечный иммунитет, антибиотики в раннем возрасте