Clear Sky Science · fr
Le sevrage pilote la régulation épigénétique médiée par le microbiome pour façonner la mémoire immunitaire chez la souris
Pourquoi les premiers aliments solides comptent
Lorsque le nourrisson — souris ou humain — passe du lait aux aliments solides, son intestin devient le domicile d’un ensemble microbien bien plus riche. Cette nouvelle communauté ne se contente pas d’aider à digérer le repas ; elle envoie des signaux qui peuvent modeler les défenses de l’organisme pour la vie. Cette étude chez la souris montre que la période brève autour du sevrage agit comme un « camp d’entraînement » immunitaire, où les bactéries intestinales règlent de façon pérenne les cellules intestinales via de subtiles marques chimiques sur l’ADN. Perturber cette fenêtre, par exemple avec des antibiotiques précoces, peut affaiblir les défenses intestinales et augmenter le risque d’inflammation intestinale et de cancer plus tard.
La vie changeante des microbes intestinaux
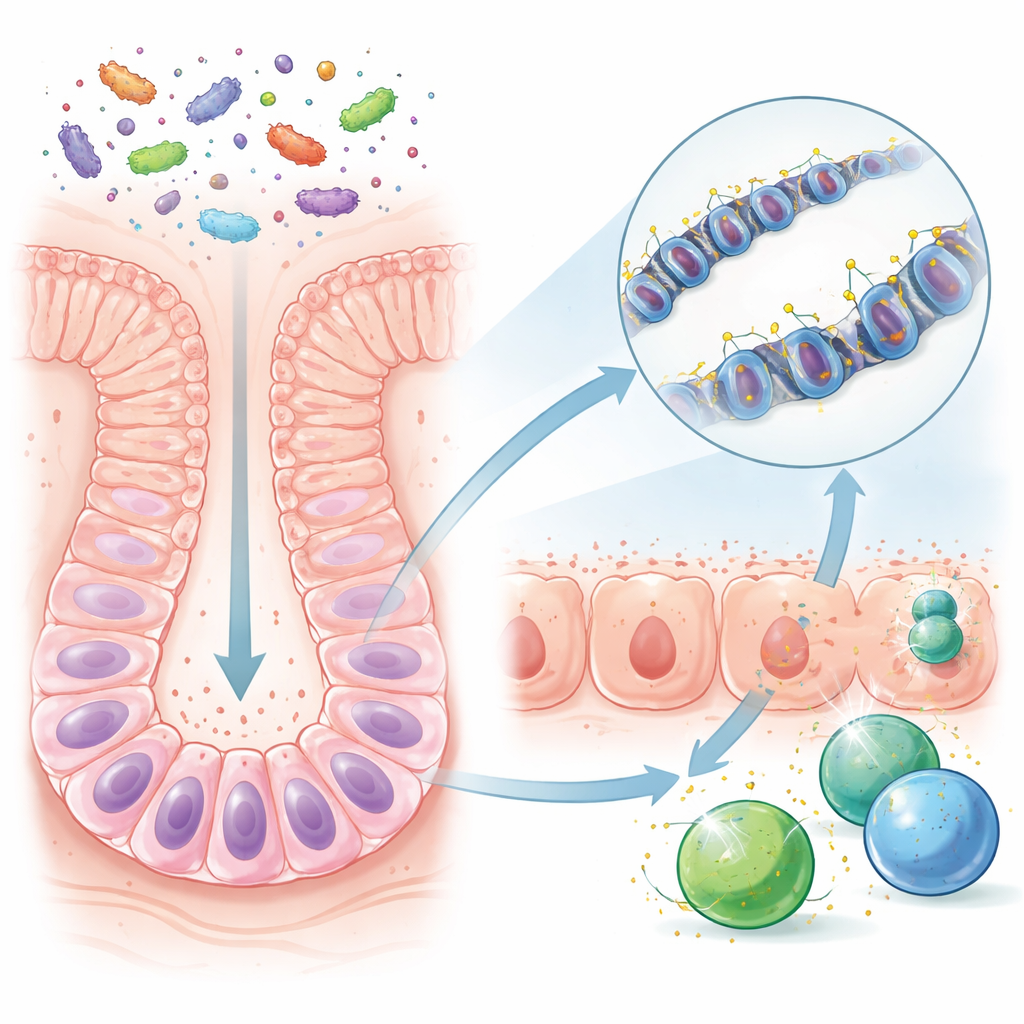
Avant le sevrage, l’intestin d’une jeune souris est relativement simple, nourri par le lait maternel et par un ensemble limité de microbes. Après le sevrage, de nouveaux aliments apportent bien d’autres espèces bactériennes et des produits microbiens. Les chercheurs ont comparé des souris élevées dans des conditions normales riches en microbes à des souris maintenues sans germes. Ils se sont concentrés sur les cellules souches intestinales à longue durée de vie, qui régénèrent en continu la muqueuse intestinale. Bien que la chimie globale de l’ADN de ces cellules paraisse similaire avec ou sans microbes, des portions spécifiques d’ADN — des régions de contrôle qui fonctionnent comme des boutons de volume pour des gènes proches — étaient notablement différentes en présence de microbes. Nombre de ces régions se situaient près de gènes impliqués dans la reconnaissance et la réponse aux microbes.

Comment les microbes inscrivent des notes durables sur l’ADN
L’équipe a constaté qu’après le sevrage, certaines régions de contrôle de l’ADN dans les cellules souches perdaient de petites marques chimiques appelées groupes méthyles. Cette « déméthylation » survient tout particulièrement sur des sites qui régulent des gènes utilisés pour présenter des fragments microbiens aux cellules immunitaires. Une fois ces régions privées de leurs marques méthyles, le changement était transmis au fil des divisions des cellules souches et lors de leur maturation en cellules ordinaires de la muqueuse intestinale. Par conséquent, les cellules intestinales d’adultes exposés aux microbes étaient prêtes à activer rapidement les gènes de défense, même longtemps après la période initiale de sevrage. En revanche, les souris sans germes, ou celles dont l’intestin n’a été colonisé que plus tard, n’ont pas développé cette préparation durable dans la même mesure.
Une brève rafale de signaux avec un impact à long terme
Qu’est-ce qui déclenche ces changements d’ADN ? Pendant le sevrage, le microbiome en expansion provoque une vague éphémère de messagers inflammatoires, dont un nommé interféron-gamma. Les auteurs ont bloqué ce signal chez de jeunes souris juste après le sevrage et ont constaté que la déméthylation critique et la préparation des gènes disparaissaient en grande partie ; le bloquer chez des adultes avait peu d’effet. Dans de petits organoïdes intestinaux cultivés en laboratoire, une exposition à faible dose d’interféron-gamma suffisait à déclencher une déméthylation rapide et une mise en état durable des gènes clés. Après ce traitement, les organoïdes répondaient plus vite et plus vigoureusement à des défis ultérieurs, y compris à des types de signaux différents — un comportement analogue à une mémoire entraînée de la muqueuse intestinale.
Antibiotiques, microbes manquants et un intestin vulnérable
L’étude a aussi testé ce qui se passe quand cette chorégraphie précoce est perturbée par des antibiotiques. Des souris traitées par de faibles doses de pénicilline de la période prénatale jusqu’au sevrage conservaient globalement beaucoup de microbes mais perdaient des groupes spécifiques de bactéries à Gram positif, qui stimulent fortement l’interféron-gamma et produisent des métabolites favorisant la déméthylation de l’ADN. Ces souris présentaient une méthylation de l’ADN plus élevée aux régions de contrôle cruciales, une expression affaiblie des gènes de présentation d’antigènes dans la muqueuse et moins de cellules immunitaires productrices d’interféron-gamma. Lorsqu’elles étaient ensuite exposées à un produit chimique induisant la colite, elles développaient une maladie plus sévère et plus persistante, et étaient plus susceptibles de former des tumeurs du côlon.
Ce que cela signifie pour la santé intestinale sur toute la vie
Dans l’ensemble, ce travail dessine la période post-sevrage comme une fenêtre étroite mais puissante pendant laquelle les changements de régime alimentaire induisant des modifications du microbiome intestinal laissent des marques durables sur les cellules souches intestinales. Ces marques épigénétiques n’entraînent pas une activation chronique des gènes immunitaires ; elles maintiennent plutôt le système en alerte, prêt à lancer une réponse rapide et équilibrée face aux menaces futures. Interférer avec cet entraînement microbien précoce — par une colonisation retardée ou un usage large d’antibiotiques — peut compromettre cette mémoire intégrée et rendre l’intestin plus susceptible à l’inflammation chronique et au cancer. Bien que l’étude ait été réalisée chez la souris, elle soulève des questions importantes sur la manière dont les choix d’alimentation infantile, les thérapies ciblant le microbiome et l’exposition précoce aux antibiotiques pourraient façonner la santé intestinale humaine pendant des décennies.
Citation: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
Mots-clés: microbiome intestinal, sevrage, mémoire épigénétique, immunité intestinale, antibiotiques en bas âge