Clear Sky Science · pt
O desmame impulsiona a regulação epigenética mediada pelo microbioma para moldar a memória imunológica em camundongos
Por que as primeiras refeições sólidas importam
Quando um filhote — de camundongo ou humano — passa do leite para alimentos sólidos, seu intestino se torna lar de uma comunidade microbiana muito mais rica. Essa nova coletividade não apenas ajuda a digerir a comida; ela envia sinais que podem esculpir as defesas do corpo por toda a vida. Este estudo em camundongos mostra que o breve período em torno do desmame funciona como um “campo de treinamento” imunológico, em que bactérias intestinais ajustam de forma permanente células intestinais por meio de marcas químicas sutis no DNA. Interromper essa janela, por exemplo com antibióticos precoces, pode enfraquecer as defesas intestinais e aumentar o risco de inflamação intestinal e câncer mais tarde.
A vida em mudança dos micróbios intestinais
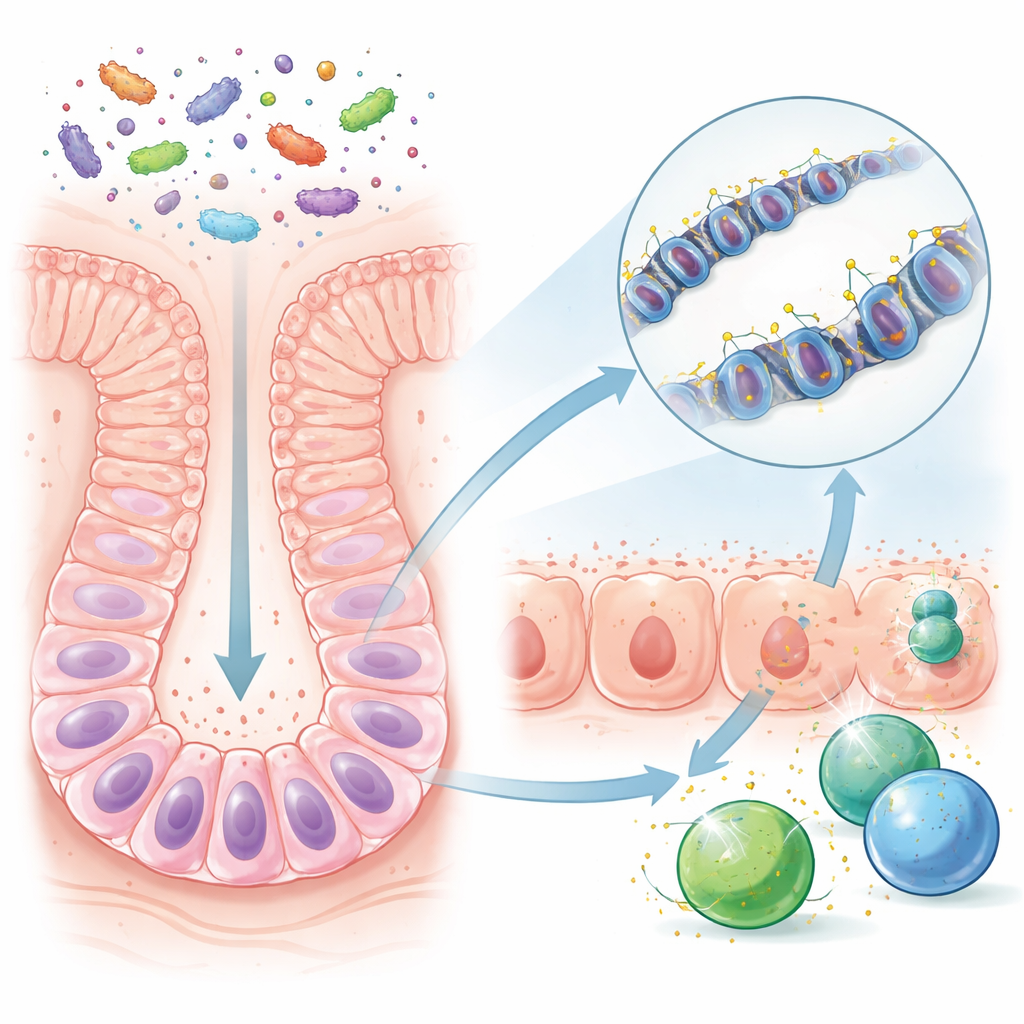
Antes do desmame, o intestino de um camundongo jovem é relativamente simples, nutrido pelo leite materno e por um conjunto limitado de microrganismos. Após o desmame, novos alimentos trazem muitas mais espécies bacterianas e produtos microbianos. Os pesquisadores compararam camundongos criados em condições normais, ricas em micróbios, com camundongos mantidos livres de germes. Eles focaram em células-tronco intestinais de longa vida, que regeneram continuamente o revestimento intestinal. Embora a química geral do DNA dessas células parecesse semelhante com ou sem micróbios, trechos específicos de DNA — regiões de controle que agem como botões de volume para genes próximos — eram notavelmente diferentes quando micróbios estavam presentes. Muitas dessas regiões ficavam próximas a genes envolvidos no reconhecimento e na resposta a microrganismos.

Como os micróbios escrevem notas duradouras no DNA
A equipe descobriu que, após o desmame, certas regiões de controle do DNA em células-tronco perderam pequenas marcas químicas chamadas grupos metil. Essa “desmetilação” ocorreu especialmente em locais que regulam genes usados para apresentar fragmentos microbianos às células imunes. Uma vez que essas regiões foram despojadas das marcas de metil, a alteração foi transmitida à medida que as células-tronco se dividiam e maturavam nas células comuns que revestem o intestino. Como resultado, células intestinais adultas em camundongos expostos a micróbios estavam preparadas para ativar genes de defesa rapidamente, mesmo muito depois do período inicial de desmame. Em contraste, camundongos livres de germes, ou camundongos cujo intestino foi colonizado apenas tardiamente, não desenvolveram esse preparo duradouro na mesma extensão.
Uma explosão breve de sinais com impacto de longo prazo
O que impulsiona essas alterações no DNA? Durante o desmame, o microbioma em expansão desencadeia uma onda de mensageiros inflamatórios de curta duração, incluindo uma chamada interferon-gama. Os autores bloquearam esse sinal em camundongos jovens logo após o desmame e verificaram que a desmetilação crítica e o preparo gênico desapareceram em grande parte; bloqueá-lo em adultos teve pouco efeito. Em “organoides” intestinais cultivados em placas, a exposição a baixos níveis de interferon-gama foi suficiente para desencadear desmetilação rápida e prontidão duradoura de genes-chave. Após esse tratamento, os organoides responderam mais rápido e com mais força a desafios posteriores, até mesmo a tipos diferentes de sinais — um comportamento semelhante a uma memória treinada no revestimento intestinal.
Antibióticos, micróbios ausentes e um intestino vulnerável
O estudo também testou o que acontece quando essa coreografia precoce é perturbada por antibióticos. Camundongos recebendo penicilina em baixa dose desde antes do nascimento até o desmame retiveram muitos micróbios no geral, mas perderam grupos específicos de bactérias Gram-positivas que são fortes indutoras de interferon-gama e produtoras de metabólitos que auxiliam a desmetilação do DNA. Esses camundongos mostraram maior metilação do DNA nas regiões de controle cruciais, expressão mais fraca de genes de apresentação de antígeno no revestimento intestinal e menos células imunes produtoras de interferon-gama. Ao serem expostos posteriormente a um químico que induz colite, desenvolveram doença mais severa e prolongada, e foram mais propensos a tumores de cólon.
O que isso significa para a saúde intestinal ao longo da vida
Em conjunto, o trabalho pinta o período pós-desmame como uma janela estreita, porém poderosa, durante a qual mudanças no microbioma impulsionadas pela dieta deixam marcas duradouras nas células-tronco intestinais. Essas marcas epigenéticas não mantêm genes imunes constantemente hiperativos; em vez disso, mantêm o sistema em alerta, pronto para montar uma resposta rápida e equilibrada a ameaças futuras. Interferir nesse treinamento microbiano precoce — por colonização atrasada ou uso amplo de antibióticos — pode comprometer essa memória incorporada e deixar o intestino mais suscetível a inflamação crônica e câncer. Embora o estudo tenha sido realizado em camundongos, ele levanta questões importantes sobre como escolhas de alimentação infantil, terapias direcionadas ao microbioma e exposição precoce a antibióticos podem moldar a saúde intestinal humana por décadas.
Citação: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
Palavras-chave: microbioma intestinal, desmame, memória epigenética, imunidade intestinal, antibióticos na primeira infância