Clear Sky Science · he
גמילה מניקה מפעילה וויסות אפיגנטי מותווך על ידי המיקרוביום לעיצוב זיכרון חיסוני בעכברים
מדוע הארוחות המוצקות הראשונות חשובות
כאשר תינוק — עכבר או אדם — עובר מחלב למזון מוצק, המעי שלו הופך לבית לקהילה מיקרוביאלית עשירה בהרבה. הקהילה החדשה הזאת לא רק מסייעת בעיכול; היא שולחת אותות שיכולים לעצב את מערכות ההגנה של הגוף לכל החיים. המחקר בעכברים מראה שתקופה קצרה סביב הגמילה פועלת כמו "מחנה אימונים" חיסוני, שבו חיידקי המעי מכוונים באופן קבוע תאי מעי באמצעות סימנים כימיים עדינים על ה-DNA. הפרעה לחלון הזה, למשל על ידי אנטיביוטיקה מוקדמת, יכולה להחליש את ההגנות במעי ולהעלות את הסיכון לדלקת מעי וסרטן בהמשך.
חיי המיקרובים שבמעי משתנים
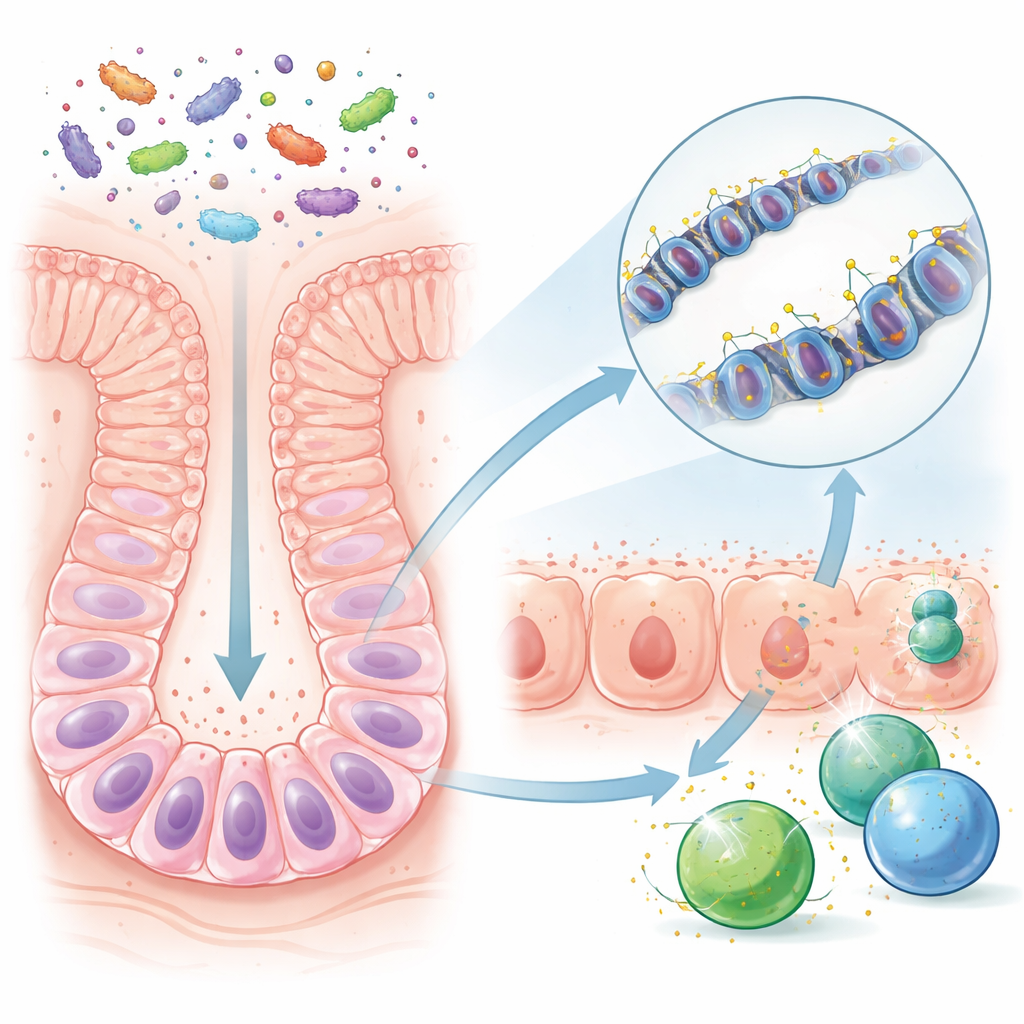
לפני הגמילה, מעי העכבר הצעיר פשוט יחסית, מזונן בחלב האם ובמערכת מיקרובים מצומצמת. אחרי הגמילה, מזונות חדשים מביאים איתם מינים חיידקיים ומוצרים מיקרוביאליים רבים יותר. החוקרים השוו עכברים שגדלו בתנאים נורמליים ועשירים במיקרובים לעכברים שנשמרו חופשיים ממיקרובים. הם התרכזו בתאי גזע מעיים ארוכי־חיים, המחדשים בהתמדה את ציפוי המעי. למרות שהכימיה הכוללת של ה-DNA בתאים אלה נראתה דומה עם או בלי מיקרובים, מקטעים ספציפיים של DNA — אזורי בקרה הפועלים ככפתורי עוצמה עבור גנים סמוכים — היו שונים באופן ניכר כאשר היו נוכחים מיקרובים. רבים מהאזורים האלה שכנו ליד גנים המעורבים בזיהוי ובתגובה למיקרובים.

איך המיקרובים כותבים הערות מתמשכות על ה-DNA
הקבוצה מצאה שלאחר הגמילה, אזורי בקרה מסוימים ב-DNA של תאי הגזע איבדו תגיות כימיות זעירות שנקראות קבוצות מתיל. "הסרת המתיל" הזו התרחשה במיוחד באתרי בקרה שמווסתים גנים המשמשים להצגת שברי מיקרובים לתאי החיסון. ברגע שאזורים אלה נוקו מתגיות המתיל, השינוי עבר בתורשה כאשר תאי הגזע התחלקו ובגרו לתאים היומיומיים שמצפים את המעי. כתוצאה מכך, תאי מעי בבוגרים שנחשפו למיקרובים היו מוכנים להפעיל גני הגנה במהירות, גם הרבה אחרי תקופת הגמילה. לעומת זאת, עכברים חופשיים ממיקרובים, או עכברים שנושבו במיקרובים רק מאוחר יותר בחיים, לא פיתחו את ההכנה העמידה הזו באותה מידה.
תהודה קצרה של אותות עם השפעה ארוכת טווח
מה מניע את השינויים האלה ב-DNA? במהלך הגמילה, המיקרוביום המתפתח מעורר גל קצר מועד של שליחי דלקת, כולל חלבון בשם אינטרפרון-גמא. המחברים חסמו אות זה בעכרים צעירים מיד לאחר הגמילה ומצאו שההסרת המתיל הקריטית וההכנה של הגנים נעלמו במידה רבה; חסימתו במבוגרים כמעט ולא השפיעה. באורגנואידים — "איברים זעירים" של מעי שגודלו במעבדה — חשיפה לרמות נמוכות של אינטרפרון-גמא הספיקה לגרום להסרת מתיל מהירה ולמוכנות מתמשכת של גנים מרכזיים. לאחר הטיפול הזה, האורגנואידים הגיבו מהר וחזק יותר לאתגרים מאוחרים, אפילו לסוגים שונים של אותות — התנהגות הדומה לזיכרון מאומן בציפוי המעי.
אנטיביוטיקה, מיקרובים חסרים ומעי פגיע
המחקר גם בדק מה קורה כשהכוריאוגרפיה המוקדמת הזאת מופרעת על ידי אנטיביוטיקה. עכברים שקיבלו פנצילין במינון נמוך מאז לפני הלידה ועד הגמילה שמרו על הרבה מיקרובים באופן כללי, אך איבדו קבוצות ספציפיות של חיידקים גרם-חיוביים שהם מגרה חזק של אינטרפרון-גמא ומפיקים מטבוליטים המסייעים להסרת מתיל ב-DNA. בעכברים אלה נצפתה רמת מתיל גבוהה יותר באזורי הבקרה הקריטיים, ביטוי חלש יותר של גנים המציגים אנטיגנים בציפוי המעי, ופחות תאי חיסון המייצרים אינטרפרון-גמא. כאשר נחשפו מאוחר יותר לכימיקל המעורר קוליטיס, הם פיתחו מחלה קשה וארוכה יותר, והיו נוטים יותר לגידולים במעי הגס.
מה משמעות זה לבריאות מעי לכל החיים
במשולב, העבודה מציירת את תקופת שלאחר הגמילה כחלון צר אך חזק שבו שינויים בתזונה המנוהלים על ידי חיידקי המעי מותירים סימנים מתמשכים על תאי גזע מעיים. הסימנים האפיגנטיים האלה אינם דוחפים באופן קבוע את גני החיסון לתרועה יתר; במקום זאת הם שומרים על המערכת במצב ערנות, מוכנה להגיב במהירות ובאיזון לאיומים בעתיד. הפרעה לאימון המיקרובי המוקדם הזה — באמצעות התיישבות מאוחרת של מיקרובים או שימוש רחב באנטיביוטיקה — עלולה לפגוע בזיכרון המובנה הזה ולהשאיר את המעי חשוף יותר לדלקת כרונית ולסרטן. למרות שהמחקר בוצע בעכברים, הוא מעלה שאלות חשובות לגבי האופן שבו בחירות ההאכלה לתינוקות, התערבויות ממוקדות-מיקרוביום וחשיפה לאנטיביוטיקה מוקדמת עשויות לעצב את בריאות המעי האנושי לעשורים.
ציטוט: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
מילות מפתח: מיקרוביום מעי, גמילה, זיכרון אפיגנטי, חיסון מעי, אנטיביוטיקה בחיי הילדות המוקדמים