Clear Sky Science · nl
Ontwenning stuurt microbioom-gemedieerde epigenetische regulatie om immuunherinnering bij muizen te vormen
Waarom de eerste vaste maaltijden ertoe doen
Wanneer een jong—muis of mens—overschakelt van melk op vast voedsel, wordt hun darm het thuis van een veel rijkere schakering microben. Deze nieuwe gemeenschap helpt niet alleen met de vertering; ze zendt signalen uit die de afweer van het lichaam voor het leven kunnen vormen. Deze studie bij muizen laat zien dat de korte periode rond de ontwenning fungeert als een immuun "trainingskamp", waarin darmbacteriën de intestinale cellen permanent afstemmen via subtiele chemische markeringen op DNA. Het verstoren van dit venster, bijvoorbeeld met vroege antibiotica, kan de darmverdediging verzwakken en het risico op darmontsteking en kanker later verhogen.
Het veranderende leven van darmmicroben
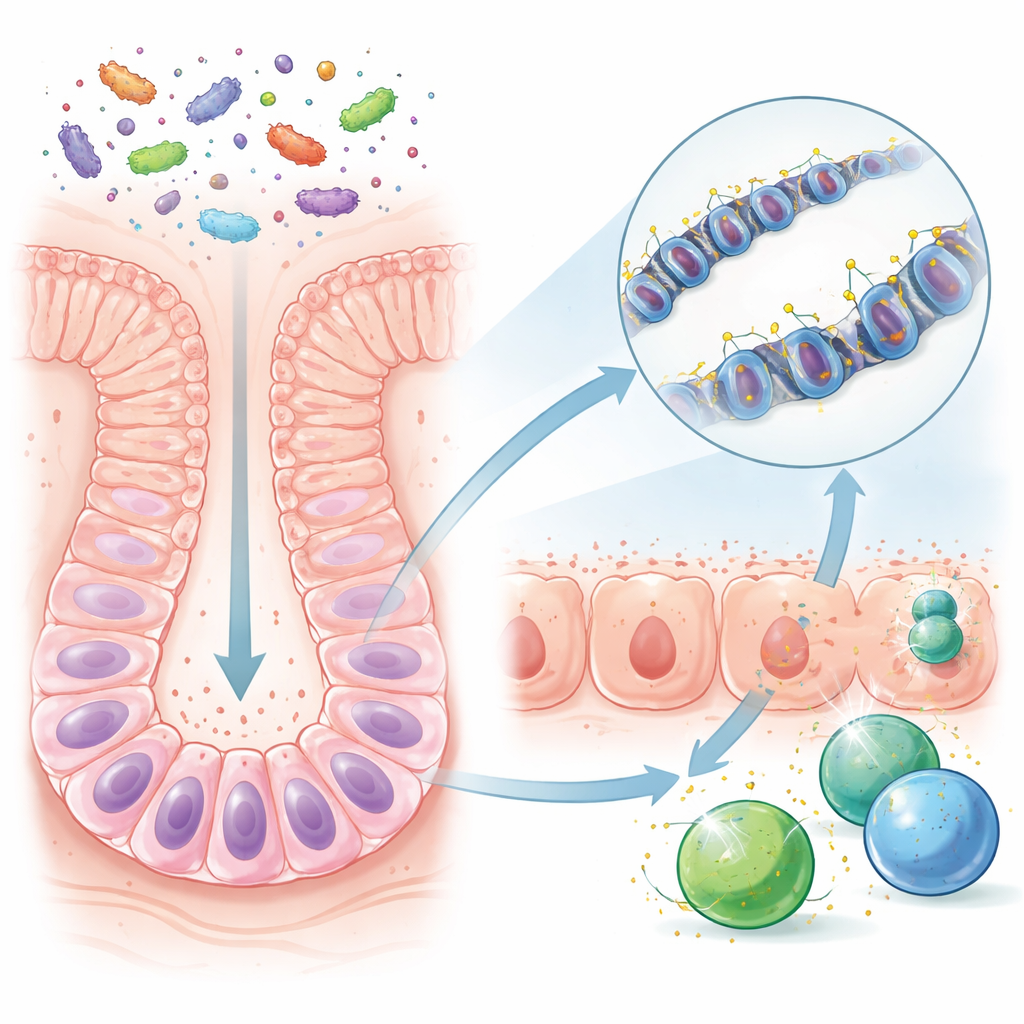
Voor de ontwenning is de darm van een jonge muis relatief eenvoudig, gevoed door moedermelk en een beperkte set microben. Na de ontwenning brengen nieuwe voedingsmiddelen veel meer bacteriesoorten en microbiële producten binnen. De onderzoekers vergeleken muizen die onder normale, microbieel rijke omstandigheden waren grootgebracht met muizen die kiemvrij werden gehouden. Ze richtten zich op langlevende intestinale stamcellen, die continu het darmslijmvlies regenereren. Hoewel de algemene DNA-chemie van deze cellen er vergelijkbaar uitzag met of zonder microben, waren specifieke DNA-gebieden—regelregio’s die als volumeknoppen voor nabijgelegen genen fungeren—merkbaar verschillend wanneer microben aanwezig waren. Veel van deze regio’s lagen nabij genen die betrokken zijn bij het herkennen en reageren op microben.

Hoe microben blijvende aantekeningen op DNA schrijven
Het team vond dat bepaalde DNA-regelregio’s in stamcellen na de ontwenning kleine chemische labels, methylgroepen, verloren. Deze "demethylatie" trad met name op op locaties die genen reguleren die gebruikt worden om microbiële fragmenten aan immuuncellen te presenteren. Zodra deze regio’s van methylgroepen waren ontdaan, werd de verandering doorgegeven naarmate stamcellen deelden en uitgroeiden tot de alledaagse cellen die het darmepitheel vormen. Als gevolg daarvan waren volwassen intestinale cellen bij muizen die aan microben waren blootgesteld getraind om verdedigingsgenen snel aan te zetten, zelfs lang nadat de ontwenning voorbij was. Daarentegen ontwikkelden kiemvrije muizen, of muizen waarvan de darm pas later in het leven gekoloniseerd werd, deze duurzame priming niet in dezelfde mate.
Een korte golf signalen met langdurige impact
Wat drijft deze DNA-veranderingen aan? Tijdens de ontwenning veroorzaakt het uitbreidende microbioom een kortstondige golf van ontstekingsboodschappers, waaronder interferon-gamma. De auteurs blokkeerden dit signaal in jonge muizen direct na de ontwenning en ontdekten dat de cruciale demethylatie en genpriming grotendeels verdwenen; blokkering bij volwassenen had weinig effect. In miniatuur-darmorganoïden gekweekt in schaaltjes was blootstelling aan lage niveaus van interferon-gamma voldoende om snelle demethylatie en langdurige paraatheid van sleutelgenen teweeg te brengen. Na deze behandeling reageerden de organoïden later sneller en krachtiger op uitdagingen, zelfs op andere typen signalen—een gedrag vergelijkbaar met een getraind geheugen in het darmslijmvlies.
Antibiotica, ontbrekende microben en een kwetsbare darm
De studie onderzocht ook wat er gebeurt wanneer deze vroegtijdige choreografie wordt verstoord door antibiotica. Muizen die vanaf de prenatale periode tot en met de ontwenning lage doses penicilline kregen, behielden veel microben in het algemeen maar verloren specifieke groepen Gram-positieve bacteriën die sterke stimulators zijn van interferon-gamma en producenten van metabolieten die helpen bij DNA-demethylatie. Deze muizen toonden hogere DNA-methylatie op de cruciale regelregio’s, zwakkere expressie van antigen-presenterende genen in hun darmepitheel en minder interferon-gamma producerende immuuncellen. Bij latere blootstelling aan een chemische stof die colitis induseert, ontwikkelden zij ernstiger en langduriger ziekte en waren ze gevoeliger voor colontumoren.
Wat dit betekent voor levenslange darmgezondheid
Gezamenlijk schetst het werk de post-ontwenningperiode als een smal maar krachtig venster waarin door dieet gedreven veranderingen in darmmicroben blijvende sporen achterlaten op intestinale stamcellen. Deze epigenetische markeringen duwen immuungenen niet voortdurend in een overactieve stand; in plaats daarvan houden ze het systeem waakzaam, klaar om een snelle, gebalanceerde respons op toekomstige bedreigingen te leveren. Verstoring van deze vroege microbiële training—door vertraagde kolonisatie of breed antibioticagebruik—kan dit ingebouwde geheugen ondermijnen en de darm vatbaarder maken voor chronische ontsteking en kanker. Hoewel de studie bij muizen is uitgevoerd, roept ze belangrijke vragen op over hoe zuigelingenvoedingskeuzes, microbiome-gerichte therapieën en vroege blootstelling aan antibiotica de menselijke darmgezondheid decennialang kunnen beïnvloeden.
Bronvermelding: Yang, L., Peery, R.C., Zhou, S. et al. Weaning drives microbiome-mediated epigenetic regulation to shape immune memory in mice. Nat Microbiol 11, 1064–1079 (2026). https://doi.org/10.1038/s41564-026-02295-6
Trefwoorden: darmmicrobioom, ontwenning, epigenetisch geheugen, intestinale immuniteit, antibiotica in de vroege levensfase