Clear Sky Science · zh
烯丙醚的催化不对称[1,2]-Wittig重排级联反应
将分子混乱化为有序
化学家常常希望构建具有镜像选择性的分子,因为生物体能区分“左手型”和“右手型”版本。本文解决了该领域的一个长期难题:如何控制一种以往难以驾驭的键重排反应,使其主要产出一种镜像构型而非随机混合。作者不仅找到了解决办法,还表明该反应通过一个出人意料的途径进行,从而推翻了几十年来课本上的观点。
这些构型变化为何重要
有机化学中许多高效反应通过在分子内部悄然重排键而非完全断裂重建来工作。这类“重排”因废料少、能在一步内构建复杂结构而备受青睐。其中称为Wittig重排的一类可以将简单的醚基转化为有价值的醇。然而,某个特定变体——烯丙醚的所谓[1,2]-Wittig重排——一直难以控制:它通常产生产物混合物,并且关键是常会打乱原有的三维构型,而非保持或生成单一构型。
一种新的级联途径
研究人员表明,可以通过将这一棘手反应设计成由特殊有机催化剂引导的两步级联来驯服它。他们的催化剂称为双功能亚胺膦(bifunctional iminophosphorane),既是异常强的碱,又提供精确的“手性”环境。首先,它引发一种行为良好的键迁移——[2,3]-重排,从而构建出具有很高手性选择性的三级手性醇中间体。随后在碱性条件下,该中间体静悄悄地再次重排,得到最终的[1,2]-Wittig产物。对于多种不同的起始物料,该序列都能可靠地给出收率良好且对映体比高的手性仲烯丙醇,意味着一种构型明显占优。
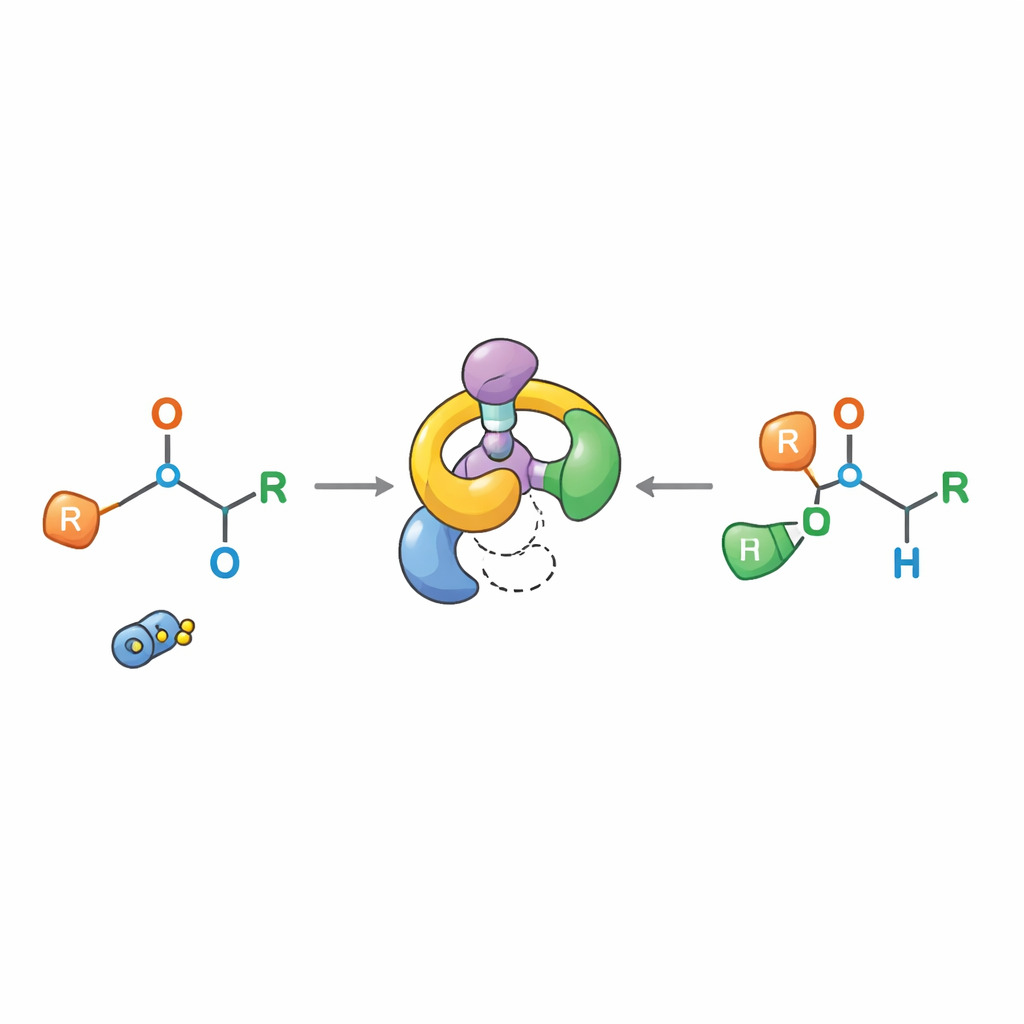
探究反应的真实路径
传统解释认为[1,2]-Wittig产物来自于断键形成自由基对再重组的过程,这种图景使得精确的立体化学控制看起来不太可能。新工作则描绘了不同的画面。通过缜密的实验——包括用对自由基敏感的添加剂进行捕获尝试、混合不同分子的“交叉”试验以及详细的时序核磁监测——作者表明反应通过一个特定的[2,3]-重排中间体进行,原子在同一分子内保持配对而非互换伙伴。第二步表面上类似于形式上被禁止的[1,3]-重排,但实际上是通过碎裂成紧密结合的离子对再有序地复合来展开,从而保留了手性中心的构型。
计算机确认隐藏步骤
为支持这一机理描述,研究团队对催化剂和底物的现实模型进行了广泛的量子化学计算。这些计算揭示了为何在第一步中会偏向形成某一对映体:优选的过渡态能形成三重强氢键网络以及芳环间有利的堆叠相互作用,而竞争构型则因相互作用较弱和位阻拥挤而不利。对于第二步,计算未能找到单一、平滑的协同路径;相反,它们支持一个逐步的离子化碎裂过程,伴随适度的能垒,随后几乎无障碍地复合。预测的能垒与实验测得的值非常接近,从而加强了离子对机理的说法。
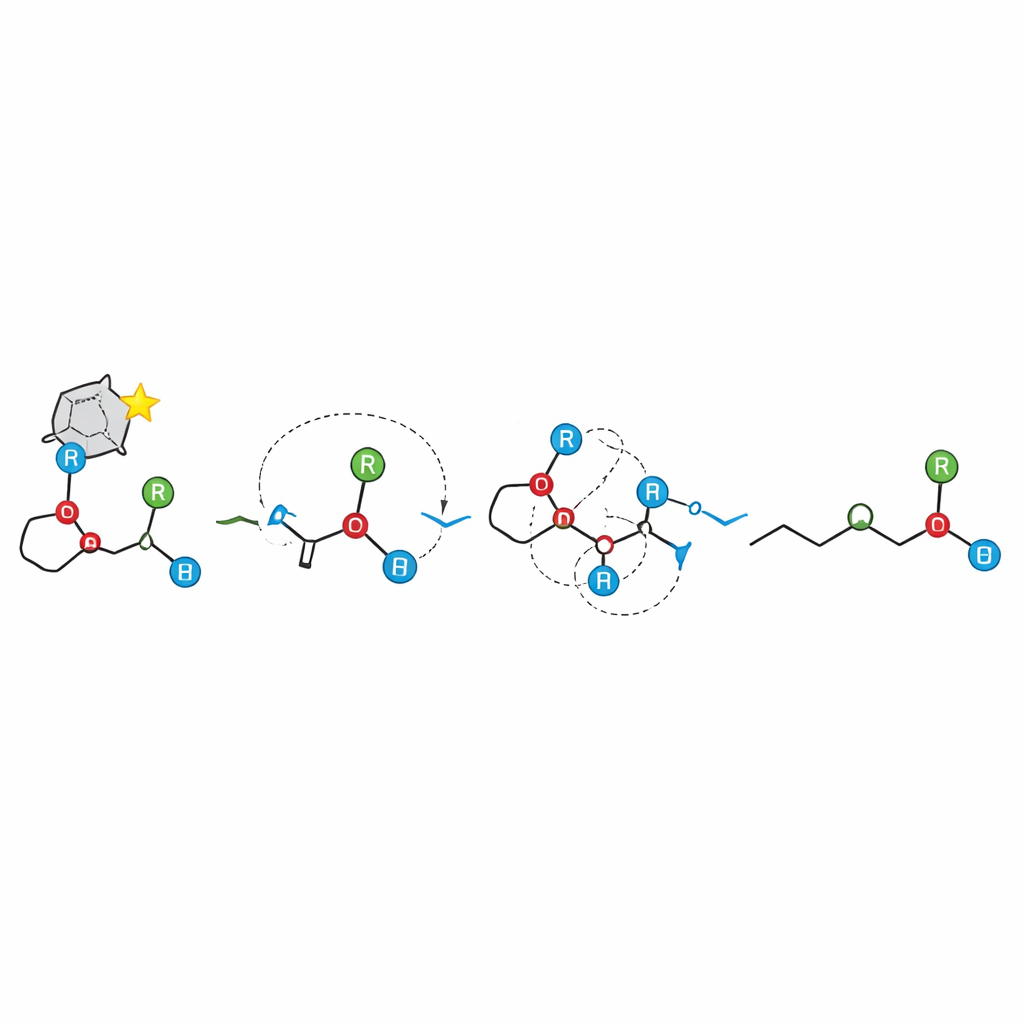
对构建手性分子的影响
从实用角度看,这项工作为合成化学家提供了一个稳健的新工具,可由容易获得的烯丙醚制备手性三级醇,并勾画出哪些结构调整有利或不利于该过程。更广泛地说,它证明即便反应通过带电碎片进行,只要这些碎片保持紧密相互作用,立体化学信息也能以惊人的保真度传递。通过否定基于自由基的[1,2]-Wittig重排观点并展示高度选择性的离子级联,该研究为重新思考和重新设计其它复杂键重排反应以实现精确三维控制打开了新局面。
引用: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
关键词: 不对称催化, σ重排反应, 手性三级醇, 反应机理, 有机合成