Clear Sky Science · pl
Katalityczna enantioselektwna kaskada [1,2]-Wittiga przemieszczenia eterów allylowych
Przekształcanie molekularnego chaosu w porządek
Chemicy często dążą do budowy cząsteczek selektywnych względem lustrzanych odbić, ponieważ nasze organizmy rozróżniają wersje „lewo‑” i „prawo‑ręczne”. Artykuł ten podejmuje długoletnią zagadkę w tej dziedzinie: jak skierować notorycznie niepokorny typ reakcji przestawiania wiązań, aby tworzył przeważnie jedną formę enancjomeryczną zamiast mieszaniny. Autorzy nie tylko znajdują sposób na osiągnięcie tego celu, lecz także pokazują, że reakcja przebiega niespodziewaną ścieżką, obalając wieloletnie podręcznikowe wyobrażenia.
Dlaczego te zmiany kształtu są istotne
Wiele potężnych reakcji w chemii organicznej polega na przesuwaniu wiązań wewnątrz cząsteczki zamiast rozbijania wszystkiego i zaczynania od nowa. Takie „przemieszczenia” są cenione, ponieważ marnują niewiele materiału i mogą zbudować złożone struktury w jednym kroku. Wśród nich ruchy znane jako przemieszczenia Wittiga mogą zamieniać proste grupy eterowe w wartościowe alkohole. Jednak szczególna wersja, tzw. [1,2]-przemieszczenie Wittiga eterów allylowych, była trudna do kontrolowania: zazwyczaj daje mieszaniny produktów i, co kluczowe, ma tendencję do mieszania konfiguracji 3D atomów zamiast zachowywania lub tworzenia jednej formy chiralnej.
Nowa ścieżka kaskadowa
Badacze wykazują, że ten kłopotliwy proces można okiełznać, włączając go w dwuetapową kaskadę prowadzoną przez specjalnie zaprojektowany katalizator organiczny. Ich katalizator, nazwany bifunkcyjnym iminofosforanem, jest jednocześnie wyjątkowo silną zasadą i precyzyjnym, „ręcznym” środowiskiem. Najpierw wywołuje dobrze zachowujące się przemieszczenie [2,3], które tworzy chiralny alkohol trzeciorzędowy z bardzo silnym uprzywilejowaniem jednej enancjomerii. Następnie, w warunkach zasadowych, ten pośrednik cicho przestawia się ponownie do końcowego produktu [1,2]-Wittiga. Dla wielu różnych substratów sekwencja ta niezawodnie dostarcza chiralne alkohole homoallylowe w dobrych wydajnościach i z wysokimi stosunkami enancjomerycznymi, co oznacza, że jedna forma dominuje.
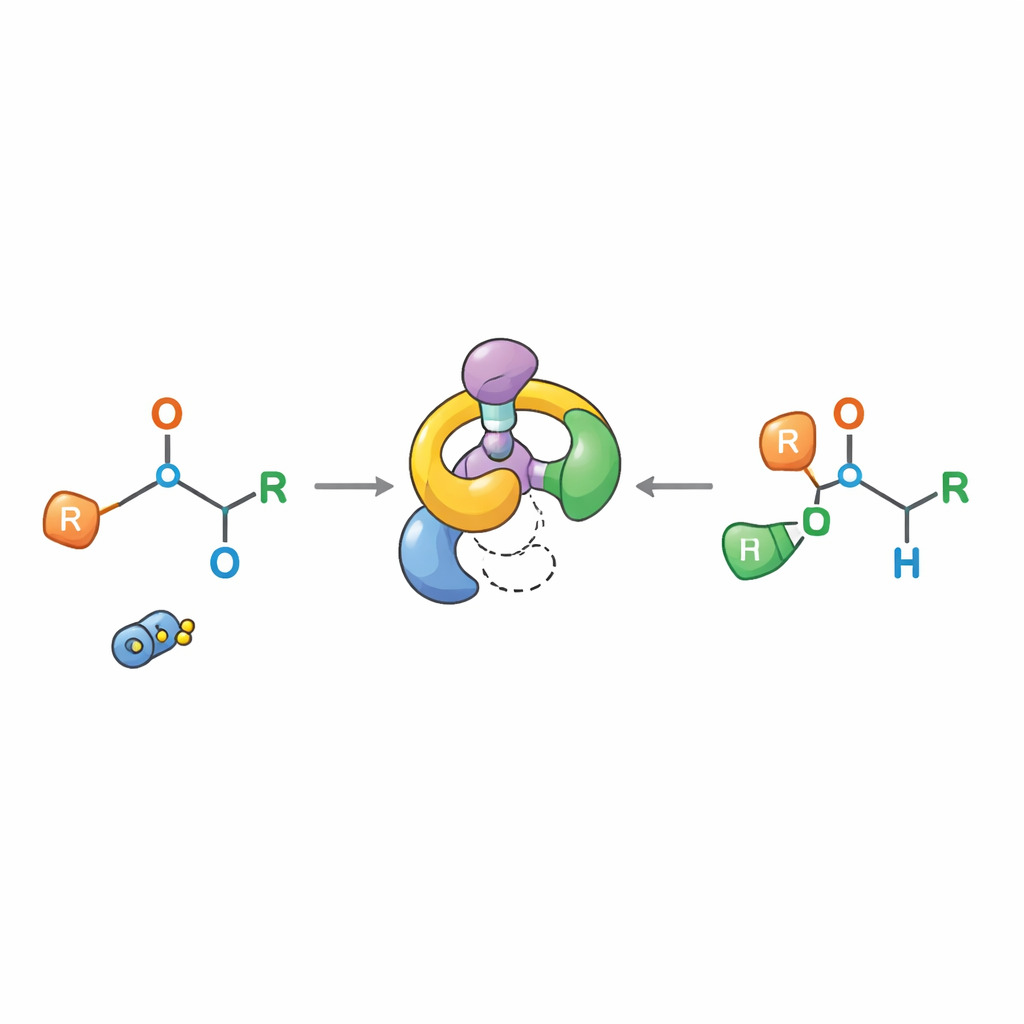
Badanie, jak reakcja naprawdę przebiega
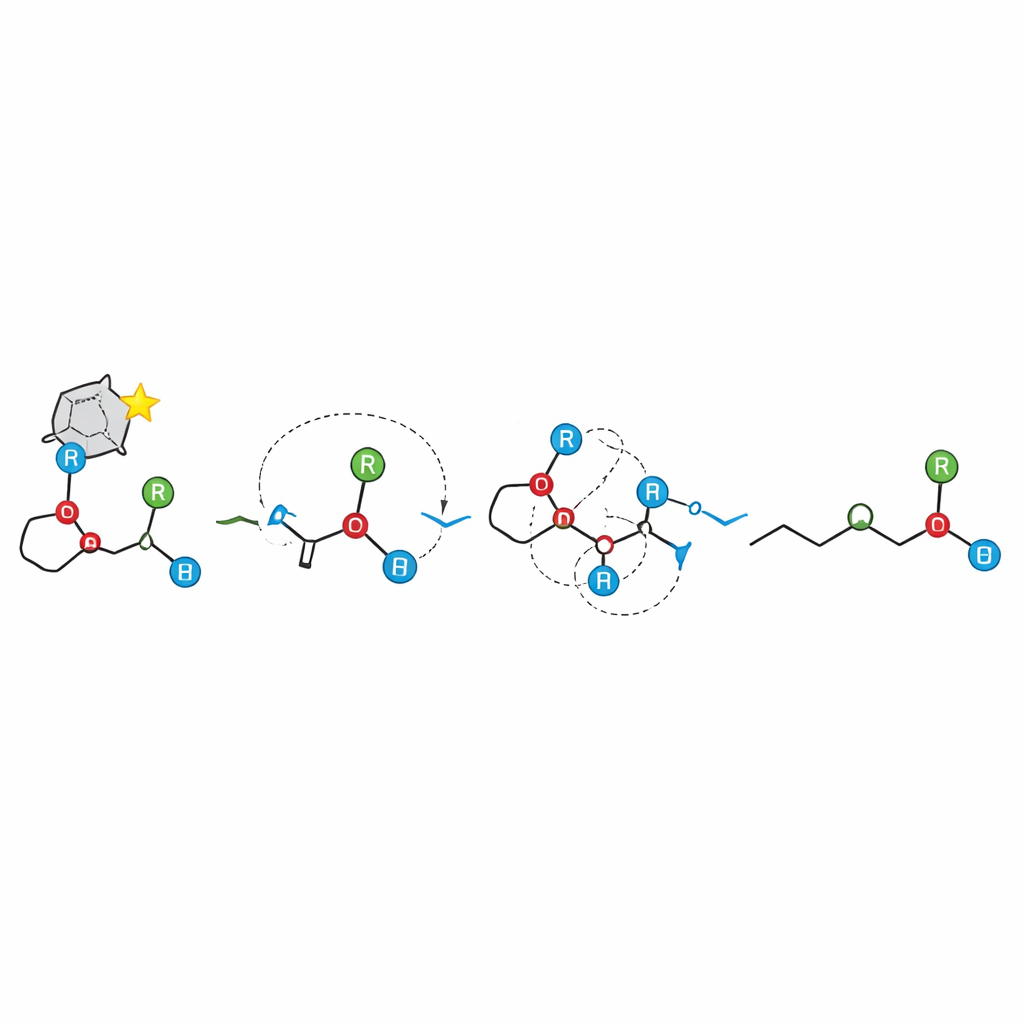
Klasyczne wyjaśnienia zakładały, że produkty [1,2]-Wittiga powstają przez rozerwanie wiązania i utworzenie luźnej pary rodników, które potem rekombinują — obraz ten sprawiał, że precyzyjna kontrola stereochemiczna wydawała się mało prawdopodobna. Nowe badania przedstawiają inny obraz. Poprzez staranne eksperymenty — w tym próby wychwycenia z użyciem dodatków wrażliwych na rodniki, testy „crossover” mieszające różne molekuły oraz szczegółowy monitoring czasowo‑zależny za pomocą NMR — autorzy pokazują, że reakcja przebiega przez specyficzny pośrednik powstały w przemieszczeniu [2,3] i że atomy pozostają sparowane w obrębie jednej cząsteczki zamiast wymieniać partnerów. Drugi krok zachowuje się jak formalnie zabronione przemieszczenie [1,3], lecz w praktyce rozwija się przez fragmentację do ściśle związanej pary jonowej, która ponownie łączy się w wysoce uporządkowany sposób, zachowując konfigurację w centrum chiralnym.
Komputery potwierdzają ukryte etapy
Aby poprzeć ten mechanistyczny obraz, zespół przeprowadził obszerne obliczenia kwantowo‑chemiczne na realistycznych modelach katalizatora i substratów. Obliczenia ujawniają, dlaczego jeden enantiomer jest faworyzowany w pierwszym kroku: preferowany stan przejściowy tworzy sieć trzech silnych wiązań wodorowych oraz korzystną interakcję stapiania między pierścieniami aromatycznymi, podczas gdy konkurencyjne ułożenia cierpią z powodu słabszych interakcji i zatłoczenia sterycznego. Dla drugiego kroku obliczenia nie znajdują pojedynczej, gładkiej, skoordynowanej ścieżki; zamiast tego wspierają etapową jonową fragmentację z umiarkowanym progiem energetycznym, po której następuje niemal bezbarierowa rekombinacja. Przewidywany próg energetyczny ściśle odpowiada zmierzonemu doświadczalnie, co wzmacnia argument za mechanizmem pary jonowej.
Implikacje dla budowy cząsteczek chiralnych
Z praktycznego punktu widzenia praca ta dostarcza chemikom syntetycznym solidnego nowego narzędzia do wytwarzania chiralnych alkoholi trzeciorzędowych z łatwo dostępnych eterów allylowych oraz określa, które modyfikacje strukturalne pomagają, a które przeszkadzają w tym procesie. Szerzej, demonstruje, że nawet gdy reakcja przebiega przez naładowane fragmenty, informacja stereochemiczna może być przekazana z niezwykłą wiernością, pod warunkiem że te fragmenty pozostają blisko związane. Obalając rodnikowy pogląd na [1,2]-przemieszczenie Wittiga i prezentując wysoce selektywną kaskadę jonową, badanie otwiera drzwi do reinterpretacji i przeprojektowania innych złożonych reakcji przestawiania wiązań w celu osiągnięcia precyzyjnej kontroli 3D.
Cytowanie: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
Słowa kluczowe: kataliza asymetryczna, przemieszczenie sigmatropowe, chiralne alkohole trzeciorzędowe, mechanizm reakcji, synteza organiczna