Clear Sky Science · it
La cascata catalitica enantioselettiva della riorganizzazione [1,2]-Wittig degli eteri allilici
Trasformare il disordine molecolare in ordine
I chimici spesso vogliono costruire molecole che siano selettive per l’immagine speculare, perché il nostro corpo distingue tra versioni “manopol” e “manodestra”. Questo articolo affronta un problema di lunga data in quell’ambito: come indirizzare un tipo di reazione notoriamente indisciplinata di riorganizzazione dei legami in modo che produca prevalentemente una sola immagine speculare invece di una miscela casuale. Gli autori non solo trovano un modo per farlo, ma dimostrano anche che la reazione procede attraverso una via inaspettata che ribalta decenni di idee consolidate sui libri di testo.
Perché questi cambi di forma sono importanti
Molte reazioni potenti in chimica organica operano spostando silenziosamente i legami all’interno di una molecola invece di rompere tutto e ricominciare da capo. Questi “riarrangiamenti” sono apprezzati perché sprecano poca materia e possono costruire strutture complesse in un singolo passaggio. Tra questi, una serie di trasformazioni note come riorganizzamenti di Wittig possono convertire eteri semplici in alcoli preziosi. Tuttavia, una versione particolare, la cosiddetta riorganizzazione [1,2]-Wittig degli eteri allilici, è stata difficile da controllare: tipicamente produce miscele di prodotti e, cosa cruciale, tende a mescolare la disposizione tridimensionale degli atomi invece di preservare o creare una singola forma enantiomerica.
Una nuova via a cascata
I ricercatori mostrano che questa reazione problematica può essere domata inserendola in una cascata a due passi guidata da un catalizzatore organico appositamente progettato. Il loro catalizzatore, chiamato iminofosforano bifunzionale, è sia una base eccezionalmente forte sia un ambiente stereochimicamente definito. Innanzitutto, induce uno spostamento di legame ben controllato noto come riorganizzazione [2,3], che costruisce un alcol terziario chirale con forte preferenza per un enantiomero. Poi, in condizioni basiche, questo intermedio si riorganizza di nuovo nel prodotto finale della riorganizzazione [1,2]-Wittig. Su molti materiali di partenza diversi, la sequenza fornisce in modo affidabile alcoli omoallilici chirali in buoni rendimenti e con alti rapporti enantiomerici, ovvero una forma enantiomerica prevale nettamente.
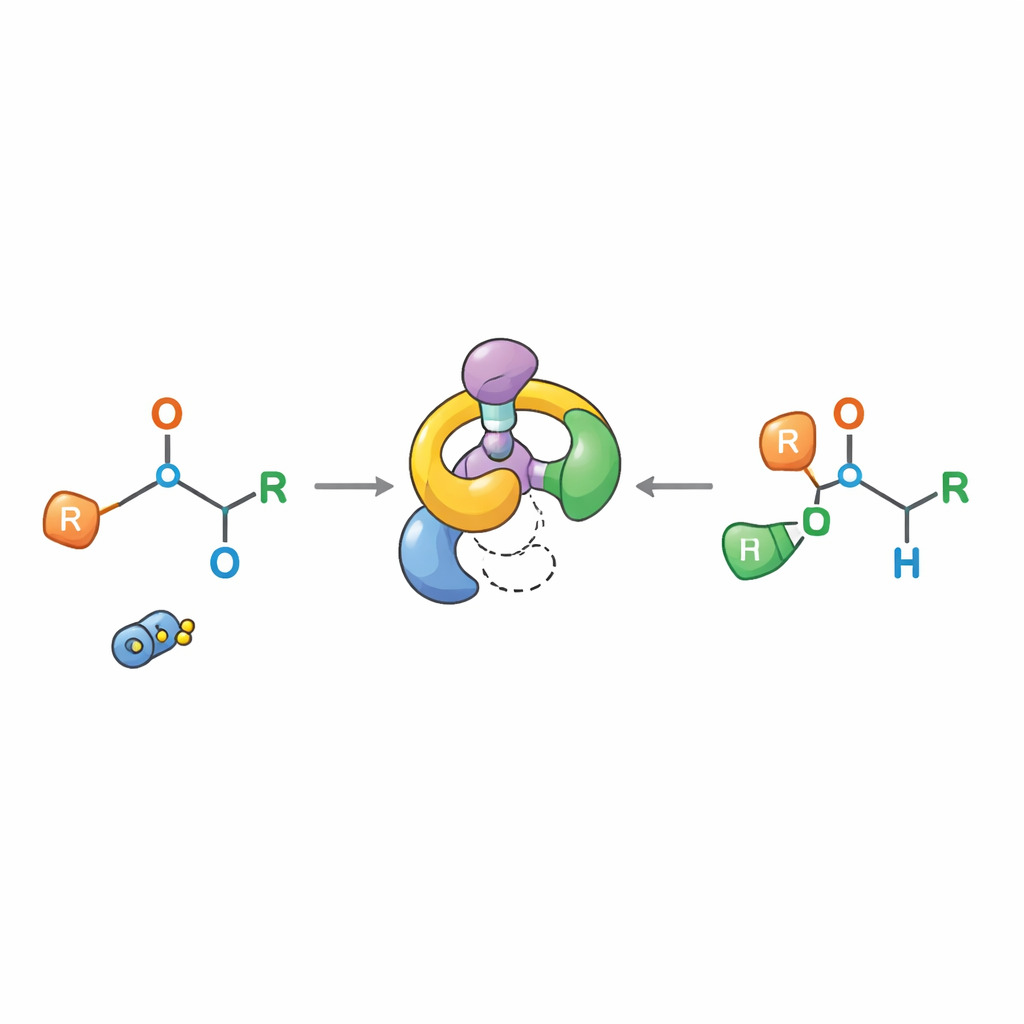
Indagare come la reazione funziona realmente
Le spiegazioni classiche sostenevano che i prodotti [1,2]-Wittig derivassero dalla rottura di un legame per formare una coppia di radicali liberi che poi si ricombinano, un quadro che rendeva il controllo stereochimico preciso poco probabile. Il nuovo lavoro dipinge un quadro diverso. Attraverso esperimenti accurati — tra cui tentativi di intrappolamento con additivi sensibili ai radicali, test di “crossover” che mescolano diverse molecole e monitoraggi NMR temporali dettagliati — gli autori mostrano che la reazione procede attraverso un intermedio specifico riorganizzato [2,3] e che gli atomi restano associati all’interno della stessa molecola invece di scambiarsi partner. Il secondo passo si comporta come un formalmente proibito riorganizzazione [1,3], ma in pratica si svolge tramite frammentazione in una coppia ionica strettamente associata che si ricompone in modo altamente ordinato, preservando la configurazione del centro chirale.
I calcoli confermano i passaggi nascosti
Per supportare questo quadro meccanicistico, il team ha condotto estesi calcoli quantomeccanici su modelli realistici del catalizzatore e dei substrati. Queste computazioni rivelano perché un enantiomero è favorito nel primo passo: lo stato di transizione preferito stabilisce una rete di tre forti legami a idrogeno e un’interazione di impilamento favorevole tra anelli aromatici, mentre gli arrangiamenti concorrenti soffrono di interazioni più deboli e ingombro sterico. Per il secondo passo, i calcoli non trovano una singola via concertata e continua; al contrario, supportano una frammentazione ionica passo-passo con una barriera energetica modesta, seguita da una ricombinazione quasi priva di barriera. La barriera energetica prevista si avvicina molto a quella misurata sperimentalmente, rafforzando l’ipotesi del meccanismo a coppia ionica.
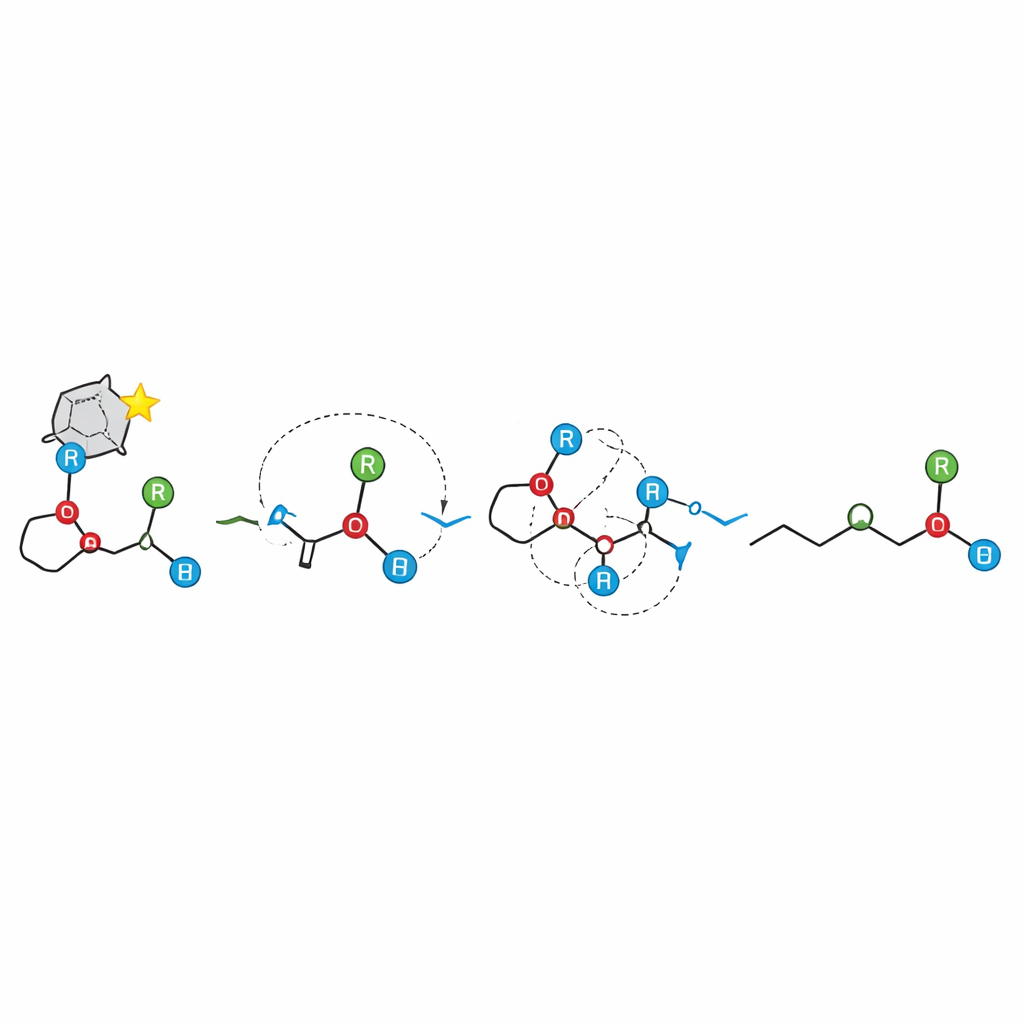
Implicazioni per la costruzione di molecole chirali
Da un punto di vista pratico, questo lavoro fornisce ai chimici sintetici un nuovo strumento robusto per ottenere alcoli terziari chirali da eteri allilici facilmente reperibili e mappa quali modifiche strutturali favoriscono o ostacolano il processo. Più in generale, dimostra che anche quando una reazione procede tramite frammenti carichi, l’informazione stereochimica può essere trasmessa con notevole fedeltà, purché quei frammenti rimangano strettamente associati. Ribaltando la visione basata sui radicali della riorganizzazione [1,2]-Wittig e mostrando una cascata ionica altamente selettiva, lo studio apre la strada a ripensare e riprogettare altre reazioni complesse di riorganizzazione dei legami per ottenere un controllo tridimensionale preciso.
Citazione: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
Parole chiave: catalisi asimmetrica, riarrangiamento sigmatropico, alcoli terziari chirali, meccanismo di reazione, sintesi organica