Clear Sky Science · ru
Каталитическая энантиоселективная каскадная [1,2]-Виттиг-переноска аллильных эфиров
Превращение молекулярного хаоса в порядок
Химики часто стремятся синтезировать молекулы с предпочтительной «зеркальной» формой, поскольку биологические системы различают «левые» и «правые» варианты. В этой статье решается давняя задача в этой области: как управлять печально известным непослушным типом реакции перестановки связей так, чтобы она давала преимущественно один энантиомер, а не случайную смесь. Авторы не только находят способ это сделать, но и показывают, что реакция идёт по неожиданному пути, который опрокидывает многолетние представления из учебников.
Почему эти изменения формы имеют значение
Во многих мощных реакциях в органической химии связи переорганизуются внутри молекулы, а не разрываются и собираются заново — это позволяет экономно расходовать сырьё и строить сложные структуры в один шаг. Среди таких процессов есть перестановки Виттига, которые превращают простые эфиры в ценные спирты. Однако особая версия — так называемая [1,2]-Виттиг-переноска аллильных эфиров — трудно поддаётся контролю: она обычно даёт смеси продуктов и, что важно, часто перемешивает трёхмерную организацию атомов, вместо того чтобы сохранять или формировать один стереовертикал.
Новый каскадный путь
Исследователи показывают, что эту проблемную реакцию можно обуздать, включив её в двухступенчатый каскад, управляемый специально разработанным органическим катализатором. Их катализатор, называемый бифункциональным иминофосфореном, сочетает в себе чрезвычайно сильное основное действие и строго «хиральную» среду. Сначала он запускает хорошо контролируемую перестановку типа [2,3], которая формирует хиральный третичный спирт с очень высоким преобладанием одного энантиомера. Затем, в основных условиях, этот интермедиат тихо перераспределяется во финальный продукт [1,2]-Виттиг. Для множества разных исходных соединений последовательность надежно даёт хиральные гомоаллильные спирты в хороших выходах и с высокими энантиомерными отношениями, то есть одна стереоформа доминирует.
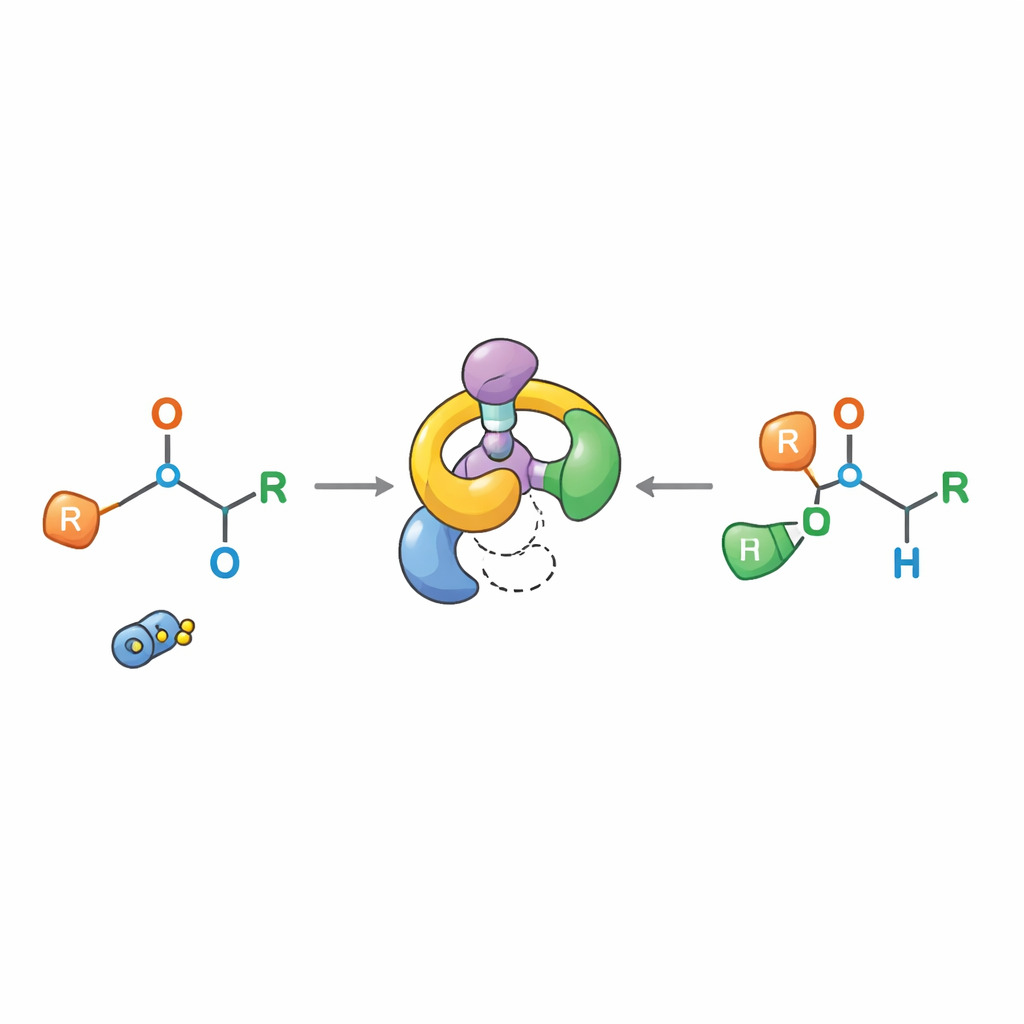
Изучение реального механизма реакции
Классические объяснения утверждали, что продукты [1,2]-Виттиг возникают через разрыв связи с образованием свободных радикалов, которые затем рекомбинируют, — картина, делающая точный стереоконтроль маловероятным. Новая работа рисует другую картину. Через аккуратные эксперименты — включая попытки ловли радикалов с чувствительными к радикалам добавками, «кроссовер»-тесты с перемешиванием разных молекул и детальное временное NMR-мониторирование — авторы показывают, что реакция проходит через специфический интермедиат после [2,3]-перестановки и что атомы остаются связанными в рамках одной молекулы, а не меняют партнёров. Вторая ступень ведёт себя как формально запретная [1,3]-перестановка, но на практике разворачивается через фрагментацию с образованием тесно связанной ионной пары, которая затем упорядоченно собирается обратно, сохраняя конфигурацию в хиральном центре.
Вычисления подтверждают скрытые этапы
Чтобы подкрепить эту механистическую картину, команда выполнила обширные квантово‑химические расчёты на реалистичных моделях катализатора и субстратов. Эти вычисления показывают, почему в первой стадии предпочтение отдается одному энантиомеру: предпочтительное переходное состояние формирует сеть из трёх сильных водородных связей и благоприятное стекинговое взаимодействие между ароматическими кольцами, тогда как конкурирующие расположения страдают от более слабых взаимодействий и стерического напряжения. Для второй стадии расчёты не обнаружили единого гладкого кооперативного пути; вместо этого они поддерживают пошаговую ионную фрагментацию с умеренным энергетическим барьером, за которой следует почти безбарьерная рекомбинация. Прогнозируемый энергетический барьер хорошо совпадает с экспериментально измеренным, что усиливает аргумент в пользу механизма через ионную пару.
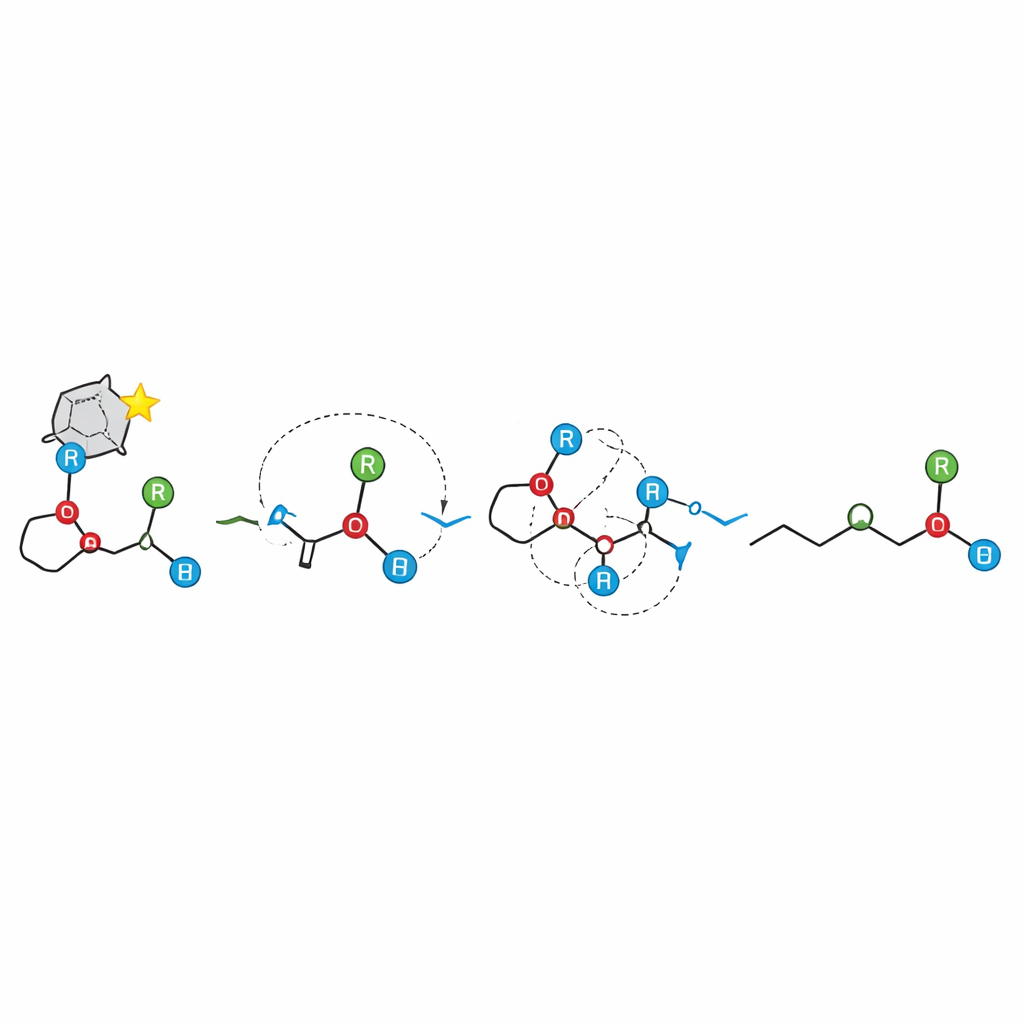
Последствия для синтеза хиральных молекул
С практической точки зрения эта работа даёт синтетическим химикам надёжный новый инструмент для получения хиральных третичных спиртов из доступных аллильных эфиров и описывает, какие структурные изменения помогают или мешают процессу. В более широком смысле она демонстрирует, что даже при участии заряженных фрагментов стереоинформация может передаваться с высокой точностью, если эти фрагменты остаются тесно связанными. Опрокинув представление о радикальном механизме [1,2]-Виттиг‑перестановки и показав высоко селективный ионный каскад, исследование открывает путь к переосмыслению и переработке других сложных реакций перестановки связей для достижения точного контроля в трёх измерениях.
Цитирование: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
Ключевые слова: асимметричный катализ, сигматропная реаранжировка, хиральные третичные спирты, механизм реакции, органический синтез