Clear Sky Science · pt
A cascata catalítica enantioseletiva da rearranjo [1,2]-Wittig de éteres allylicos
Transformando Desordem Molecular em Ordem
Químicos frequentemente desejam construir moléculas com seletividade por imagem especular, porque nossos corpos distinguem versões “canhotas” e “destras”. Este artigo aborda um enigma antigo nessa área: como controlar um tipo de reação de troca de ligações notoriamente indisciplinada para que produza predominantemente uma imagem especular em vez de uma mistura aleatória. Os autores não apenas encontram uma forma de fazer isso, como também mostram que a reação ocorre por um caminho inesperado que derruba décadas de ideias consagradas nos livros-texto.
Por Que Essas Mudanças de Forma Importam
Muitas reações poderosas na química orgânica operam deslizando ligações dentro de uma molécula em vez de quebrar tudo e recomeçar. Esses “rearranjos” são valorizados porque desperdiçam pouco material e podem construir estruturas complexas em um único passo. Entre eles, um conjunto de movimentos conhecidos como rearranjos de Wittig pode transformar éteres simples em álcoois valiosos. No entanto, uma versão particular, o chamado rearranjo [1,2]-Wittig de éteres allylicos, tem sido difícil de controlar: tipicamente gera misturas de produtos e, crucialmente, tende a embaralhar a disposição 3D dos átomos em vez de preservar ou criar uma única forma mãos.
Um Novo Caminho em Cascata
Os pesquisadores mostram que essa reação problemática pode ser domada ao integrá‑la a uma cascata de duas etapas guiada por um catalisador orgânico especialmente desenhado. Seu catalisador, chamado iminofosforano bifuncional, é simultaneamente uma base excepcionalmente forte e um ambiente quiral preciso. Primeiro, ele desencadeia um deslocamento de ligação bem comportado conhecido como rearranjo [2,3], que constrói um álcool terciário quiral com alta preferência por uma das imagens especulares. Em seguida, sob condições básicas, esse intermediário silenciosamente se reorganiza novamente no produto final do [1,2]-Wittig. Em muitos substratos diferentes, a sequência fornece de maneira confiável álcoois homoallylicos quirais com bons rendimentos e altas razões enantioméricas, o que significa que uma forma mão domina fortemente.
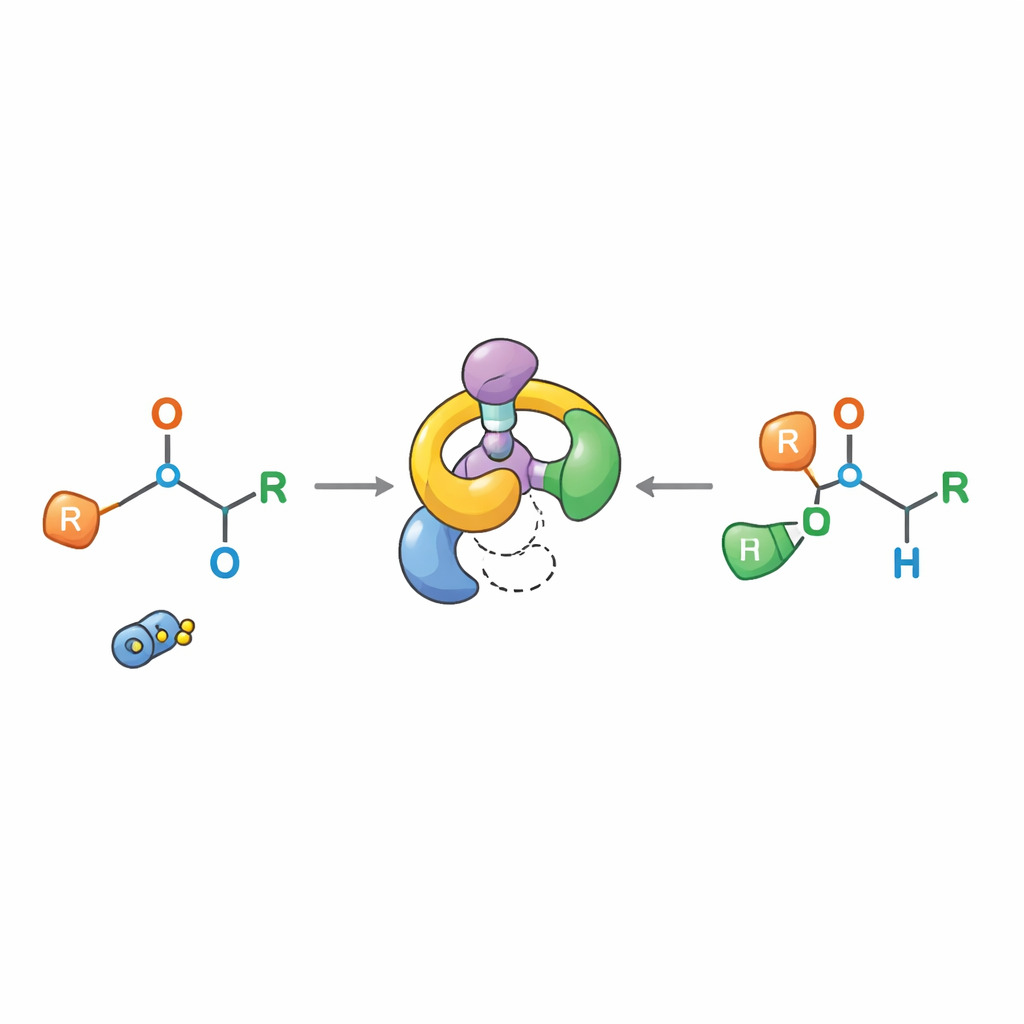
Investigando Como a Reação Realmente Funciona
Explicações clássicas sustentavam que os produtos do [1,2]-Wittig surgiam pela quebra de uma ligação formando um par livre de radicais que depois se recombinava, uma imagem que tornava o controle estereoquímico preciso improvável. O novo trabalho pinta um quadro diferente. Através de experimentos cuidadosos — incluindo tentativas de captura com aditivos sensíveis a radicais, testes de “crossover” que misturam moléculas diferentes e monitoramento detalhado por RMN com resolução temporal — os autores mostram que a reação prossegue por um intermediário específico rearranjado via [2,3] e que os átomos permanecem pareados dentro de uma única molécula em vez de trocarem parceiros. A segunda etapa comporta‑se como um formalmente proibido rearranjo [1,3], mas na prática se desenrola por fragmentação em um par iônico fortemente associado que se recombina de maneira altamente ordenada, preservando a configuração no centro quiral.
Computadores Confirmam os Passos Ocultos
Para apoiar esse quadro mecanístico, a equipe realizou extensos cálculos quântico‑químicos em modelos realistas do catalisador e dos substratos. Esses cálculos revelam por que um enantiômero é favorecido na primeira etapa: o estado de transição preferido forma uma rede de três fortes ligações de hidrogênio e uma interação de empilhamento favorável entre anéis aromáticos, enquanto arranjos concorrentes sofrem com interações mais fracas e impedimento estérico. Para a segunda etapa, os cálculos não encontram um único caminho concertado suave; em vez disso, sustentam uma fragmentação iônica em etapas com uma barreira de energia moderada, seguida por recombinação quase sem barreira. A barreira de energia prevista coincide de perto com a medida experimentalmente, fortalecendo a hipótese do mecanismo por par iônico.
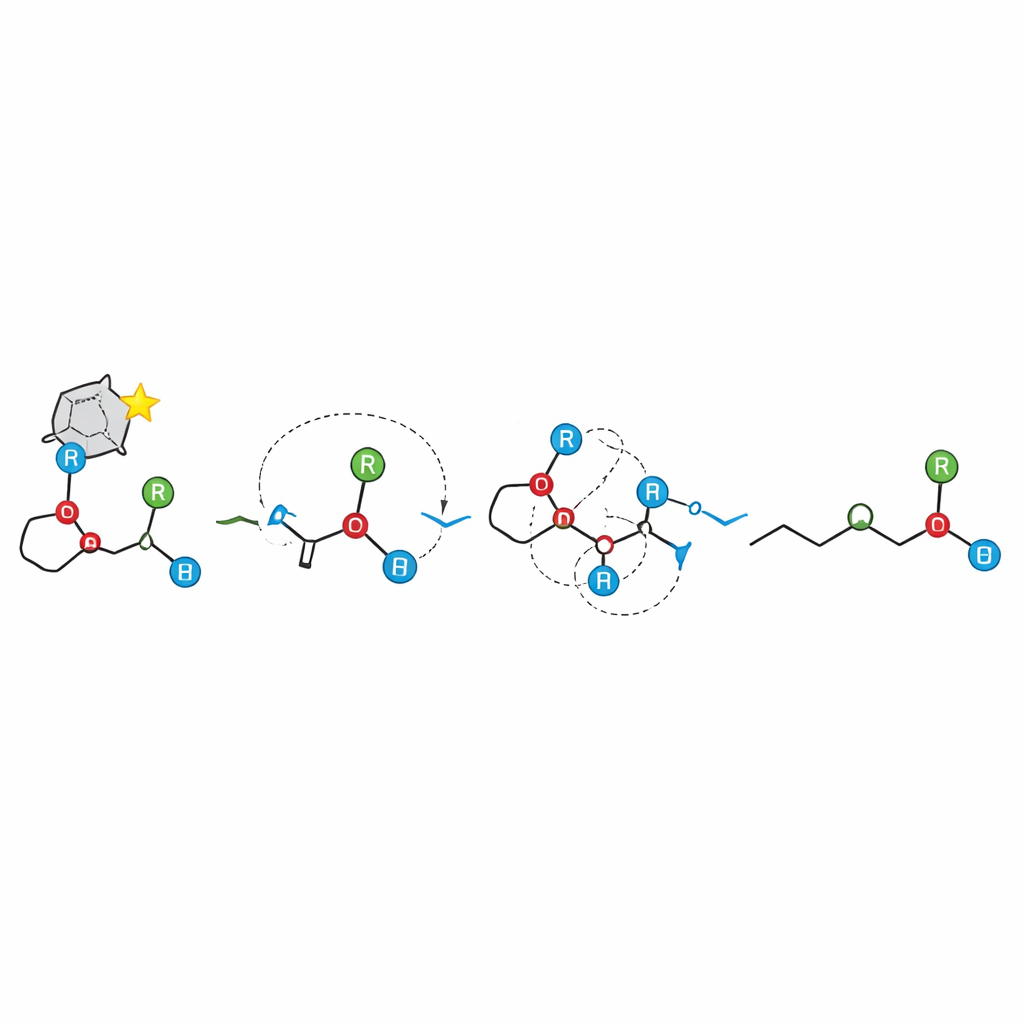
Implicações para Construir Moléculas Quirais
Do ponto de vista prático, este trabalho fornece aos químicos sintéticos uma nova ferramenta robusta para preparar álcoois terciários quirais a partir de éteres allylicos prontamente disponíveis, e mapeia quais ajustes estruturais ajudam ou dificultam o processo. Mais amplamente, demonstra que mesmo quando uma reação prossegue por fragmentos carregados, a informação estereoquímica pode ser transmitida com notável fidelidade, desde que esses fragmentos permaneçam estreitamente associados. Ao derrubar a visão baseada em radicais do rearranjo [1,2]-Wittig e ao mostrar uma cascata iônica altamente seletiva, o estudo abre caminho para repensar e redesenhar outras reações complexas de rearranjo de ligações para alcançar controle 3D preciso.
Citação: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
Palavras-chave: catálise assimétrica, rearranjo sigmatrópico, álcoois terciários quirais, mecanismo de reação, síntese orgânica