Clear Sky Science · es
La cascada catalítica enantioselectiva de la reorganización [1,2]-Wittig de éteres alílicos
Convertir el caos molecular en orden
Los químicos a menudo buscan construir moléculas con selectividad de imagen especular, porque nuestros cuerpos distinguen entre las versiones “izquierda” y “derecha”. Este artículo aborda un enigma de larga data en ese campo: cómo dirigir un tipo de reacción de reorganización de enlaces notoriamente turbulento para que produzca mayoritariamente una imagen especular en lugar de una mezcla aleatoria. Los autores no solo encuentran una manera de lograrlo, sino que además muestran que la reacción transcurre por una vía inesperada que derriba décadas de pensamiento de libro de texto.
Por qué importan estos cambios de forma
Muchas reacciones potentes en química orgánica funcionan desplazando enlaces dentro de una molécula en lugar de romperlo todo y recomponerlo. Estos “reordenamientos” son valiosos porque desperdician muy poco material y pueden construir estructuras complejas en un solo paso. Entre ellos, un conjunto de movimientos conocidos como reordenamientos de Wittig puede convertir éteres simples en alcoholes valiosos. Sin embargo, una versión en particular, la llamada reorganización [1,2]-Wittig de éteres alílicos, ha sido difícil de controlar: típicamente da mezclas de productos y, lo que es crucial, tiende a barajar la disposición tridimensional de los átomos en lugar de preservar o crear una única forma quiral.
Una nueva vía en cascada
Los investigadores muestran que esta reacción problemática puede domarse integrándola en una cascada de dos pasos guiada por un catalizador orgánico especialmente diseñado. Su catalizador, denominado iminofosforano bifuncional, es tanto una base excepcionalmente fuerte como un entorno “quiral” preciso. Primero, induce un desplazamiento de enlace bien comportado conocido como reorganización [2,3], que construye un alcohol terciario quiral con muy alta preferencia por una de las imágenes especulares. Luego, en condiciones básicas, este intermedio se reordena silenciosamente de nuevo para dar el producto final de la reorganización [1,2]-Wittig. A través de muchos materiales de partida distintos, la secuencia entrega de forma fiable alcoholes homoalílicos quirales en buenos rendimientos y con altas relaciones enantioméricas, lo que significa que una forma quiral domina claramente.
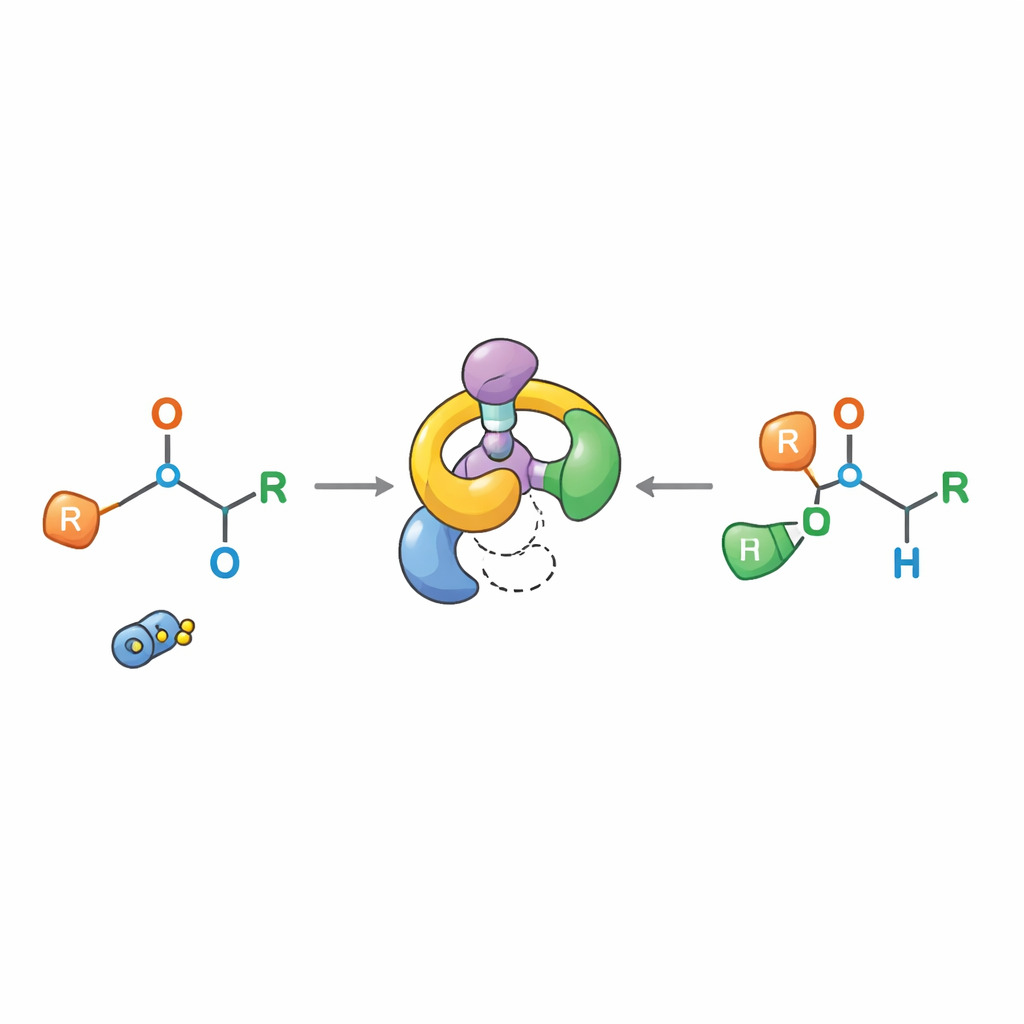
Investigar cómo funciona realmente la reacción
Las explicaciones clásicas sostenían que los productos [1,2]-Wittig provenían de la ruptura de un enlace para formar un par laxo de radicales que luego se recombinaban, una imagen que hacía que el control estereoquímico preciso pareciera poco probable. El nuevo trabajo pinta una imagen diferente. Mediante experimentos cuidadosos —incluyendo intentos de atrapamiento con aditivos sensibles a radicales, pruebas de “crossover” que mezclan moléculas diferentes y monitorización por RMN con resolución temporal— los autores muestran que la reacción progresa a través de un intermedio específico reordenado por [2,3] y que los átomos permanecen emparejados dentro de una sola molécula en lugar de intercambiar parejas. El segundo paso se comporta como un reordenamiento [1,3] formalmente prohibido, pero en la práctica se desarrolla mediante fragmentación en un par iónico estrechamente asociado que vuelve a unirse de forma muy ordenada, preservando la configuración en el centro quiral.
Los ordenadores confirman los pasos ocultos
Para respaldar este panorama mecanístico, el equipo realizó extensos cálculos cuántico‑químicos sobre modelos realistas del catalizador y los sustratos. Estos cálculos revelan por qué un enantiómero se favorece en el primer paso: el estado de transición preferido forma una red de tres enlaces de hidrógeno fuertes y una interacción de apilamiento favorable entre anillos aromáticos, mientras que las disposiciones competidoras sufren interacciones más débiles y hacinamiento estérico. Para el segundo paso, los cálculos no encuentran una vía concertada única y continua; en su lugar, apoyan una fragmentación iónica escalonada con una barrera energética moderada, seguida de una recombinación prácticamente sin barrera. La barrera energética predicha coincide estrechamente con la medida experimentalmente, reforzando el caso a favor del mecanismo por par iónico.
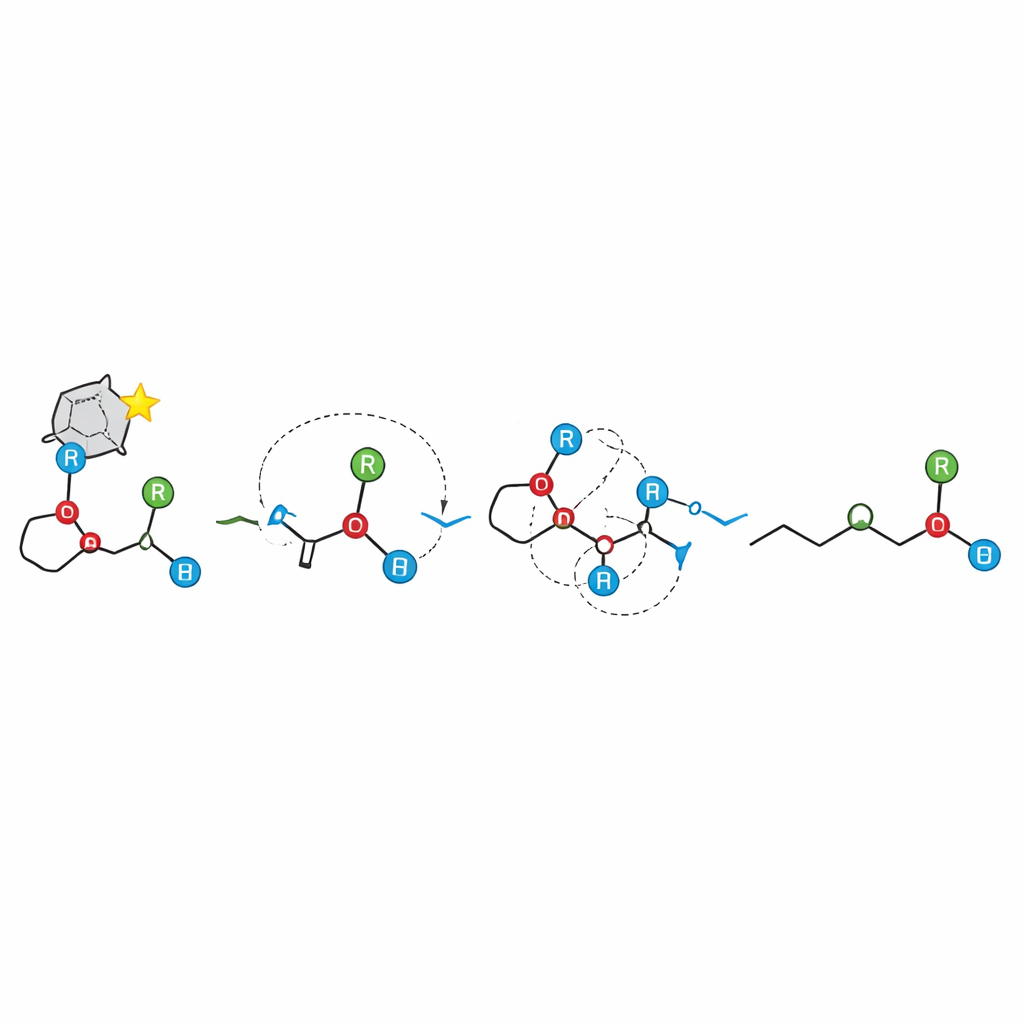
Implicaciones para la construcción de moléculas quirales
Desde un punto de vista práctico, este trabajo proporciona a los químicos sintéticos una nueva herramienta sólida para obtener alcoholes terciarios quirales a partir de éteres alílicos fácilmente disponibles, y traza qué ajustes estructurales ayudan o dificultan el proceso. Más ampliamente, demuestra que incluso cuando una reacción progresa a través de fragmentos cargados, la información estereoquímica puede transmitirse con fidelidad notable, siempre que esos fragmentos permanezcan estrechamente asociados. Al derribar la visión basada en radicales de la reorganización [1,2]-Wittig y mostrar una cascada iónica altamente selectiva, el estudio abre la puerta a replantear y rediseñar otras reacciones complejas de reordenamiento de enlaces para lograr un control 3D preciso.
Cita: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
Palabras clave: catálisis asimétrica, reordenamiento sigmatrópico, alcoholes terciarios quirales, mecanismo de reacción, síntesis orgánica