Clear Sky Science · fr
La cascade catalytique énantiosélective de réarrangement [1,2]-Wittig des éthers allyliques
Transformer le désordre moléculaire en ordre
Les chimistes cherchent souvent à construire des molécules qui sont sélectives vis‑à‑vis de leur image miroir, car nos organismes distinguent les versions « gauches » et « droites ». Cet article aborde une énigme de longue date dans ce domaine : comment contrôler un type de réaction notoirement capricieux d’échange de liaisons pour qu’elle produise majoritairement une seule énantiomère au lieu d’un mélange aléatoire. Les auteurs trouvent non seulement une solution, mais montrent aussi que la réaction suit une voie inattendue qui renverse des idées établies depuis des décennies.
Pourquoi ces changements de forme comptent
Beaucoup de réactions puissantes en chimie organique fonctionnent en faisant glisser des liaisons à l’intérieur d’une même molécule plutôt qu’en tout détruisant et en recommençant. Ces « réarrangements » sont précieux parce qu’ils gaspillent très peu de matière et permettent de construire des structures complexes en une seule étape. Parmi eux, une famille de transformations appelées réarrangements de Wittig peut convertir de simples groupes éther en alcools utiles. Cependant, une variante particulière, le réarrangement [1,2]-Wittig des éthers allyliques, a été difficile à maîtriser : il donne typiquement des mélanges de produits et, surtout, tend à brouiller l’agencement tridimensionnel des atomes au lieu de préserver ou de créer une seule configuration chirale.
Une nouvelle voie en cascade
Les chercheurs montrent que cette réaction problématique peut être domptée en l’intégrant dans une cascade en deux étapes pilotée par un catalyseur organique spécialement conçu. Leur catalyseur, appelé iminophosphorane bifonctionnel, est à la fois une base exceptionnellement forte et un environnement chirale précis. D’abord, il déclenche un déplacement de liaison bien maîtrisé connu sous le nom de réarrangement [2,3], qui construit un alcool tertiaire chiral avec une très forte préférence pour un énantiomère. Ensuite, en conditions basiques, cet intermédiaire se réorganise discrètement en produit final du [1,2]-Wittig. Sur une large gamme de substrats, la séquence fournit de manière fiable des alcools homoallyliques chiraux avec de bons rendements et des rapports énantiomériques élevés, ce qui signifie qu’une forme chirale domine nettement.
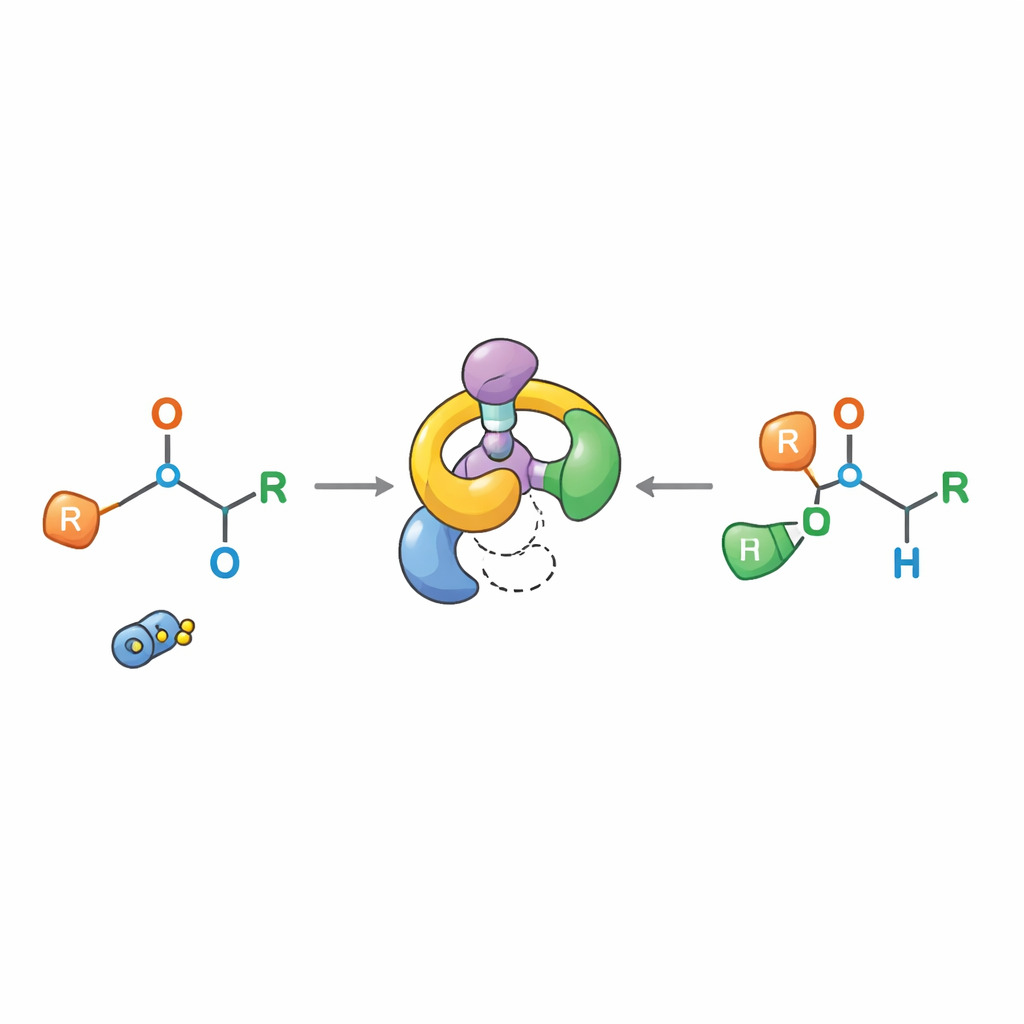
Explorer le véritable mécanisme de la réaction
Les explications classiques soutenaient que les produits [1,2]-Wittig provenaient de la rupture d’une liaison pour former une paire lâche de radicaux qui se recombinaient ensuite, un scénario qui rendait le contrôle stéréochimique précis peu probable. Le nouveau travail propose un autre tableau. Par des expériences soigneuses — incluant des tentatives de piégeage avec des additifs sensibles aux radicaux, des tests de « crossover » mélangeant différentes molécules et un suivi NMR chronologique détaillé — les auteurs montrent que la réaction passe par un intermédiaire spécifique issu du réarrangement [2,3] et que les atomes restent appariés au sein d’une même molécule plutôt que d’échanger leurs partenaires. La seconde étape se comporte comme un réarrangement [1,3] formellement interdit, mais en pratique elle se déroule via une fragmentation en une paire d’ions étroitement associée qui se recombine de manière très ordonnée, préservant la configuration du centre chiral.
Des calculs confirment les étapes cachées
Pour étayer ce paysage mécanistique, l’équipe a réalisé des calculs quantico‑chimiques étendus sur des modèles réalistes du catalyseur et des substrats. Ces calculs révèlent pourquoi un énantiomère est favorisé lors de la première étape : l’état de transition préféré forme un réseau de trois liaisons hydrogène fortes et une interaction de empilement bénéfique entre anneaux aromatiques, tandis que les arrangements concurrents souffrent d’interactions plus faibles et d’encombrement stérique. Pour la seconde étape, les calculs ne trouvent pas de voie concertée unique et continue ; au contraire, ils soutiennent une fragmentation ionique par étapes avec une barrière d’énergie modeste, suivie d’une recombinaison presque sans barrière. La barrière d’énergie prédite correspond de près à celle mesurée expérimentalement, renforçant l’argument en faveur du mécanisme en paire d’ions.
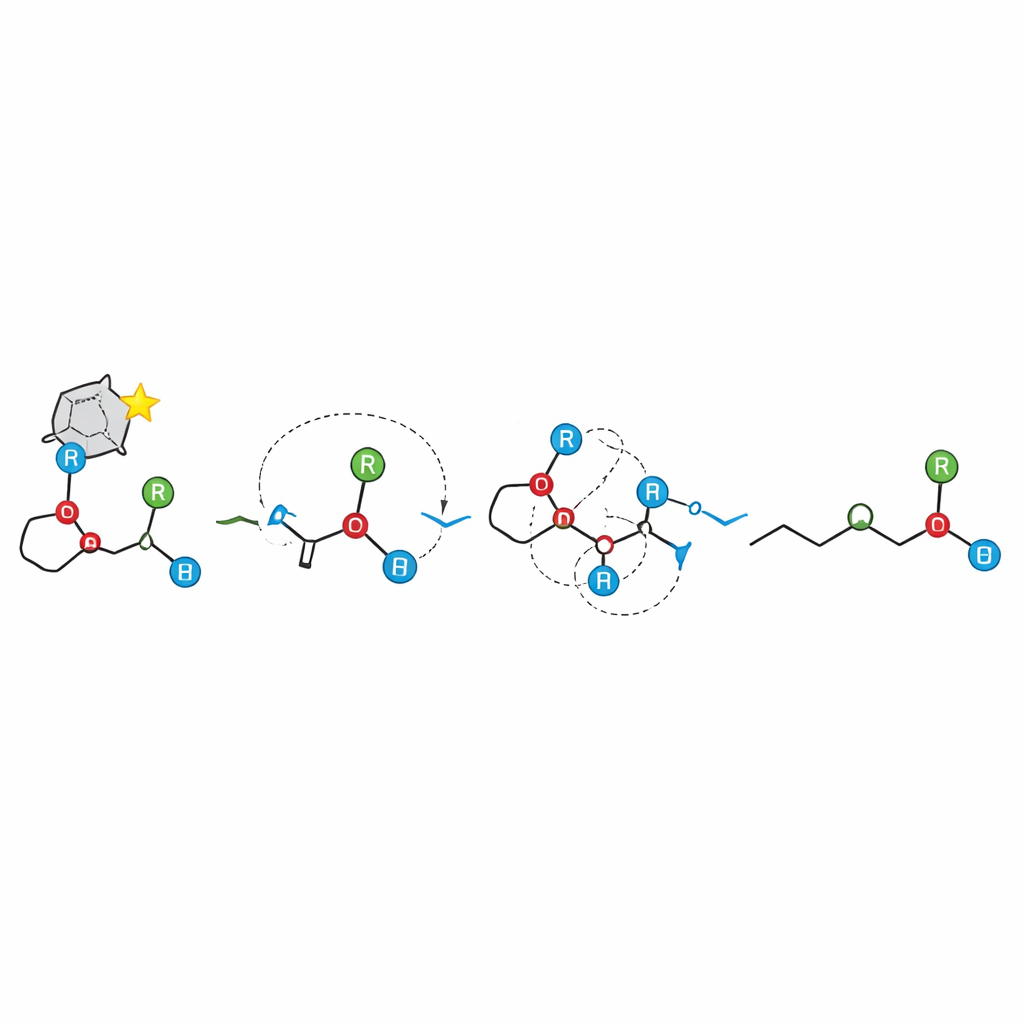
Conséquences pour la construction de molécules chirales
Du point de vue pratique, ce travail offre aux chimistes synthéticiens un nouvel outil robuste pour produire des alcools tertiaires chiraux à partir d’éthers allyliques facilement accessibles, et il cartographie les modifications structurales qui aident ou entravent le processus. Plus largement, il démontre que, même lorsqu’une réaction passe par des fragments chargés, l’information stéréochimique peut être transmise avec une fidélité remarquable, pourvu que ces fragments restent étroitement associés. En renversant la vision fondée sur des radicaux du réarrangement [1,2]-Wittig et en présentant une cascade ionique hautement sélective, l’étude ouvre la voie à repenser et redessiner d’autres réactions complexes de réarrangement de liaisons afin d’obtenir un contrôle tridimensionnel précis.
Citation: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
Mots-clés: catalyse asymétrique, réarrangement sigmatropique, alcools tertiaires chiraux, mécanisme réactionnel, synthèse organique