Clear Sky Science · sv
Den katalytiska enantioselektiva [1,2]-Wittig-omläggningskaskaden av allyletrar
Att förvandla molekylärt kaos till ordning
Kemister vill ofta konstruera molekyler som är spegelbildsselek-tiva, eftersom våra kroppar kan skilja på ”vänster‑” och ”höger‑”versioner. Denna artikel tar sig an ett länge olöst problem inom området: hur man styr en notoriskt besvärlig typ av bindningsomfördelningsreaktion så att den ger huvudsakligen ena spegelbilden i stället för en slumpmässig blandning. Författarna hittar inte bara ett sätt att göra detta, de visar också att reaktionen sker via en oväntad väg som ifrågasätter årtionden av lärobokstänkande.
Varför dessa formförändringar spelar roll
Många kraftfulla reaktioner i organisk kemi fungerar genom att diskret omfördela bindningar inom en molekyl i stället för att bryta upp allt och börja om. Dessa ”omläggningar” uppskattas eftersom de slösar minimalt med material och kan bygga komplexa strukturer i ett enda steg. Bland dem kan en uppsättning rörelser som kallas Wittig-omläggningar förvandla enkla ethergrupper till värdefulla alkoholer. En särskild variant, den så kallade [1,2]-Wittig-omläggningen av allyletrar, har dock varit svår att kontrollera: den ger typiskt produktblandningar och tenderar avgörande nog att skada molekylens tredimensionella ordning i stället för att bevara eller skapa en enskild handform.
En ny kaskadväg
Forskarna visar att denna problematiska reaktion kan tygla genom att göra den till en tvåstegs kaskad styrd av en särskild utformad organisk katalysator. Deras katalysator, en bifunktionell iminofosforan, är både en exceptionellt stark bas och en precis ”handad” omgivning. Först triggar den en välordnad bindningsförskjutning känd som en [2,3]-omläggning, som konstruerar en kiral tertiär alkohol med mycket hög preferens för en spegelbild. Sedan, under basiska förhållanden, omfördelar denna intermediär tyst igen till den slutliga [1,2]-Wittig-produkten. Över många olika startmaterial levererar sekvensen konsekvent kirala homoallyliska alkoholer i goda utbyten och med höga enantiomerförhållanden, vilket betyder att en handform dominerar starkt.
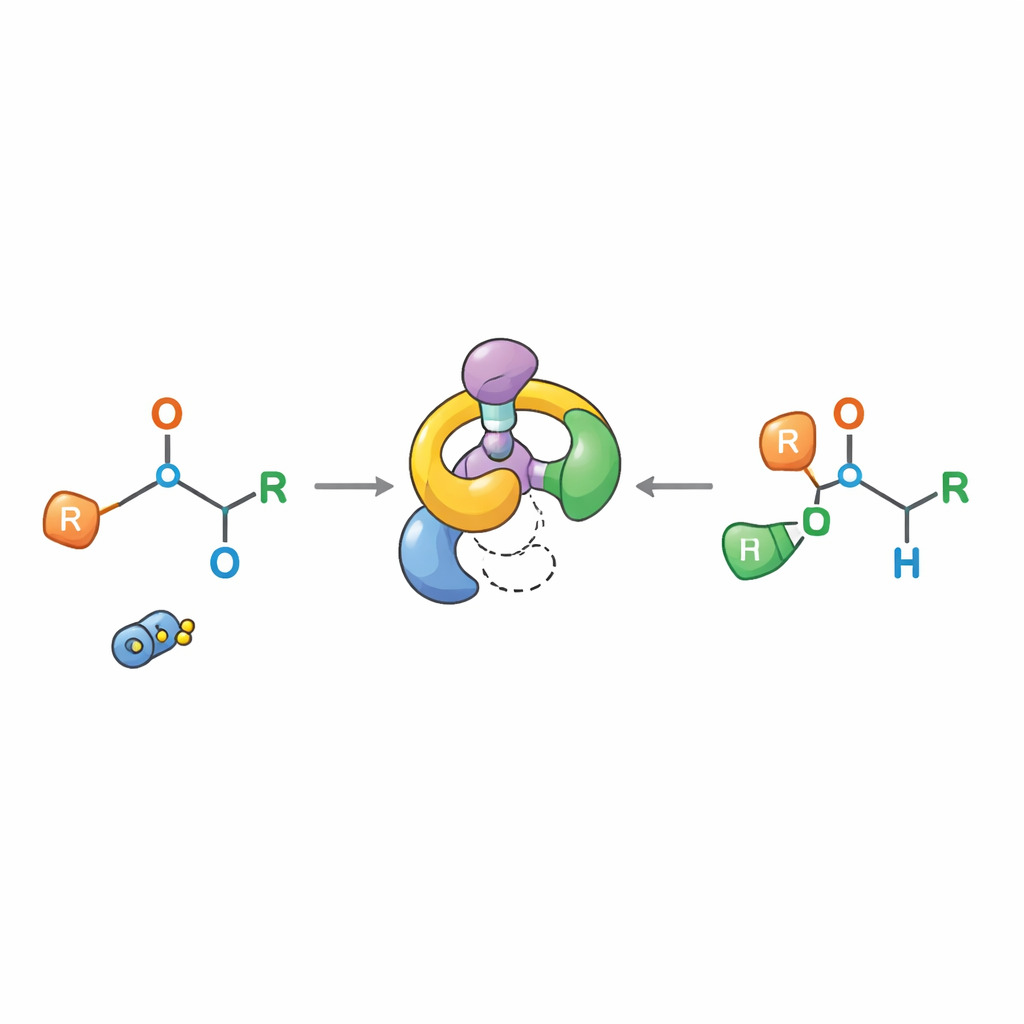
Undersöker hur reaktionen faktiskt fungerar
De klassiska förklaringarna hävdade att [1,2]-Wittig-produkter uppstod genom att en bindning bröts för att bilda ett löst par radikaler som senare åter förenades, en bild som gjorde precis stereokemisk kontroll osannolik. Det nya arbetet målar upp en annan bild. Genom noggranna experiment—inklusive fångstförsök med radikalkänsliga tillsatser, ”crossover”-tester som blandar olika molekyler och detaljerad tidsupplöst NMR-övervakning—visar författarna att reaktionen fortlöper via en specifik [2,3]-omlagd intermediär och att atomerna förblir parade inom en enskild molekyl i stället för att byta partner. Andra steget beter sig likt en formellt förbjuden [1,3]-omläggning, men i praktiken utvecklas det genom fragmentering till ett tätt associerat jonsystem som snabbt slår ihop sig igen på ett högst ordnat sätt och bevarar konfigurationen vid det kirala centret.
Datorberäkningar bekräftar de dolda stegen
För att stärka denna mekanistiska bild genomförde gruppen omfattande kvantkemiska beräkningar på realistiska modeller av katalysatorn och substraten. Dessa beräkningar visar varför ena enantiomeren gynnas i första steget: den föredragna övergångstillståndet bildar ett nätverk av tre starka vätebindningar och en fördelaktig staplingsinteraktion mellan aromatiska ringar, medan konkurrerande arrangemang lider av svagare interaktioner och sterisk trängsel. För det andra steget misslyckas beräkningarna med att hitta en enda, jämn, simultan väg; i stället stöder de en stegvist utförd jonisk fragmentering med en måttlig energibarriär, följt av nästan barriärfri återförening. Den förutsagda energibarriären stämmer väl överens med den som mätts experimentellt, vilket stärker fallet för jonskiktsmekanismen.
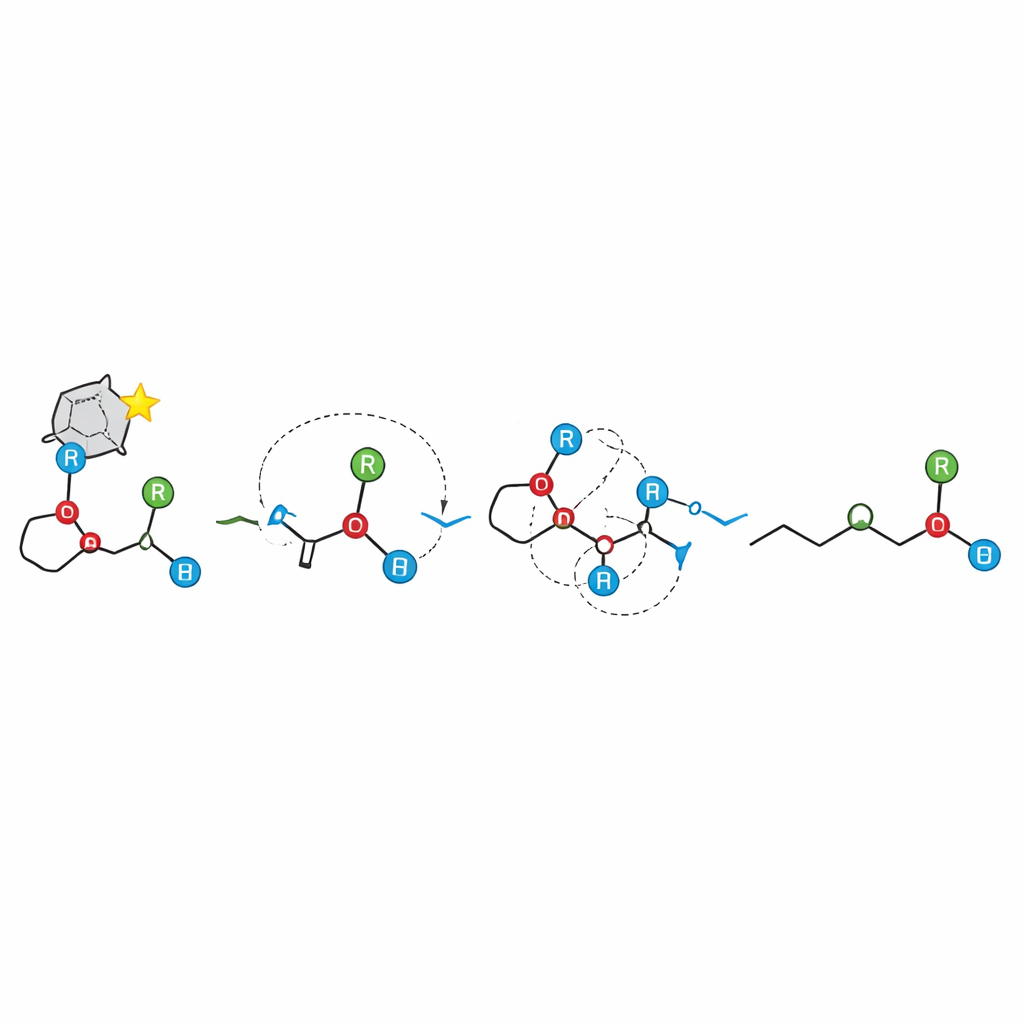
Konsekvenser för konstruktion av kirala molekyler
I praktiska termer ger detta arbete syntetiska kemister ett robust nytt verktyg för att framställa kirala tertiära alkoholer från lättillgängliga allyletrar, och det kartlägger vilka strukturella justeringar som hjälper eller hindrar processen. Mer generellt visar det att även när en reaktion går via laddade fragment kan stereokemisk information föras vidare med anmärkningsvärd trohet, så länge dessa fragment förblir nära associerade. Genom att kullkasta den radikalbaserade bilden av [1,2]-Wittig-omläggningen och visa upp en högselektiv jonisk kaskad, öppnar studien dörren för att ompröva och omdesigna andra komplexa bindningsomläggande reaktioner för att uppnå precis 3D-kontroll.
Citering: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
Nyckelord: asymmetrisk katalys, sigmatrop omläggning, kirala tertiära alkoholer, reaktionsmekanism, organisk syntes