Clear Sky Science · ja
アリルエーテルの触媒的不斉[1,2]-ウィッティヒ転位カスケード
分子の混沌を秩序へ変える
化学者はしばしば鏡像異性体を選択的に合成したがります。というのも、生体は「左手型」と「右手型」を区別するからです。本論文はこの長年の課題に取り組んでいます:制御が極めて難しい種類の結合再配置反応を、ランダムな混合物ではなく一方の鏡像体が優勢に得られるように導く方法を示しています。著者らはその手法を見いだすだけでなく、反応が教科書的な考えを覆す予期せぬ経路を経ることも明らかにしています。
なぜこれらの形変化が重要か
多くの強力な有機反応は、分子内で結合を巧みにすべらせることで進行し、大々的に分解して再構築するよりもずっと効率的です。こうした「転位」は廃棄物が少なく、一段で複雑な構造を作れるため重宝されます。中でもウィッティヒ転位と呼ばれる一群は、単純なエーテルを価値あるアルコールに変えることができます。しかし特にアリルエーテルの[1,2]-ウィッティヒ転位は制御が難しく、生成物が混合しやすく、重要な点として立体配置を保持したり一方の鏡像を選択したりするのではなく、しばしば3次元配列を乱してしまいます。
新しいカスケード経路
研究者たちは、この扱いにくい反応を特別に設計した有機触媒のもとで二段階のカスケードに組み込むことで制御可能にできることを示しました。彼らの触媒はビファンクショナルなイミノホスホラニで、非常に強い塩基性をもちつつ、精密な「手性」環境を提供します。まず、それは[2,3]-転位と呼ばれる挙動良好な結合移動を誘起し、高い光学選択性でキラルな第三級アルコールを構築します。続いて塩基条件下でこの中間体が静かに再配置して最終的な[1,2]-ウィッティヒ生成物になります。さまざまな出発物質にわたり、この連続反応はキラルなホモアリルアルコールを良好な収率と高いエナンチオマー比で安定して与え、一方の鏡像体が強く優勢になります。
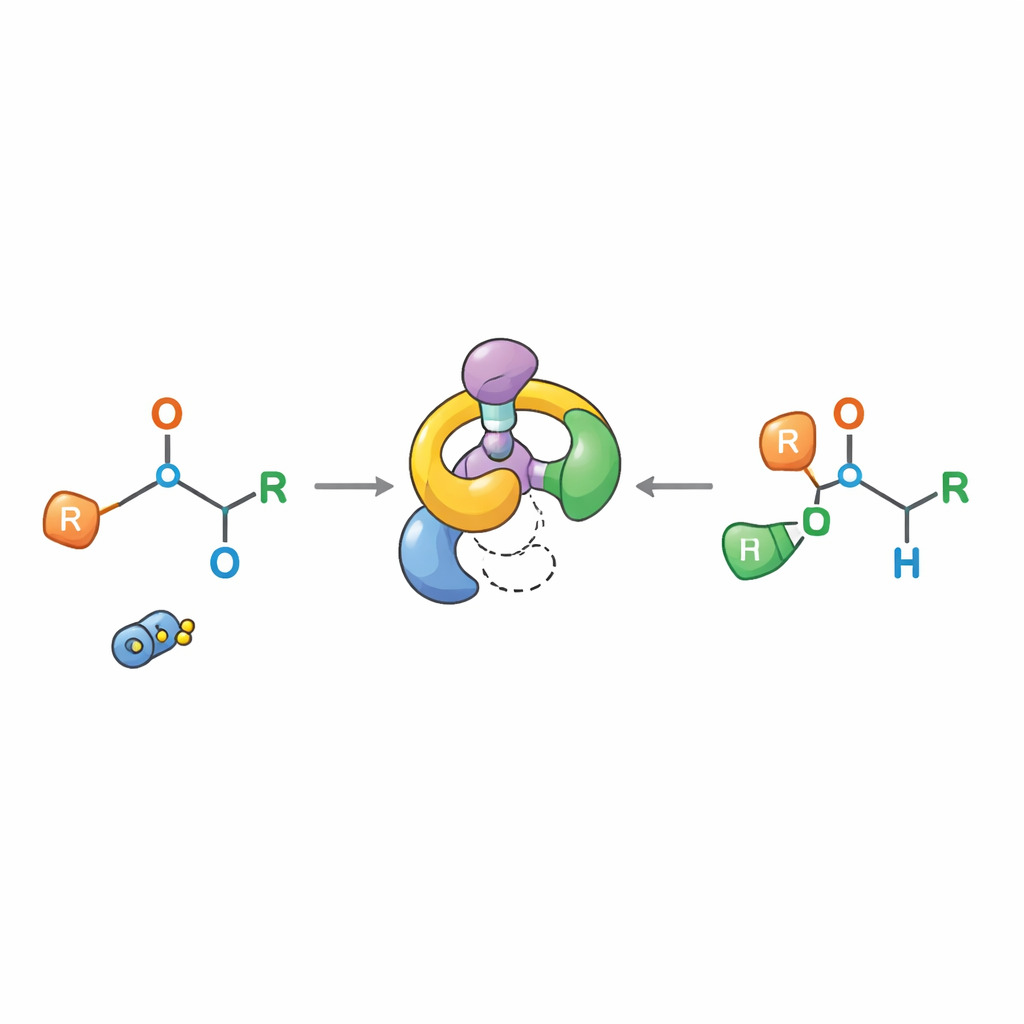
反応が実際にどのように進むかを探る
古典的な説明では、[1,2]-ウィッティヒ生成物は結合を切ってすぐ離れるラジカル対を形成し、それが後で再結合することで生じるとされてきました。この見方では精密な立体化学制御は期待しにくいものです。新しい研究は異なる像を示します。ラジカルに敏感な添加剤によるトラップ試験、異なる分子を混ぜる“クロスオーバー”試験、時間分解NMRによる詳細な追跡など慎重な実験を通じて、反応は特定の[2,3]-転位中間体を経由し、原子は分子内でペアのまま交換せずに進行することが示されました。第二段階は形式的には禁止された[1,3]-転位のように見えますが、実際には緊密に相互作用したイオン対への断片化を経て、非常に秩序立った形で再結合することで展開し、キラル中心の構成を保持します。
計算が示す隠れたステップ
この機構像を裏付けるため、チームは触媒と基質の実モデルに対して広範な量子化学計算を行いました。これらの計算は、第一段階である一方のエナンチオマーが優先される理由を示しています。好ましい遷移状態では3つの強い水素結合のネットワークと芳香環間の安定なスタッキング相互作用が形成され、競合する配座はより弱い相互作用と立体的圧迫を被ります。第二段階については、一つの滑らかな協奏的経路は見つからず、代わりに穏やかなエネルギー障壁を伴う段階的なイオン性断片化と、ほぼ障壁のない再結合を支持する結果が出ました。予測された活性化エネルギーは実験で測定された値とよく一致し、イオン対機構の主張を強めています。
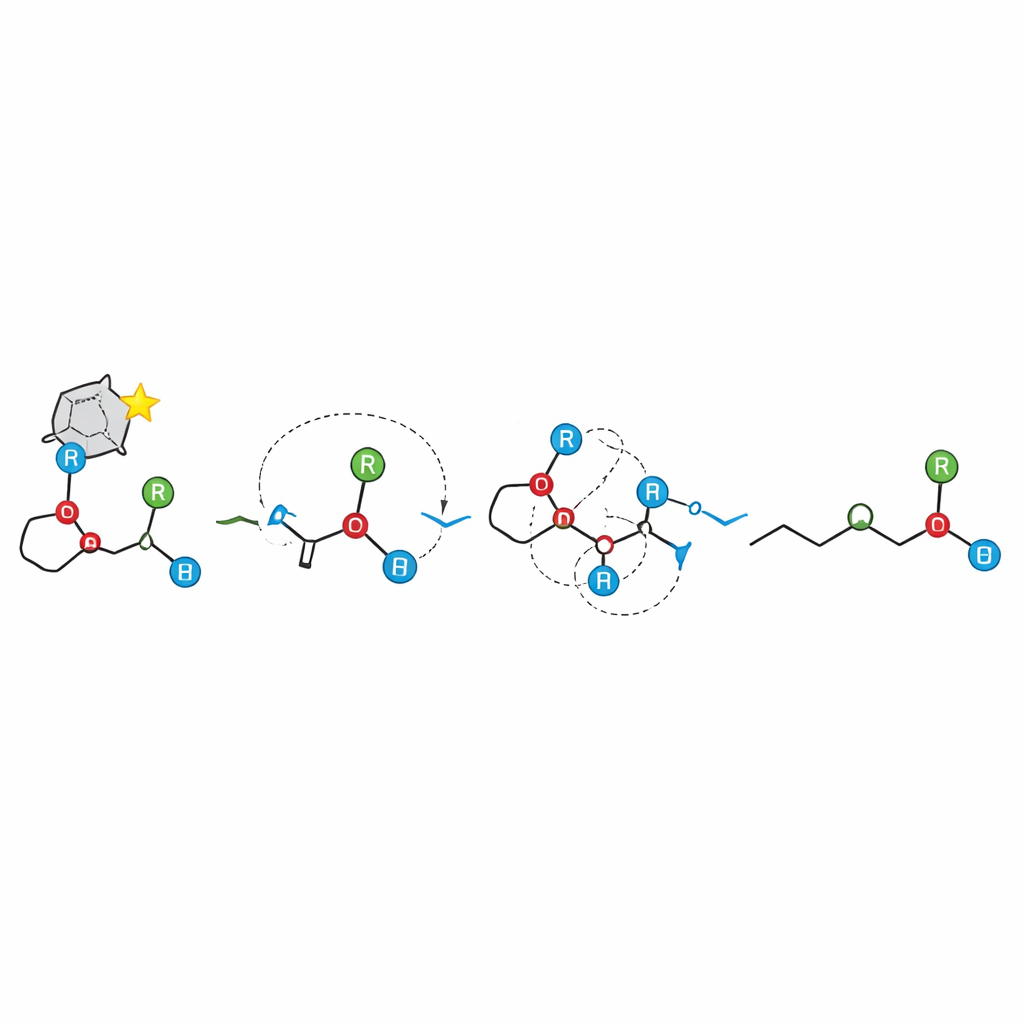
キラル分子合成への示唆
実用的な観点から、この研究は容易に入手できるアリルエーテルからキラル第三級アルコールを作るための堅牢な新ツールを有機合成化学者に提供するとともに、どの構造修飾が反応を助けるか阻害するかを示しています。より広くは、反応が荷電断片を経る場合でも、それらの断片が密接に結びついたままであれば立体化学情報は驚くほど忠実に伝達され得ることを実証しています。ラジカル基盤の見方を覆し、高選択性のイオン性カスケードを示した本研究は、他の複雑な結合再配置反応を見直し、再設計して精密な3次元制御を達成する道を開きます。
引用: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
キーワード: 不斉触媒, シグマトロピック転位, キラル第三級アルコール, 反応機構, 有機合成