Clear Sky Science · nl
De katalytische enantioselectieve [1,2]-Wittig-rearrangementcascade van allylethers
Moleculaire rommel omzetten in orde
Chemici willen vaak moleculen bouwen die spiegelbeeldselectief zijn, omdat ons lichaam onderscheid kan maken tussen de "linkshandige" en "rechtshandige" versies. Dit artikel pakt een langlopend raadsel in dat gebied aan: hoe stuur je een berucht onvoorspelbaar type bindingverplaatsende reactie zo dat deze voornamelijk één spiegelbeeld oplevert in plaats van een willekeurige mix. De auteurs vinden niet alleen een manier om dit te doen, ze tonen ook aan dat de reactie via een onverwachte route verloopt die decennia aan tekstboekdenken omverwerpt.
Waarom deze vormveranderingen ertoe doen
Veel krachtige reacties in de organische chemie werken door bindingen binnen een molecule geruisloos te verschuiven in plaats van alles af te breken en opnieuw te beginnen. Deze "rearrangementen" zijn gewaardeerd omdat ze weinig materiaal verspillen en complexe structuren in slechts één stap kunnen opbouwen. Tot deze groep behoren Wittig-rearrangementen die eenvoudige ethergroepen in waardevolle alcoholen kunnen omzetten. Een specifieke variant, het zogenaamde [1,2]-Wittig-rearrangement van allylethers, is echter moeilijk te beheersen: het geeft doorgaans mengsels van producten en heeft bovendien de neiging de driedimensionale rangschikking van atomen door elkaar te halen in plaats van één handig vorm te behouden of te creëren.
Een nieuw cascadepad
De onderzoekers laten zien dat deze lastige reactie getemd kan worden door haar onderdeel te maken van een tweestapscascade geleid door een speciaal ontworpen organische katalysator. Hun katalysator, een bifunctionele iminofosforaan, is zowel een uitzonderlijk sterke base als een precies "handig" omgeving. Eerst activeert hij een goedgedisciplineerde bindingsverschuiving bekend als een [2,3]-rearrangement, die een chirale tertiaire alcohol opbouwt met een zeer sterke voorkeur voor één spiegelbeeld. Daarna herverdeelt dit intermediair onder basische omstandigheden rustig opnieuw naar het uiteindelijke [1,2]-Wittig-product. Over veel verschillende uitgangsmaterialen levert de sequentie betrouwbaar chirale homoallylische alcoholen in goede opbrengsten en met hoge enantiomere verhoudingen, wat betekent dat één handige vorm sterk domineert.
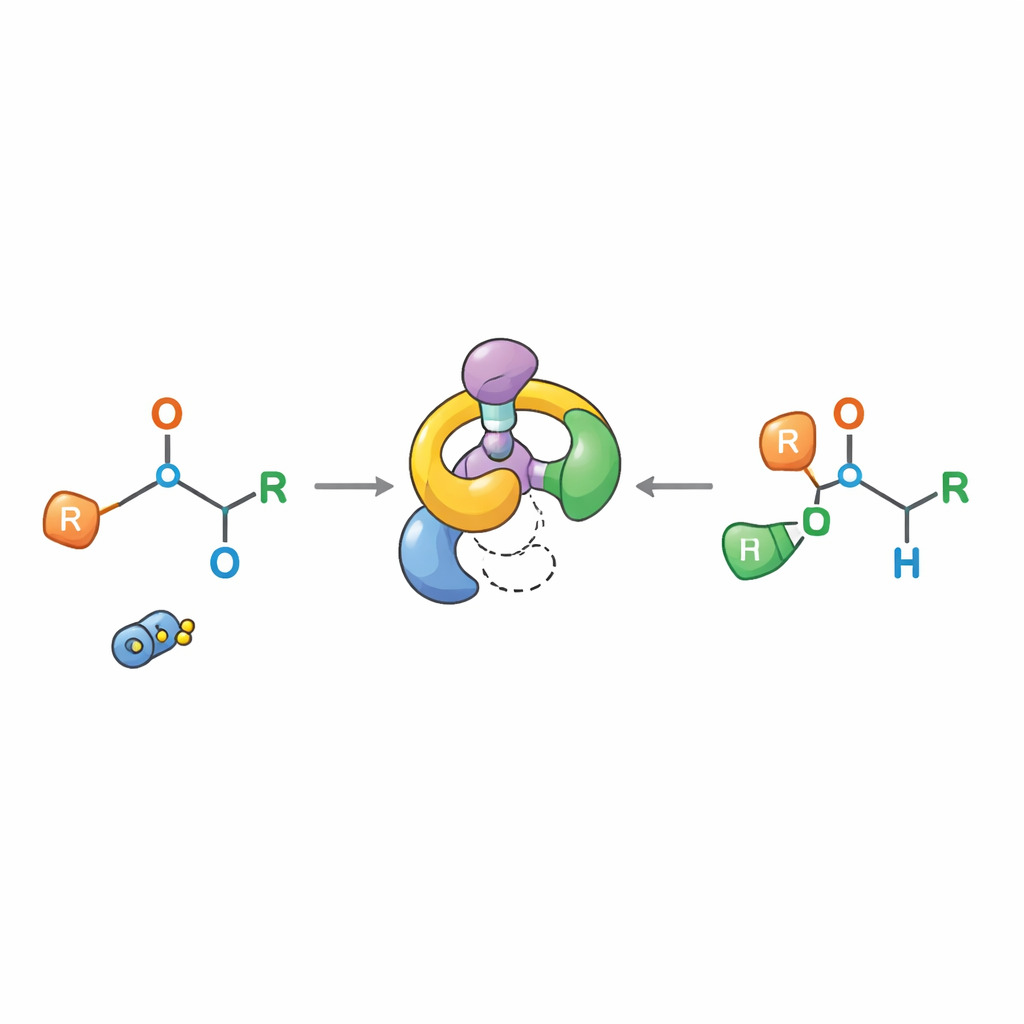
Onderzoeken hoe de reactie echt werkt
Klassieke verklaringen stelden dat [1,2]-Wittig-producten ontstonden door het verbreken van een binding om een losse paar radicalen te vormen die later weer recombineren, een beeld dat nauwkeurige stereochemische controle onwaarschijnlijk maakte. Het nieuwe werk schetst een ander beeld. Door zorgvuldig uitgevoerde experimenten — inclusief pogingen tot vangen met radicaalgevoelige additieven, "crossover"-testen die verschillende moleculen mengen, en gedetailleerde tijdsafhankelijke NMR-monitoring — tonen de auteurs aan dat de reactie verloopt via een specifiek [2,3]-gerearrangeerd intermediair en dat atomen gekoppeld blijven binnen één molecule in plaats van partners te wisselen. De tweede stap gedraagt zich als een formeel verboden [1,3]-rearrangement, maar in de praktijk ontvouwt het zich via fragmentatie naar een nauw geassocieerd ionenpaar dat op ordelijke wijze weer samensmelt en daarbij de configuratie van het chirale centrum behoudt.
Computers bevestigen de verborgen stappen
Om dit mechanistische beeld te onderbouwen, voerde het team uitgebreide quantumchemische berekeningen uit op realistische modellen van de katalysator en substraten. Deze berekeningen tonen waarom in de eerste stap één enantiomeer wordt bevoordeeld: de gevraagde overgangstoestand vormt een netwerk van drie sterke waterstofbruggen en een gunstige stapelingsinteractie tussen aromatische ringen, terwijl concurrerende orden lijden onder zwakkere interacties en sterische hinder. Voor de tweede stap vonden de berekeningen geen enkele vloeiende, concerted route; in plaats daarvan ondersteunen ze een stapsgewijze ionische fragmentatie met een bescheiden energiedrempel, gevolgd door vrijwel drempelvrije recombinatie. De voorspelde energiedrempel komt nauw overeen met die experimenteel gemeten, wat het geval voor het ionenpaarmechanisme versterkt.
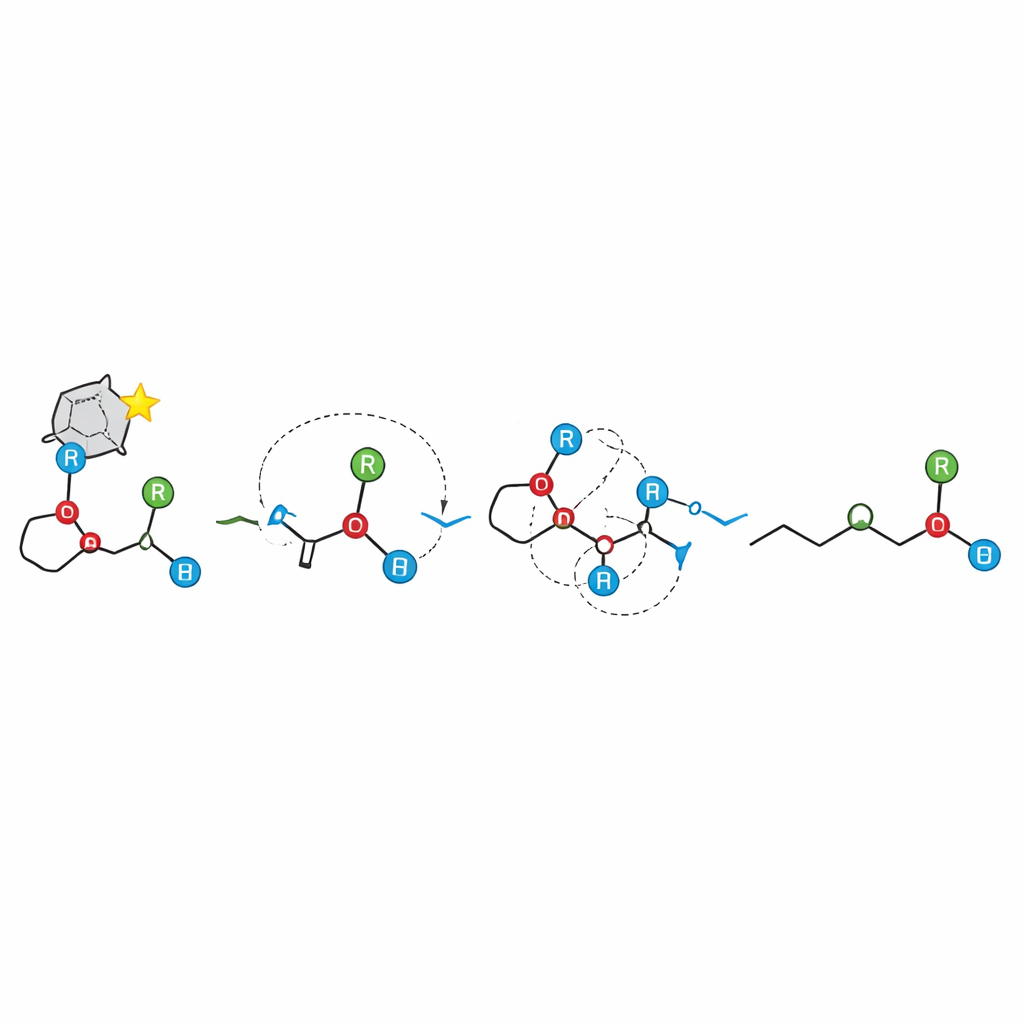
Gevolgen voor het bouwen van chirale moleculen
In praktische zin biedt dit werk synthetische chemici een robuust nieuw instrument om chirale tertiaire alcoholen te maken uit gemakkelijk verkrijgbare allylethers, en het kaart uit welke structurele aanpassingen het proces helpen of hinderen. Meer in het algemeen toont het aan dat zelfs wanneer een reactie via geladen fragmenten verloopt, stereochemische informatie met opmerkelijke getrouwheid kan worden doorgegeven, mits die fragmenten nauw geassocieerd blijven. Door de radicaalgebaseerde kijk op het [1,2]-Wittig-rearrangement omver te werpen en een zeer selectieve ionische cascade te demonstreren, opent de studie de deur om andere complexe bindingsrearrangerende reacties te heroverwegen en opnieuw te ontwerpen om precieze 3D-controle te bereiken.
Bronvermelding: Kang, T., O’Yang, J., Kasten, K. et al. The catalytic enantioselective [1,2]-Wittig rearrangement cascade of allylic ethers. Nat. Chem. 18, 800–809 (2026). https://doi.org/10.1038/s41557-025-02022-4
Trefwoorden: asymmetrische katalyse, sigmatropische rearrangement, chirale tertiaire alcoholen, reactiemechanisme, organische synthese