Clear Sky Science · zh
整合多组学与单细胞分析揭示由CDKN2A介导的铜死亡机制推动甲状腺癌进展
为什么铜与甲状腺癌重要
甲状腺癌通常可以治愈,但一小部分病人会出现肿瘤复发、转移或对标准疗法产生耐药。与此同时,研究人员发现了一种由金属铜触发的新型细胞死亡方式。本研究将这两条线索结合起来:探讨与铜相关的细胞死亡通路及其调控基因,如何塑造甲状腺肿瘤及其周围免疫细胞的行为。通过将大规模组学分析与单细胞和动物实验相结合,作者揭示了一个令人惊讶的基因网络,该网络似乎有助于甲状腺癌的生长和扩散——并可能为未来治疗提供新的靶点。 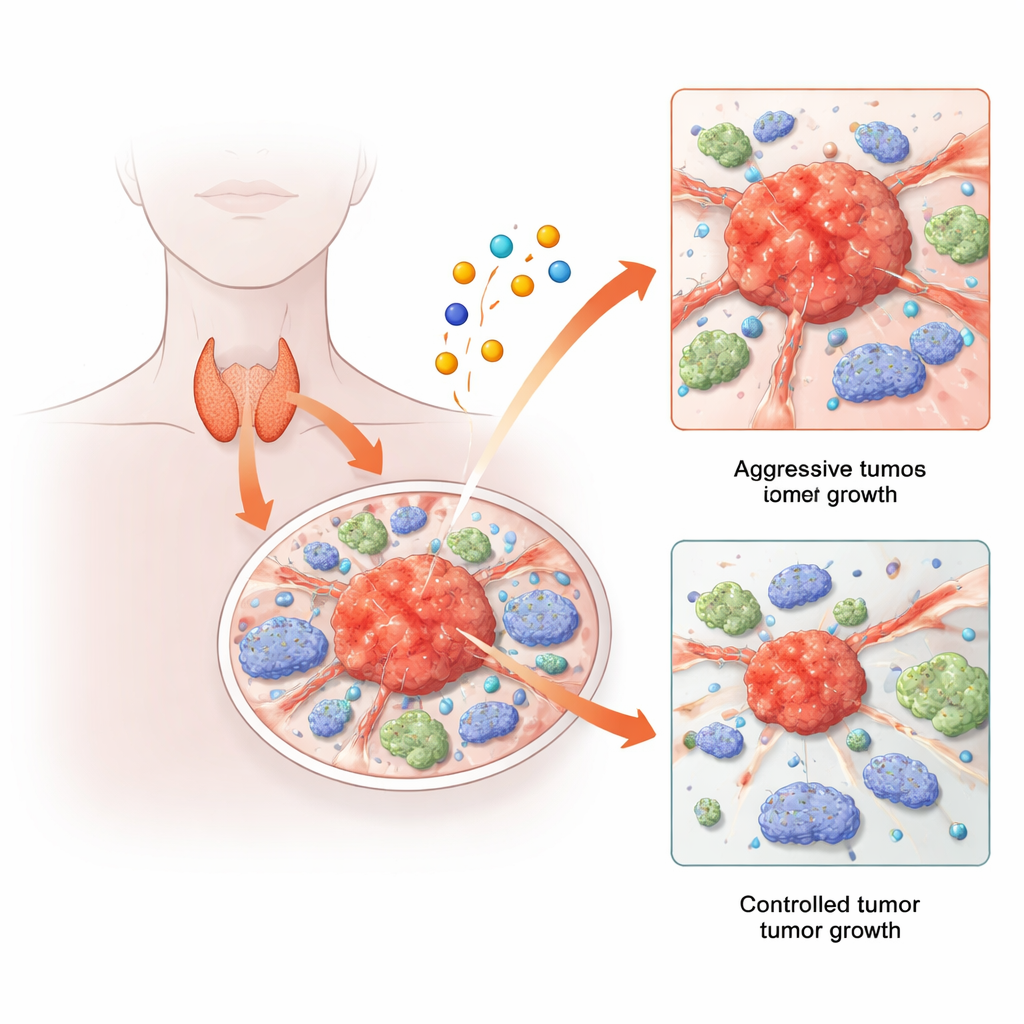
在大量患者中考察与铜相关的基因
研究者首先利用“多组学”数据集——来自数百名甲状腺癌患者的大规模遗传与分子测量数据。他们聚焦于19个已知参与铜触发细胞死亡的基因,比较这些基因在肿瘤与正常甲状腺组织中的表达差异。通过统计聚类分析,他们根据这些铜相关基因的活性将患者分为两种分子亚型。一类亚型表现出更强的免疫反应相关信号,而另一类更与代谢改变相关,即细胞的能量与合成机制。这些不同的模式表明,铜生物学可能不仅影响肿瘤细胞本身,还会改变肿瘤与机体免疫防御之间的相互作用。
免疫环境与患者预后
接着,团队考察了这些铜相关亚型与肿瘤微环境——肿瘤周围的免疫细胞与支持组织混合体——的关联。他们发现,一类亚型具有更高的免疫“检查点”分子表达,这些分子是现代免疫治疗药物的重要靶点,并伴有更多类型免疫细胞的浸润。他们还基于铜相关基因构建了一个风险评分,可以区分预后更好与更差的患者。高评分患者总生存期较短,并且肿瘤中的免疫细胞构成不同,包括抗癌的T细胞数量较少。这提示铜相关通路可能影响免疫系统识别和攻击甲状腺肿瘤的能力。
锁定一个关键的促病基因
在这19个铜相关基因中,有一个基因格外突出:CDKN2A。与大多数在肿瘤中下调的基因不同,CDKN2A在甲状腺癌中持续升高,并且与更差的预后密切相关。单细胞测序——一种在数千个单独细胞中读取基因活性的技术——显示CDKN2A在甲状腺肿瘤细胞以及某些免疫与支持细胞中尤为活跃。在体外和小鼠实验中,增强甲状腺癌细胞中的CDKN2A使其在培养皿和动物体内表现出更强的生长、侵袭与迁移能力。抑制CDKN2A则产生相反效果,缩小肿瘤并减少肺转移。这些发现令人瞩目,因为CDKN2A在许多癌症中传统上被视为抑制细胞增殖的“刹车”;在甲状腺这个背景下,它似乎更像是加速器。
促进肿瘤生长的隐秘RNA回路
为了解CDKN2A为何异常活跃,作者寻找其上游调控回路。他们发现了一个由三部分RNA组成的网络,包括长链非编码RNA GAS5、一个小型调控RNA miR-128-3p,以及CDKN2A基因。本质上,GAS5充当“海绵”结合miR-128-3p,阻止该小RNA附着并抑制CDKN2A。当GAS5水平升高时,miR-128-3p被耗竭,CDKN2A失去抑制,癌细胞变得更具侵袭性;当GAS5被敲低时,miR-128-3p回升,CDKN2A水平下降,肿瘤细胞的增殖和转移能力显著减弱。 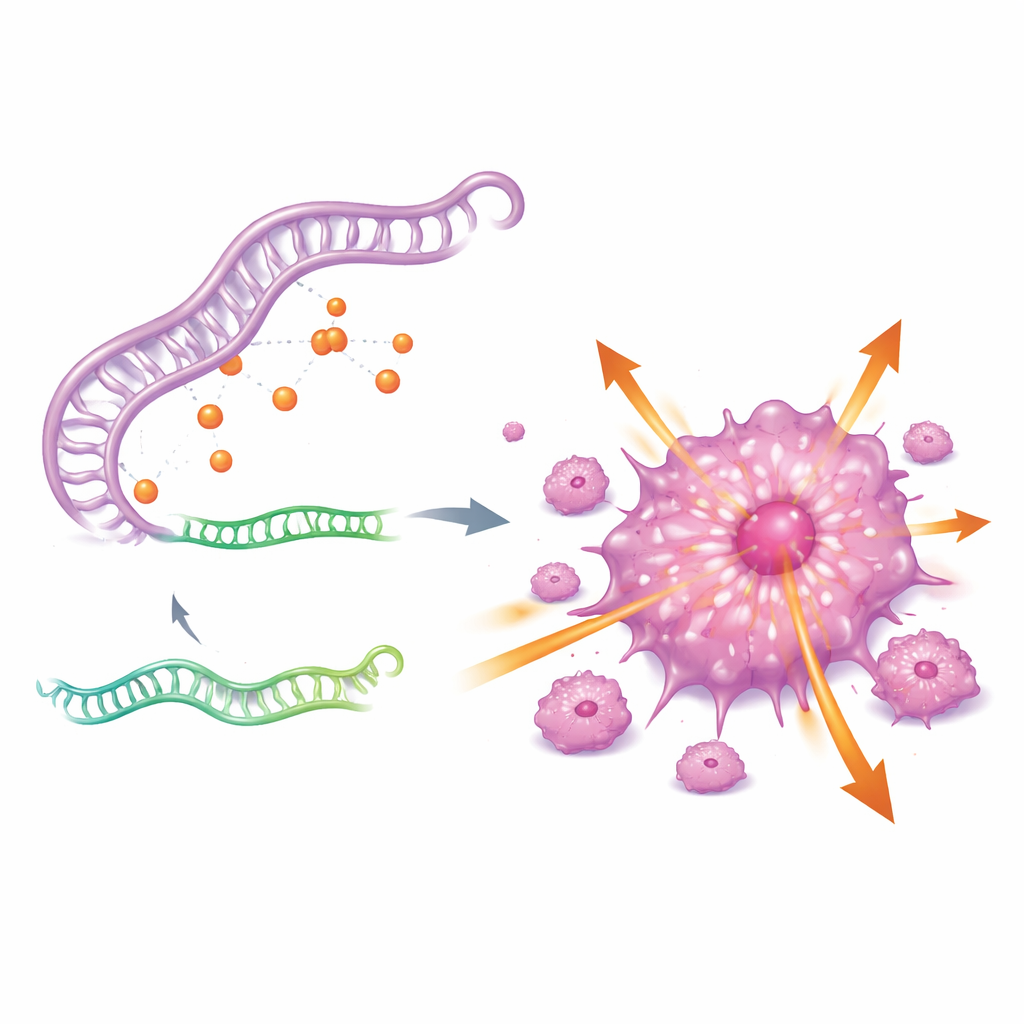
这对未来临床意味着什么
这项工作描绘了一个系统层面的图景,展示了铜相关细胞死亡通路、甲状腺肿瘤细胞与周围免疫细胞如何相互交织。尽管该研究尚未直接证明铜触发的细胞死亡就是推动甲状腺癌的因果因素,但它清楚地表明铜相关基因——尤其是GAS5/miR-128-3p/CDKN2A网络——与更具危险性的疾病相关。对患者而言,这最终可能转化为新的血液或组织检测手段以更好评估风险,或开发出破坏该RNA回路或调节铜相关过程的新药物,从而将状态从促癌转向抑癌。
引用: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
关键词: 甲状腺癌, 铜死亡, 肿瘤微环境, CDKN2A, 非编码RNA