Clear Sky Science · tr
Entegre çoklu-omikler ve tek hücreli analiz, tiroid karsinomunun ilerlemesini yönlendiren CDKN2A aracılı cuproptozis mekanizmalarını ortaya koyuyor
Neden Bakır ve Tiroid Kanseri Önemli?
Tiroid kanseri genellikle tedavi edilebilir olsa da, hastaların küçük bir bölümünde tümörler nüksedebilir, yayılabilir veya standart tedavilere direnç gösterebilir. Aynı zamanda araştırmacılar, bakır metalinin tetiklediği yeni bir hücre ölümü yolunu keşfettiler. Bu çalışma, bu iki hikâyeyi bir araya getiriyor: bakırla bağlantılı hücre ölümü yollarının ve bunları kontrol eden genlerin tiroid tümörlerinin ve çevresindeki immün hücrelerin davranışını nasıl şekillendirdiğini inceliyor. Büyük veri analizlerini tek hücreli ve hayvan deneyleriyle birleştirerek, tiroid kanserinin büyümesine ve yayılmasına yardımcı olduğu görünen ve gelecekteki tedaviler için yeni hedefler sunabilecek şaşırtıcı bir gen ağı ortaya çıkarıyor. 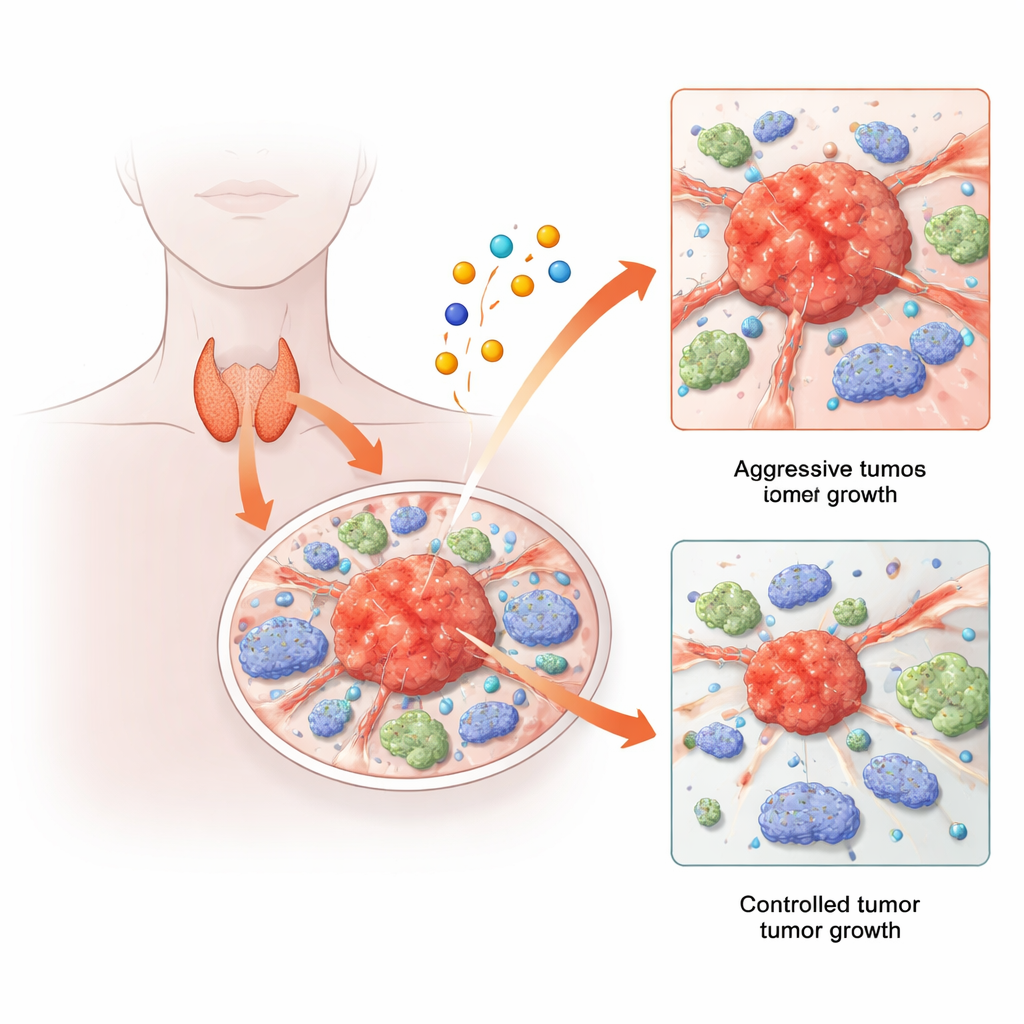
Birçok Hastada Bakırla İlişkili Genleri İncelemek
Araştırmacılar, yüzlerce tiroid kanseri hastasından elde edilen genetik ve moleküler ölçümlerin büyük koleksiyonları olan “çoklu-omik” veri setleriyle başladılar. Bakır tetiklemesinin rol oynadığı bilinen 19 gene odaklandılar ve bu genlerin tümörlerde normal tiroid dokusuna kıyasla nasıl davrandığını sorguladılar. İstatistiksel kümeleme kullanarak, bu bakırla ilişkili genlerin aktivitesine göre hastaları iki moleküler alt tipe ayırdılar. Bir alt tip immün yanıtlara ilişkin daha güçlü sinyaller gösterirken, diğeri hücrenin enerji ve yapı taşı mekanizmalarını kapsayan metabolik değişikliklerle daha çok ilişkiliydi. Bu farklı desenler, bakır biyolojisinin yalnızca tümör hücrelerini değil, aynı zamanda tümörlerin vücudun savunma mekanizmalarıyla etkileşimini de etkileyebileceğini düşündürdü.
İmmün Çevre ve Hastalık Seyri
Takım daha sonra bu bakırla ilişkili alt tiplerin tümör mikroçevresi—kanserin etrafındaki immün hücreler ve destekleyici doku karışımı—ile nasıl ilişkilendiğini inceledi. Bir alt tipin immün “kontrol noktası” moleküllerinin daha yüksek ekspresyonuna sahip olduğunu ve birçok immün hücre türünün daha yoğun infiltrasyonunu gösterdiğini buldular; bu moleküller modern immünoterapi ilaçlarının ana hedefleridir. Ayrıca, bakırla ilişkili genlere dayalı bir risk skoru oluşturarak hastaları daha iyi veya daha kötü sağkalım gösteren gruplara ayırdılar. Yüksek skora sahip hastalar genellikle daha kısa genel sağkalım gösterdi ve tümörlerinde daha az kanserle savaşan T hücresi de dahil olmak üzere farklı bir immün hücre dengesi vardı. Bu, bakırla ilişkili yolların immün sistemin tiroid tümörlerini tanıma ve saldırma kapasitesini etkileyebileceğini öne sürüyor.
Önemli Bir Sorun Yaratıcı Gene Odaklanmak
19 bakırla ilişkili gen arasında öne çıkan bir gen vardı: CDKN2A. Diğerlerinin çoğunun tümörlerde azaldığı yerde, CDKN2A tiroid kanserinde tutarlı şekilde yükselmişti ve kötü sonuçlarla güçlü şekilde ilişkiliydi. Tek hücre dizilemesi—binlerce bireysel hücrede gen aktivitesini gösteren bir yöntem—CDKN2A’nın özellikle tiroid tümör hücrelerinde ve belirli immün ve destek hücrelerinde aktif olduğunu gösterdi. Laboratuvar deneylerinde, tiroid kanseri hücrelerinde CDKN2A’yı artırmak, bu hücrelerin hem besiyerlerinde hem de fare modellerinde daha agresif biçimde büyümesine, invade olmasına ve göç etmesine yol açtı. CDKN2A’nın susturulması ters etki yaratarak tümörleri küçülttü ve akciğer metastazlarını azalttı. Bu bulgular dikkat çekicidir çünkü CDKN2A birçok kanser bağlamında klasik olarak hücre bölünmesini frenleyen bir “fren” olarak görülür; burada ise en azından tiroid ortamında bir gaz pedalına benzer davranıyor gibi görünüyor.
Tümör Büyümesini Besleyen Gizli Bir RNA Devresi
CDKN2A’nın neden bu kadar aktif olduğunu anlamak için yazarlar yukarı yönlü bir düzenleyici devre aradılar. Uzun kodlamayan RNA olan GAS5, küçük düzenleyici RNA miR-128-3p ve CDKN2A genini içeren üç parçalı bir RNA ağı keşfettiler. Özetle, GAS5 miR-128-3p’yi bağlayan bir sünger görevi görerek bu küçük RNA’nın CDKN2A’ya bağlanıp onu baskılamasını engelliyor. GAS5 düzeyleri yüksek olduğunda miR-128-3p tutularak etkisiz hale geliyor, CDKN2A kontrol dışı kalıyor ve kanser hücreleri daha agresif hale geliyor. GAS5 baskılanınca miR-128-3p geri geliyor, CDKN2A seviyeleri düşüyor ve tümör hücreleri büyüme ve yayılma yeteneklerinin büyük bir kısmını kaybediyor. 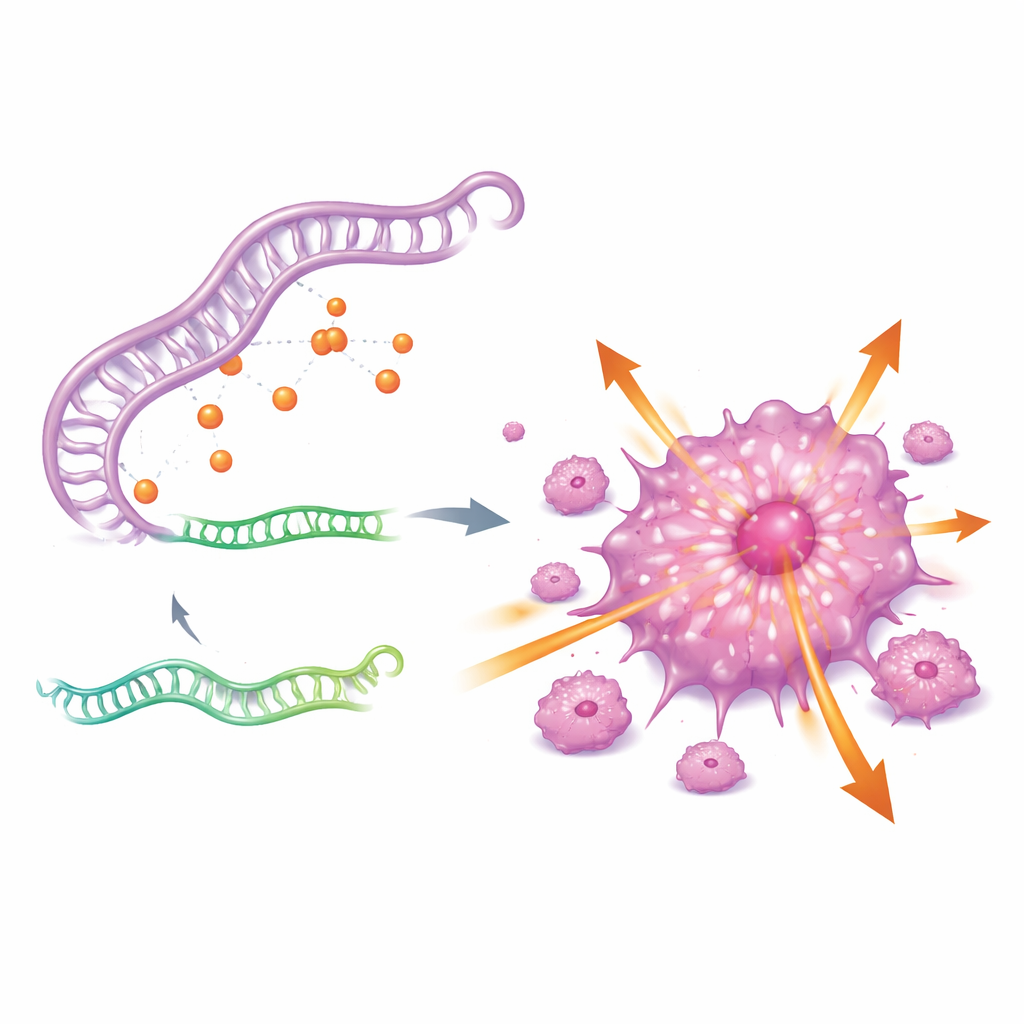
Gelecek Tedavi İçin Ne Anlama Geliyor?
Bu çalışma, bakırla bağlantılı bir hücre ölümü yolunun, tiroid tümör hücrelerinin ve çevrelerindeki immün hücrelerin nasıl iç içe geçtiğine dair sistem düzeyinde bir resim çiziyor. Çalışma henüz bakır tetikli hücre ölümünün doğrudan tiroid kanserini tetiklediğini kanıtlamasa da, bakırla ilişkili genlerin—özellikle GAS5/miR-128-3p/CDKN2A ağının—daha tehlikeli hastalıkla bağlantılı olduğunu açıkça gösteriyor. Hastalar için bu, nihayetinde riski daha iyi değerlendirebilecek yeni kan veya doku testlerine ve bu RNA devresini bozacak ya da bakırla ilişkili süreçleri modüle ederek dengeyi tümör büyümesi lehine değil tümör kontrolü lehine çevirebilecek yeni ilaçlara yol açabilir.
Atıf: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Anahtar kelimeler: tiroid kanseri, cuproptozis, tümör mikroçevresi, CDKN2A, kodlamayan RNA