Clear Sky Science · ar
التحليل المتكامل متعدد الأوميك والخلايا المفردة يكشف آليات الموت المرتبطة بـ CDKN2A والمدفوعة بالنحاس التي تسهم في تطور سرطان الغدة الدرقية
لماذا يهم النحاس وسرطان الغدة الدرقية
عادة ما يكون سرطان الغدة الدرقية قابلاً للعلاج، لكن شريحة مقلقة من المرضى تطور أوراماً تعود، أو تنتشر، أو تقاوم العلاجات القياسية. في الوقت نفسه، اكتشف الباحثون وسيلة جديدة لموت الخلايا تحفزها فلزات النحاس. تجمَع هذه الدراسة هذين الخطين من البحث: فهي تستقصي كيف تشكل مسارات موت الخلايا المرتبطة بالنحاس والجينات التي تتحكم بها سلوك أورام الغدة الدرقية والخلايا المناعية المحيطة بها. من خلال دمج تحليل البيانات الضخمة مع تجارب الخلايا المفردة والنماذج الحيوانية، يكشف المؤلفون عن شبكة جينية مفاجئة تبدو أنها تساعد سرطان الغدة الدرقية على النمو والانتشار — وقد تقدم أهدافاً جديدة للعلاجات المستقبلية. 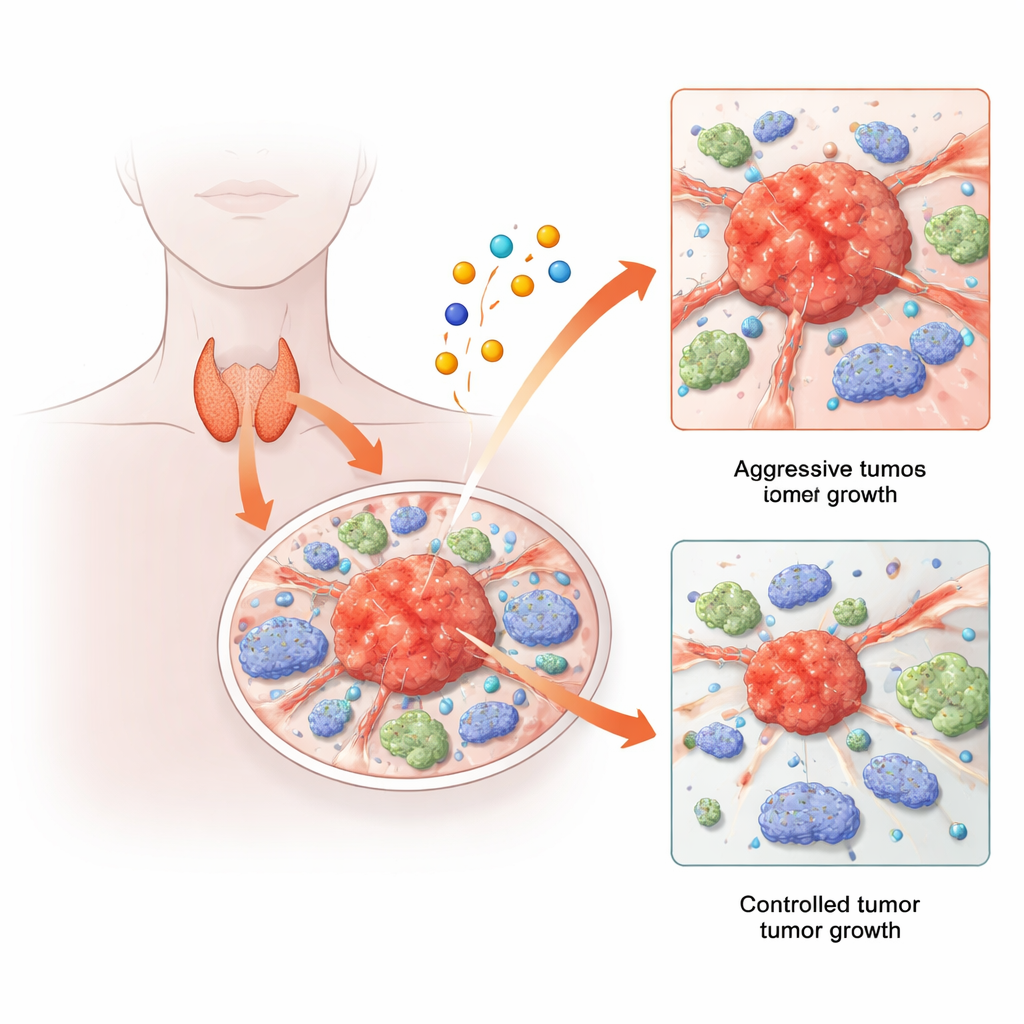
مراجعة الجينات المرتبطة بالنحاس عبر العديد من المرضى
بدأ الباحثون بمجموعات بيانات «متعددة الأوميك» — مجموعات كبيرة من القياسات الجينية والجزيئية — مأخوذة من مئات مرضى سرطان الغدة الدرقية. ركزوا على 19 جيناً معروفةً بأنها تشارك في موت الخلايا المحفَّز بالنحاس، ودرسوا سلوك هذه الجينات في الأورام مقارنةً بالنسيج الدرقي الطبيعي. باستخدام التجميع الإحصائي، صنّفوا المرضى إلى نوعين جزيئيين بناءً على نشاط هذه الجينات المرتبطة بالنحاس. أظهر أحد النوعين إشارات أقوى مرتبطة بالاستجابات المناعية، بينما ارتبط الآخر بتغيرات في الأيض، أي آليات الطاقة والمكوّنات الخلوية. أشارت هذه الأنماط المميزة إلى أن بيولوجيا النحاس قد تؤثر ليس فقط في خلايا الورم نفسها، بل أيضاً في كيفية تفاعل الأورام مع دفاعات الجسم.
البيئة المناعية المحيطة وتوقعات المرضى
بعد ذلك، فحص الفريق كيف ترتبط هذه الأنواع المرتبطة بالنحاس بالبيئة الميكروية للورم — مزيج الخلايا المناعية والأنسجة الداعمة حول السرطان. وجدوا أن أحد الأنواع أظهر تعبيراً أعلى لجزيئات «نقاط التفتيش» المناعية، وهي أهداف رئيسية لأدوية المناعة الحديثة، ووجود تسلل أكبر لأنواع متعددة من الخلايا المناعية. كما أنشأوا درجة مخاطرة مبنية على الجينات المرتبطة بالنحاس قادرة على تمييز المرضى ذوي البقاء الأفضل مقابل الأسوأ. المرضى ذوو الدرجات العالية مالوا إلى قصر البقاء الكلي وتوازن مختلف للخلايا المناعية في أورامهم، بما في ذلك عدد أقل من خلايا T المناعية المحاربة للسرطان. يقترح ذلك أن المسارات المرتبطة بالنحاس قد تؤثر في قدرة الجهاز المناعي على التعرف على أورام الغدة الدرقية ومهاجمتها.
التركيز على جين مفتعل للمشاكل
من بين الجينات الـ19 المرتبطة بالنحاس، برز جين واحد: CDKN2A. بخلاف معظم الجينات الأخرى التي انخفضت في الأورام، كان CDKN2A مرتفع التعبير باستمرار في سرطان الغدة الدرقية وارتبط بقوة بنتائج أسوأ. أظهر التسلسل الخلوي المفرد — الأسلوب الذي يقرأ نشاط الجينات في آلاف الخلايا الفردية — أن CDKN2A ينشط بشكل خاص في خلايا أورام الغدة الدرقية وبعض الخلايا المناعية والخلايا الداعمة. في تجارب مخبرية، أدى تعزيز تعبير CDKN2A في خلايا سرطان الغدة الدرقية إلى نموها وغزوها وهجرتها بشكل أعنف، سواء في الأطباق أو في الفئران. أما إسكات CDKN2A فكان له التأثير المعاكس، حيث قلّص الأورام وخفّض النقائل الرئوية. هذه النتائج لافتة لأن CDKN2A يُنظر إليه تقليدياً كبذرة توقف لتقسّم الخلايا في سرطانات عديدة؛ هنا يبدو أنه يتصرف أكثر كمسَرِّع، على الأقل في سياق الغدة الدرقية.
دائرة RNA خفيّة تغذي نمو الورم
لفهم سبب نشاط CDKN2A بهذا الشكل، بحث المؤلفون عن دائرة تنظيمية صاعدة. كشفوا عن شبكة RNA ثلاثية الأجزاء تتضمن حمضاً نووياً ريبياً طويل غير مشفر يُسمى GAS5، ورنا صغيراً تنظيمياً يُدعى miR-128-3p، وجين CDKN2A. جوهرياً، يعمل GAS5 كإسفنجة تربط miR-128-3p، مانعةً هذا الرنا الصغير من الالتحام بـ CDKN2A وكبحه. عندما تكون مستويات GAS5 مرتفعة، يُحتجز miR-128-3p، ويهرب CDKN2A من السيطرة، فتتصاعد عدائية الخلايا السرطانية. أما عند تثبيط GAS5، فينتعش miR-128-3p، وتنخفض مستويات CDKN2A، وتفقد خلايا الورم جزءاً كبيراً من قدرتها على النمو والانتشار. 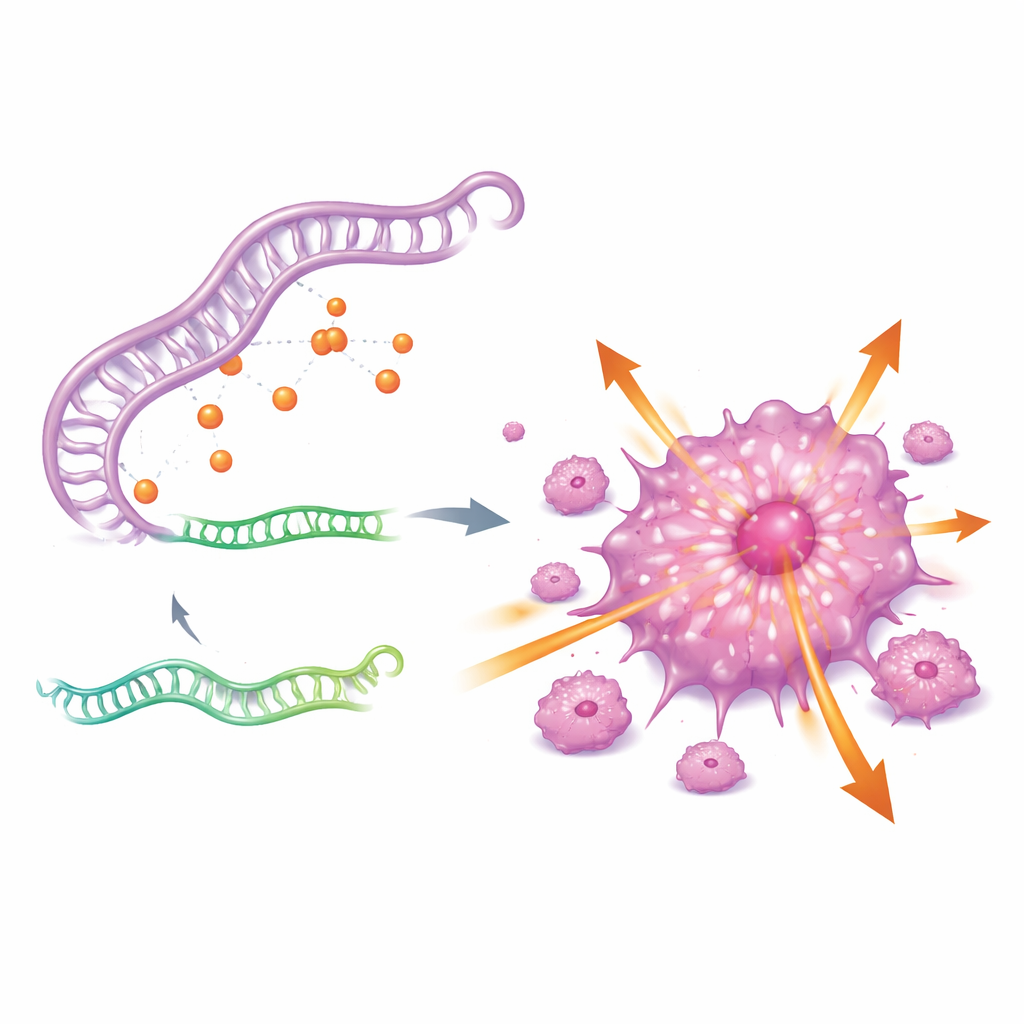
ماذا يعني هذا للرعاية المستقبلية
تقدّم هذه الدراسة صورة نظامية لكيف يرتبط مسار موت الخلايا المرتبط بالنحاس بخلايا أورام الغدة الدرقية والخلايا المناعية المحيطة بها. وبينما لا تثبت الدراسة بعد أن موت الخلايا المحفَّز بالنحاس هو سبب مباشر لتقدّم سرطان الغدة الدرقية، فإنها تُظهر بوضوح أن الجينات المرتبطة بالنحاس — وخصوصاً شبكة GAS5/miR-128-3p/CDKN2A — مرتبطة بمرض أخطر. بالنسبة للمرضى، قد يترجم ذلك مستقبلاً إلى اختبارات دم أو نسيجية أفضل لتقدير المخاطر، وإلى أدوية جديدة تعطل هذه الدائرة الريبية أو تعدّل العمليات المرتبطة بالنحاس لتحوّط التوازن بعيداً عن نمو الورم ونحو السيطرة عليه.
الاستشهاد: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
الكلمات المفتاحية: سرطان الغدة الدرقية, الموت بالخلايا المرتبط بالنحاس (cuproptosis), البيئة الميكروية للورم, CDKN2A, الحمض النووي الريبي غير المشفر