Clear Sky Science · it
Analisi integrata multi-omica e single-cell rivela meccanismi di cuproptosi mediati da CDKN2A che guidano la progressione del carcinoma tiroideo
Perché rame e cancro della tiroide sono importanti
Il cancro della tiroide è di solito trattabile, ma una minoranza preoccupante di pazienti sviluppa tumori che recidivano, si diffondono o resistono alle terapie standard. Allo stesso tempo, i ricercatori hanno scoperto un nuovo modo in cui le cellule possono morire, innescato dal metallo rame. Questo studio unisce queste due storie: esplora come le vie di morte cellulare legate al rame e i geni che le regolano plasmano il comportamento dei tumori tiroidei e delle cellule immunitarie circostanti. Combinando analisi su larga scala con esperimenti su singola cellula e su modelli animali, gli autori rivelano una rete genica sorprendente che sembra favorire la crescita e la diffusione del cancro tiroideo—and potrebbe offrire nuovi bersagli per trattamenti futuri. 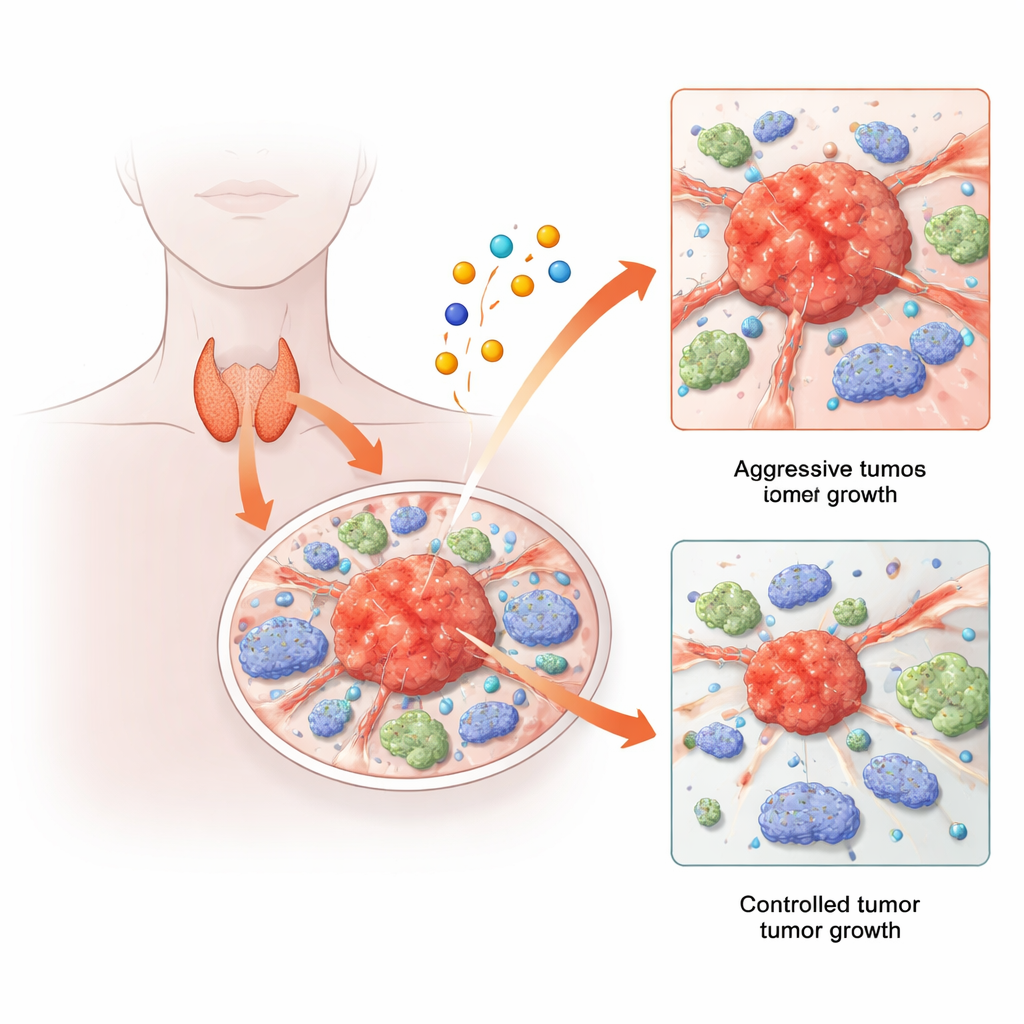
Analisi dei geni legati al rame in molti pazienti
I ricercatori hanno iniziato con dataset “multi-omici”—ampie raccolte di misurazioni genetiche e molecolari—provenienti da centinaia di pazienti con cancro della tiroide. Si sono concentrati su 19 geni noti per essere coinvolti nella morte cellulare indotta dal rame e hanno esaminato come questi geni si comportassero nei tumori rispetto al tessuto tiroideo normale. Utilizzando tecniche statistiche di clustering, hanno raggruppato i pazienti in due sottotipi molecolari basati sull’attività di questi geni correlati al rame. Un sottotipo mostrava segnali più forti legati alle risposte immunitarie, mentre l’altro era più associato a cambiamenti nel metabolismo, la macchina energetica e dei mattoni cellulari. Questi schemi distinti suggerivano che la biologia del rame potrebbe influenzare non solo le cellule tumorali, ma anche il modo in cui i tumori interagiscono con le difese dell’organismo.
Microambiente immunitario e prospettiva dei pazienti
Successivamente, il gruppo ha esaminato come questi sottotipi correlati al rame fossero collegati al microambiente tumorale—la miscela di cellule immunitarie e tessuto di supporto attorno al tumore. Hanno riscontrato che un sottotipo presentava una maggiore espressione di molecole di “checkpoint” immunitario, bersagli chiave dei farmaci immunoterapici moderni, e una maggiore infiltrazione da parte di molti tipi di cellule immunitarie. Hanno inoltre costruito un punteggio di rischio basato su geni associati al rame in grado di separare i pazienti con una sopravvivenza migliore da quelli con una peggiore. I pazienti con punteggi elevati tendevano ad avere una sopravvivenza globale più breve e un diverso equilibrio di cellule immunitarie nei loro tumori, incluse meno cellule T antitumorali. Ciò suggerisce che le vie legate al rame potrebbero influenzare l’efficacia con cui il sistema immunitario riconosce e attacca i tumori tiroidei.
Individuazione di un gene chiave problematico
Tra i 19 geni correlati al rame, uno è emerso in modo particolare: CDKN2A. A differenza della maggior parte degli altri, ridotti nei tumori, CDKN2A risultava costantemente elevato nel cancro della tiroide ed era fortemente associato a esiti peggiori. Il sequenziamento a singola cellula—un approccio che legge l’attività genica in migliaia di singole cellule—ha mostrato che CDKN2A è particolarmente attivo nelle cellule tumorali tiroidee e in certe cellule immunitarie e di supporto. In esperimenti di laboratorio, l’aumento di CDKN2A nelle cellule del cancro tiroideo ne ha potenziato la crescita, l’invasività e la migrazione, sia in colture che in modelli murini. Il silenziamento di CDKN2A ha avuto l’effetto opposto, riducendo i tumori e diminuendo le metastasi polmonari. Questi risultati sono sorprendenti perché CDKN2A è classicamente visto come un “freno” sulla divisione cellulare in molti tumori; in questo contesto tiroideo sembra invece comportarsi più come un acceleratore.
Un circuito di RNA nascosto che alimenta la crescita tumorale
Per capire perché CDKN2A sia così attivo, gli autori hanno cercato un circuito regolatorio a monte. Hanno identificato una rete a tre componenti di RNA che coinvolge una lncRNA (RNA lungo non codificante) chiamata GAS5, un piccolo RNA regolatorio chiamato miR-128-3p e il gene CDKN2A. In sostanza, GAS5 agisce come una spugna che lega miR-128-3p, impedendo a questo piccolo RNA di attaccarsi a CDKN2A e di attenuarne l’espressione. Quando i livelli di GAS5 sono alti, miR-128-3p è sequestrato, CDKN2A sfugge al controllo e le cellule tumorali diventano più aggressive. Quando GAS5 viene silenziata, miR-128-3p recupera la sua funzione, i livelli di CDKN2A scendono e le cellule tumorali perdono gran parte della loro capacità di crescere e diffondersi. 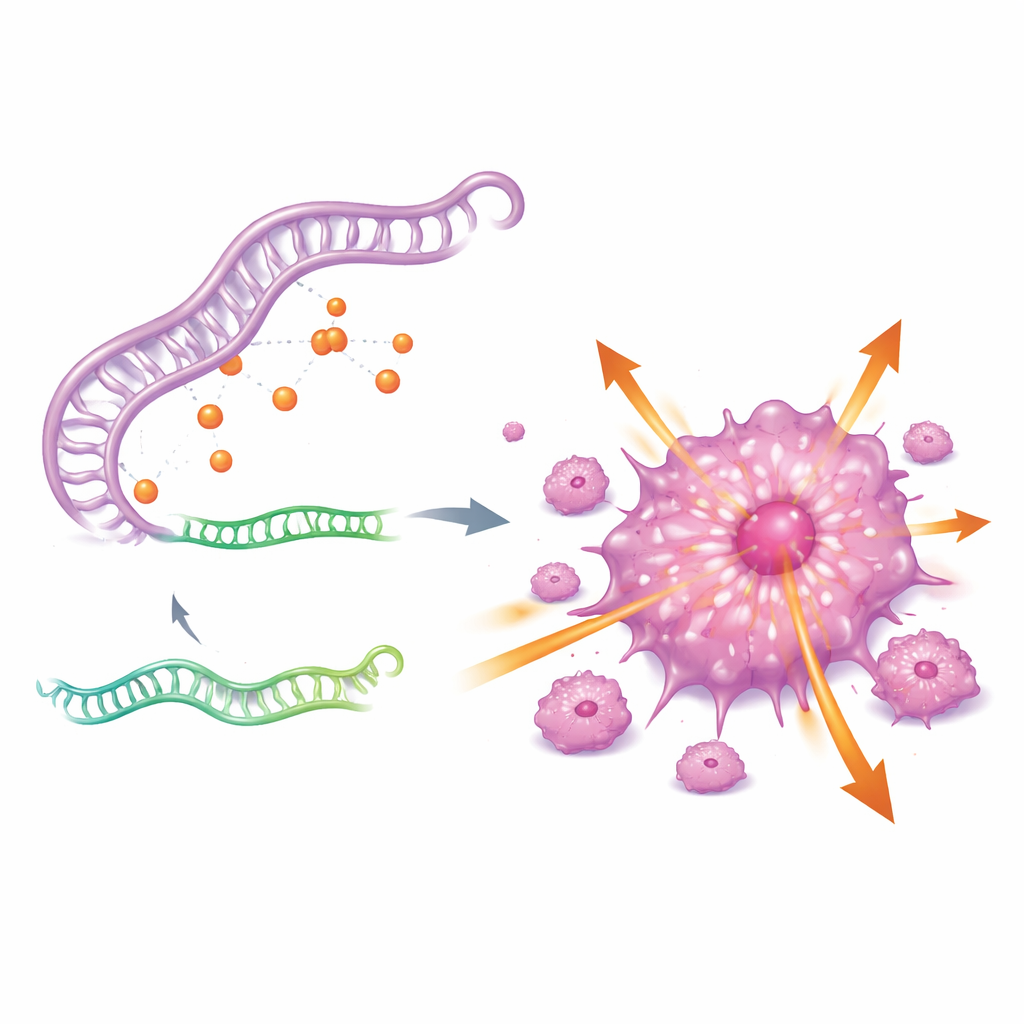
Cosa significa per le cure future
Questo lavoro dipinge un quadro a livello di sistema di come una via di morte cellulare legata al rame, le cellule tumorali tiroidee e le cellule immunitarie circostanti siano intrecciate. Pur non dimostrando ancora che la cuproptosi stia direttamente guidando il cancro della tiroide, lo studio mostra chiaramente che i geni correlati al rame—e in particolare la rete GAS5/miR-128-3p/CDKN2A—sono associati a una malattia più pericolosa. Per i pazienti, ciò potrebbe tradursi in futuro in nuovi test su sangue o tessuto per valutare meglio il rischio, e in nuovi farmaci che interrompono questo circuito di RNA o modulano i processi legati al rame per spostare l’equilibrio lontano dalla crescita tumorale e verso il controllo del tumore.
Citazione: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Parole chiave: cancro della tiroide, cuproptosi, microambiente tumorale, CDKN2A, RNA non codificante