Clear Sky Science · ru
Интегрированный мультиомный и одно-клеточный анализ выявляет механизмы купроптоза, опосредованные CDKN2A, приводящие к прогрессированию рака щитовидной железы
Почему медь и рак щитовидной железы важны
Рак щитовидной железы обычно поддаётся лечению, но у небольшого, но тревожного числа пациентов развиваются опухоли, которые рецидивируют, метастазируют или устойчивы к стандартной терапии. Одновременно исследователи обнаружили новый путь гибели клеток, запускаемый металлом медью. В этом исследовании эти две истории объединены: авторы изучают, как меди-связанные пути гибели клеток и гены, их регулирующие, формируют поведение опухолей щитовидной железы и окружающих иммунных клеток. Комбинируя анализ больших данных с одно-клеточными и животными экспериментами, они раскрывают неожиданный генетический каскад, который, по-видимому, способствует росту и распространению рака щитовидной железы — и может предложить новые мишени для будущих терапий. 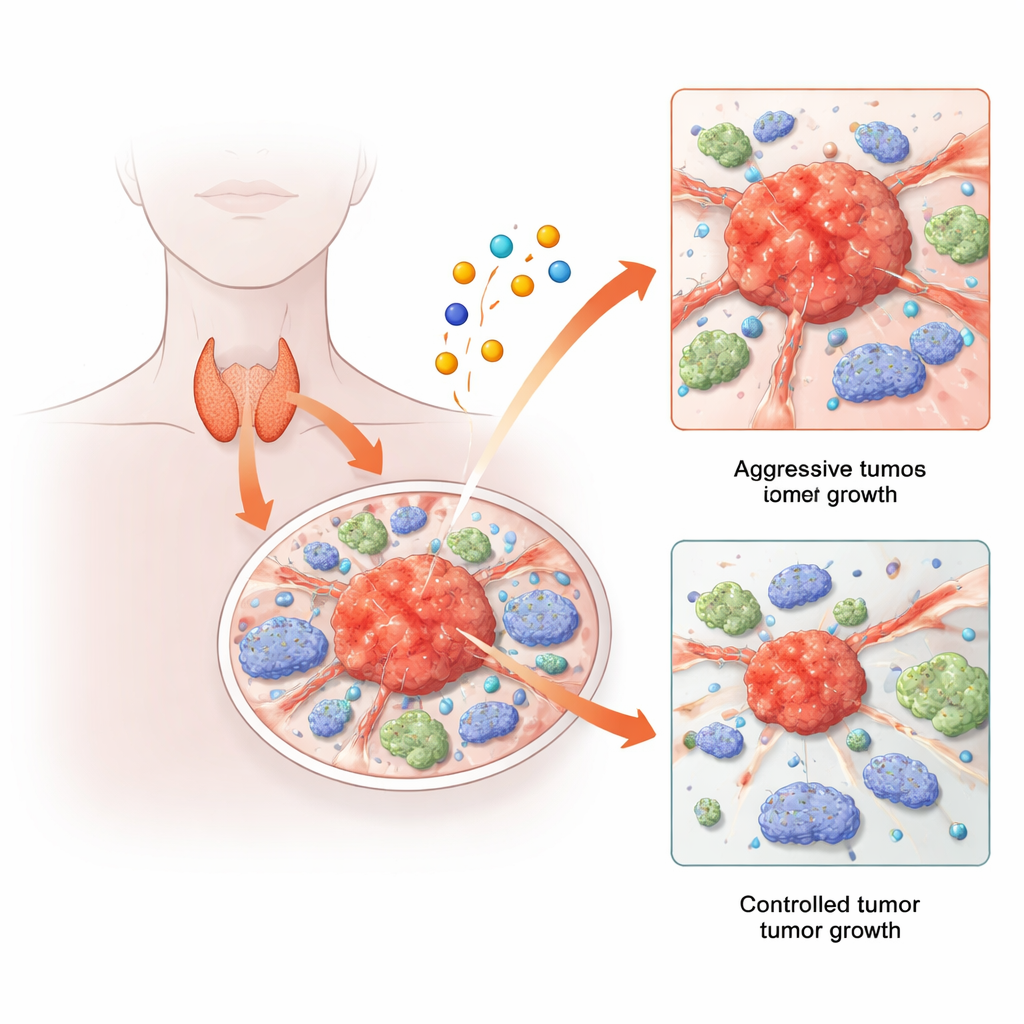
Анализ меди-связанных генов у большого числа пациентов
Исследователи начали с «мультиомных» наборов данных — больших коллекций генетических и молекулярных измерений — от сотен пациентов с раком щитовидной железы. Они сосредоточились на 19 генах, известных участием в меди-индуцированной гибели клеток, и сравнили их поведение в опухолях и в нормальной ткани щитовидной железы. С помощью статистической кластеризации пациенты были разделены на два молекулярных подтипа по активности этих меди-связанных генов. Один подтип демонстрировал более выраженные сигналы, связанные с иммунными ответами, тогда как другой был сильнее связан с изменениями метаболизма — энергетической и «строительной» машиной клетки. Эти отличия позволили предположить, что медная биология может влиять не только на сами опухолевые клетки, но и на то, как опухоли взаимодействуют с системой защиты организма.
Иммунное окружение и прогноз пациентов
Далее команда изучила, как эти меди-связанные подтипы коррелируют с опухолевым микросредой — сочетанием иммунных клеток и вспомогательной ткани вокруг опухоли. Они обнаружили, что у одного подтипа была более высокая экспрессия иммунных «контрольных» молекул, являющихся важными мишенями современных иммунотерапевтических препаратов, и более выраженная инфильтрация различными типами иммунных клеток. Авторы также создали риск-скор на основе меди-ассоциированных генов, который мог разделять пациентов на группы с лучшей и худшей выживаемостью. Пациенты с высоким скором, как правило, имели более короткую общую выживаемость и иной баланс иммунных клеток в опухолях, в том числе меньше Т-клеток, борющихся с раком. Это указывает на то, что меди-связанные пути могут влиять на способность иммунной системы распознавать и атаковать опухоли щитовидной железы.
Выделение ключевого проблемного гена
Среди 19 меди-связанных генов выделился один: CDKN2A. В отличие от большинства других, экспрессия которых была снижена в опухолях, CDKN2A постоянно была повышена при раке щитовидной железы и тесно ассоциировалась с худшим прогнозом. Одно-клеточная секвенирование — подход, считывающий активность генов в тысячах отдельных клеток — показало, что CDKN2A особенно активен в опухолевых клетках щитовидной железы и в некоторых иммунных и поддерживающих клетках. В лабораторных экспериментах усиление экспрессии CDKN2A в раковых клетках щитовидной железы делало их более пролиферативными, инвазивными и подвижными как в культурах, так и у мышей. Подавление CDKN2A имело обратный эффект: опухоли уменьшались, и снижалось число метастазов в лёгких. Эти результаты примечательны тем, что CDKN2A в классическом представлении рассматривается как «тормоз» клеточного деления в многих видах рака; в контексте щитовидной железы он, по-видимому, действует скорее как акселератор.
Скрытый РНК-контур, подпитывающий рост опухоли
Чтобы понять, почему CDKN2A столь активен, авторы искали вышестоящую регулирующую цепь. Они выявили трёхзвенную РНК-сеть, включающую длинную некодирующую РНК GAS5, короткую регуляторную РНК miR-128-3p и сам ген CDKN2A. По сути, GAS5 выступает губкой, связывающей miR-128-3p и препятствующей этой малой РНК прикрепляться к CDKN2A и подавлять его. При высоком уровне GAS5 miR-128-3p секвестрируется, CDKN2A уходит из-под контроля, и раковые клетки становятся более агрессивными. При подавлении GAS5 miR-128-3p восстанавливается, уровень CDKN2A падает, и опухолевые клетки теряют большую часть своей способности к росту и распространению. 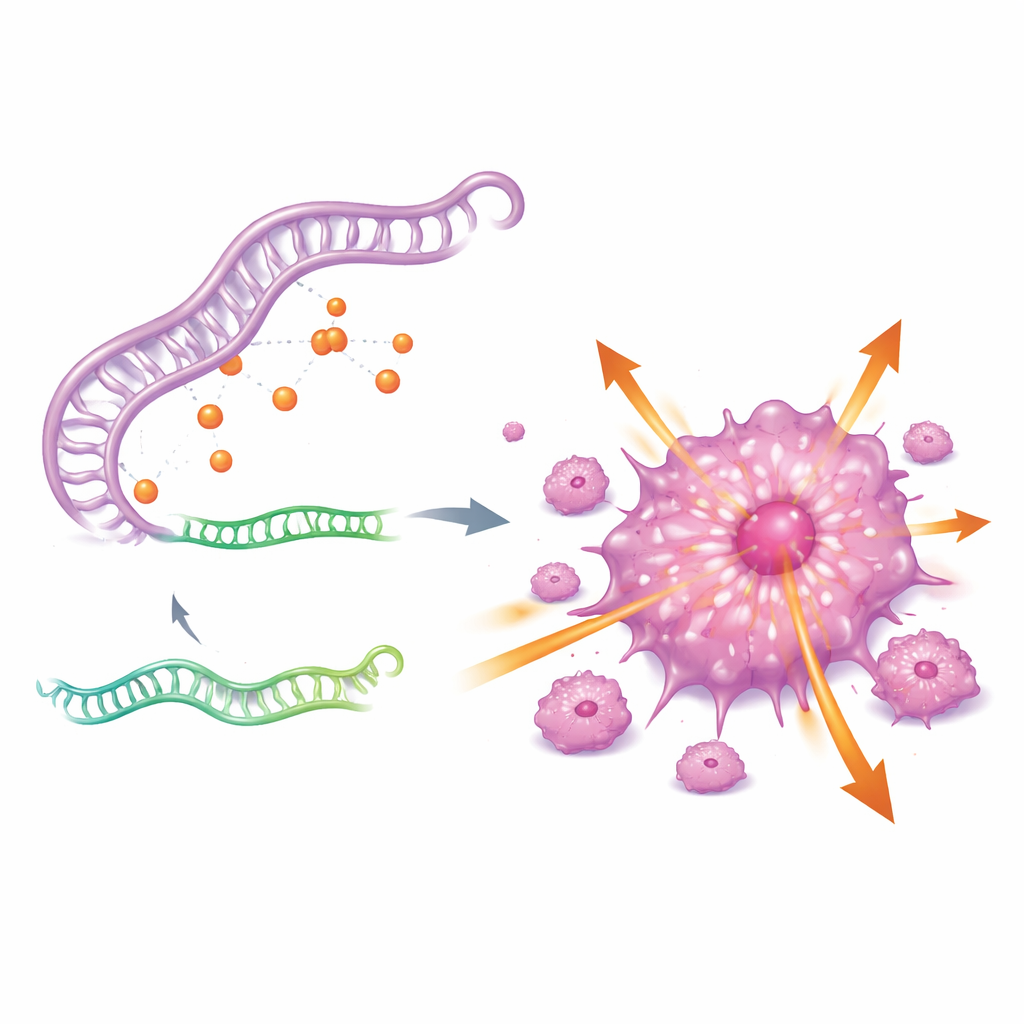
Что это означает для будущей помощи пациентам
Эта работа создаёт системную картину того, как меди-связанный путь смерти клеток, клетки опухоли щитовидной железы и окружающие иммунные клетки переплетены между собой. Хотя исследование ещё не доказывает, что меди-индуцированная гибель клеток непосредственно движет прогрессированием рака щитовидной железы, оно ясно показывает, что меди-ассоциированные гены — и особенно сеть GAS5/miR-128-3p/CDKN2A — связаны с более агрессивным течением болезни. Для пациентов это в перспективе может означать новые анализы крови или ткани для более точной оценки риска и новые препараты, нарушающие этот РНК-контур или модулирующие меди-связанные процессы, чтобы склонить баланс в пользу контроля опухоли, а не её роста.
Цитирование: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Ключевые слова: рак щитовидной железы, купроптоз, опухолевый микросреда, CDKN2A, некодирующая РНК