Clear Sky Science · pl
Zintegrowana analiza multi-omics i pojedynczych komórek ujawnia mechanizmy cuproptozy związane z CDKN2A napędzające progresję raka tarczycy
Dlaczego miedź i rak tarczycy mają znaczenie
Rak tarczycy zazwyczaj nadaje się do leczenia, ale niepokojąca mniejszość pacjentów rozwija guzy, które nawracają, dają przerzuty lub opierają się standardowym terapiom. Równocześnie badacze odkryli nowy sposób śmierci komórkowej wywoływany przez metal — miedź. Niniejsze badanie łączy te dwa wątki: bada, jak szlaki śmierci komórkowej związane z miedzią oraz geny je kontrolujące kształtują zachowanie nowotworów tarczycy i komórek układu odpornościowego w ich otoczeniu. Dzięki połączeniu analiz dużych zbiorów danych z badaniami pojedynczych komórek i eksperymentami na zwierzętach autorzy odkrywają zaskakującą sieć genową, która zdaje się sprzyjać wzrostowi i rozprzestrzenianiu się raka tarczycy — i może wskazywać nowe cele terapeutyczne w przyszłości. 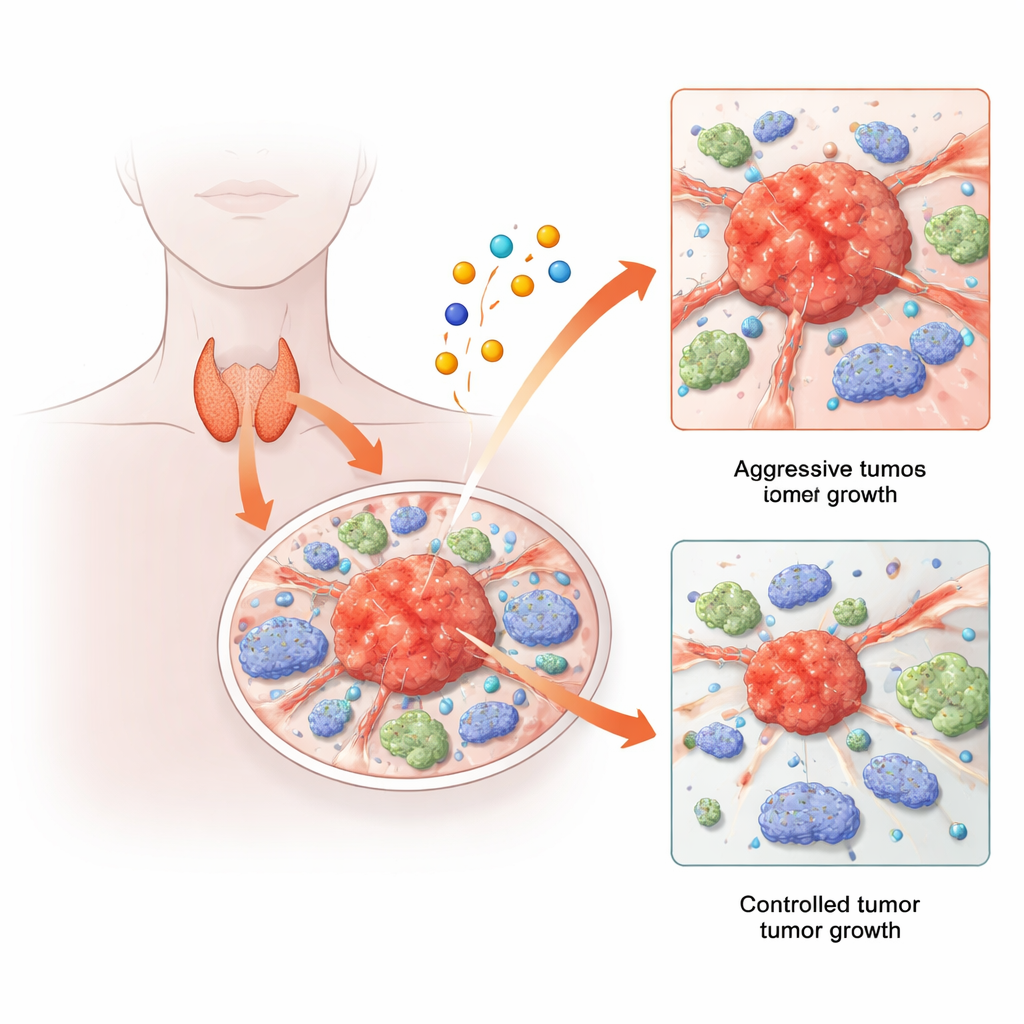
Analiza genów związanych z miedzią u wielu pacjentów
Badacze zaczęli od zestawów danych „multi-omics” — dużych zbiorów genetycznych i molekularnych pomiarów — pochodzących od setek pacjentów z rakiem tarczycy. Skoncentrowali się na 19 genach znanych z udziału w śmierci komórkowej wywoływanej przez miedź i sprawdzili, jak te geny zachowywały się w guzach w porównaniu z prawidłową tkanką tarczycy. Przy użyciu klasteryzacji statystycznej podzielili pacjentów na dwa podtypy molekularne na podstawie aktywności tych genów związanych z miedzią. Jeden podtyp wykazywał silniejsze sygnały związane z odpowiedzią immunologiczną, podczas gdy drugi wiązał się bardziej ze zmianami w metabolizmie — maszynerii energetycznej i budulcowej komórki. Te odrębne wzorce sugerowały, że biologia miedzi może wpływać nie tylko na same komórki nowotworowe, lecz także na sposób, w jaki guzy wchodzą w interakcje z obroną organizmu.
Mikrośrodowisko immunologiczne i rokowania pacjentów
Następnie zespół zbadał, jak te podtypy związane z miedzią korelują z mikrośrodowiskiem guza — mieszanką komórek odpornościowych i tkanki wspierającej otaczającej nowotwór. Stwierdzili, że jeden podtyp miał wyższą ekspresję cząsteczek „punktów kontrolnych” immunologicznych, które są kluczowymi celami nowoczesnych leków immunoterapeutycznych, oraz większe nacieki wielu typów komórek odpornościowych. Opracowali też punktację ryzyka opartą na genach związanych z miedzią, która rozdzielała pacjentów na lepsze i gorsze rokowania. Pacjenci z wysokimi wynikami mieli tendencję do krótszego przeżycia całkowitego i innego składu komórek odpornościowych w guzie, w tym mniej komórek T zdolnych do walki z rakiem. To sugeruje, że szlaki związane z miedzią mogą wpływać na to, jak skutecznie układ odpornościowy rozpoznaje i atakuje guzy tarczycy.
Skupienie się na kluczowym genie wywołującym problemy
Wśród 19 genów powiązanych z miedzią wyróżnił się jeden: CDKN2A. W przeciwieństwie do większości pozostałych, które były obniżone w guzach, CDKN2A był konsekwentnie podwyższony w raku tarczycy i silnie powiązany z gorszymi wynikami klinicznymi. Sekwencjonowanie pojedynczych komórek — metoda odczytująca aktywność genów w tysiącach indywidualnych komórek — pokazało, że CDKN2A jest szczególnie aktywny w komórkach nowotworowych tarczycy oraz w niektórych komórkach odpornościowych i komórkach podporowych. W eksperymentach laboratoryjnych zwiększenie ekspresji CDKN2A w komórkach raka tarczycy sprawiało, że rosły, naciekały i migrowały agresywniej, zarówno in vitro, jak i u myszy. Wyciszenie CDKN2A dawało efekt przeciwny — zmniejszenie guzów i ograniczenie przerzutów do płuc. Te obserwacje są uderzające, ponieważ CDKN2A tradycyjnie uważany jest za „hamulec” podziałów komórkowych w wielu nowotworach; tutaj wydaje się pełnić rolę przyspieszającą, przynajmniej w kontekście tarczycy.
Ukryty obwód RNA, który zasila wzrost guza
Aby zrozumieć, dlaczego CDKN2A jest tak aktywny, autorzy szukali obwodu regulacyjnego działającego od góry. Odkryli trójskładnikową sieć RNA obejmującą długiego RNA niekodującego nazwanego GAS5, małą regulatorową mikroRNA miR-128-3p oraz gen CDKN2A. W uproszczeniu GAS5 działa jak gąbka wiążąca miR-128-3p, uniemożliwiając temu małemu RNA przyłączenie się do CDKN2A i jego stłumienie. Gdy poziomy GAS5 są wysokie, miR-128-3p jest izolowane, CDKN2A wymyka się kontroli, a komórki nowotworowe stają się bardziej agresywne. Po zahamowaniu GAS5 miR-128-3p odzyskuje aktywność, poziomy CDKN2A spadają, a komórki guza tracą dużą część zdolności do wzrostu i rozprzestrzeniania się. 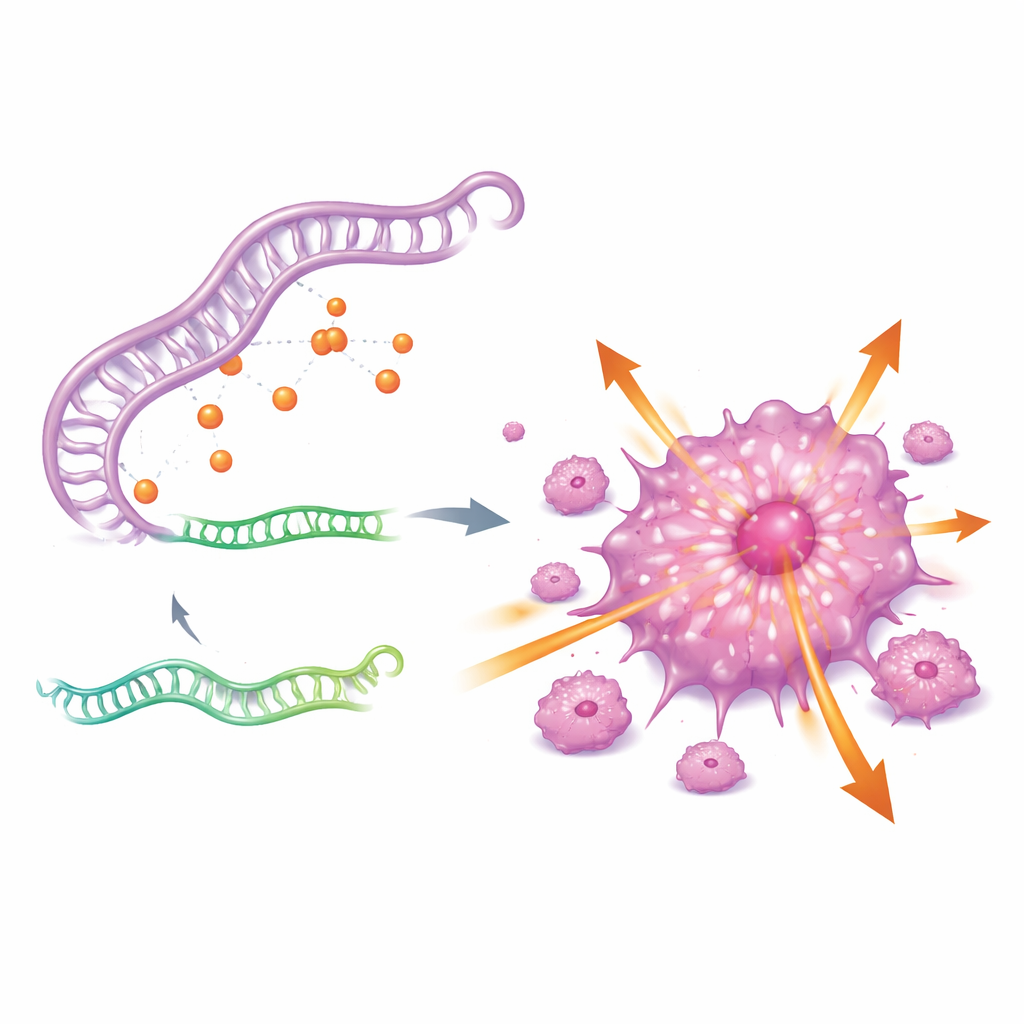
Co to oznacza dla przyszłej opieki
Praca ta kreśli obraz systemowy tego, jak szlak śmierci komórkowej związany z miedzią, komórki nowotworowe tarczycy i otaczające je komórki odpornościowe są ze sobą powiązane. Chociaż badanie nie dowodzi jeszcze, że śmierć komórkowa wywoływana przez miedź bezpośrednio napędza raka tarczycy, wyraźnie pokazuje, że geny związane z miedzią — a szczególnie sieć GAS5/miR-128-3p/CDKN2A — korelują z bardziej agresywną chorobą. Dla pacjentów może to w przyszłości oznaczać nowe testy krwi lub tkanki do lepszej oceny ryzyka oraz nowe leki, które zakłócą ten obwód RNA lub zmodyfikują procesy związane z miedzią, przeważając równowagę od wzrostu guza ku jego kontroli.
Cytowanie: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Słowa kluczowe: rak tarczycy, cuproptoza, mikrośrodowisko guza, CDKN2A, RNA niekodujące