Clear Sky Science · es
El análisis integrado multi-ómico y unicelular revela mecanismos de cuproptosis mediada por CDKN2A que impulsan la progresión del carcinoma de tiroides
Por qué importan el cobre y el cáncer de tiroides
El cáncer de tiroides suele ser tratable, pero una minoría preocupante de pacientes desarrolla tumores que recidivan, se diseminan o resisten las terapias estándar. Al mismo tiempo, los investigadores han descubierto una nueva vía de muerte celular desencadenada por el metal cobre. Este estudio une esas dos historias: explora cómo las vías de muerte celular vinculadas al cobre, y los genes que las regulan, moldean el comportamiento de los tumores de tiroides y de las células inmunitarias circundantes. Combinando análisis de grandes datos con experimentos unicelulares y en animales, los autores descubren una red génica sorprendente que parece ayudar al cáncer de tiroides a crecer y diseminarse, y que podría ofrecer nuevos blancos para tratamientos futuros. 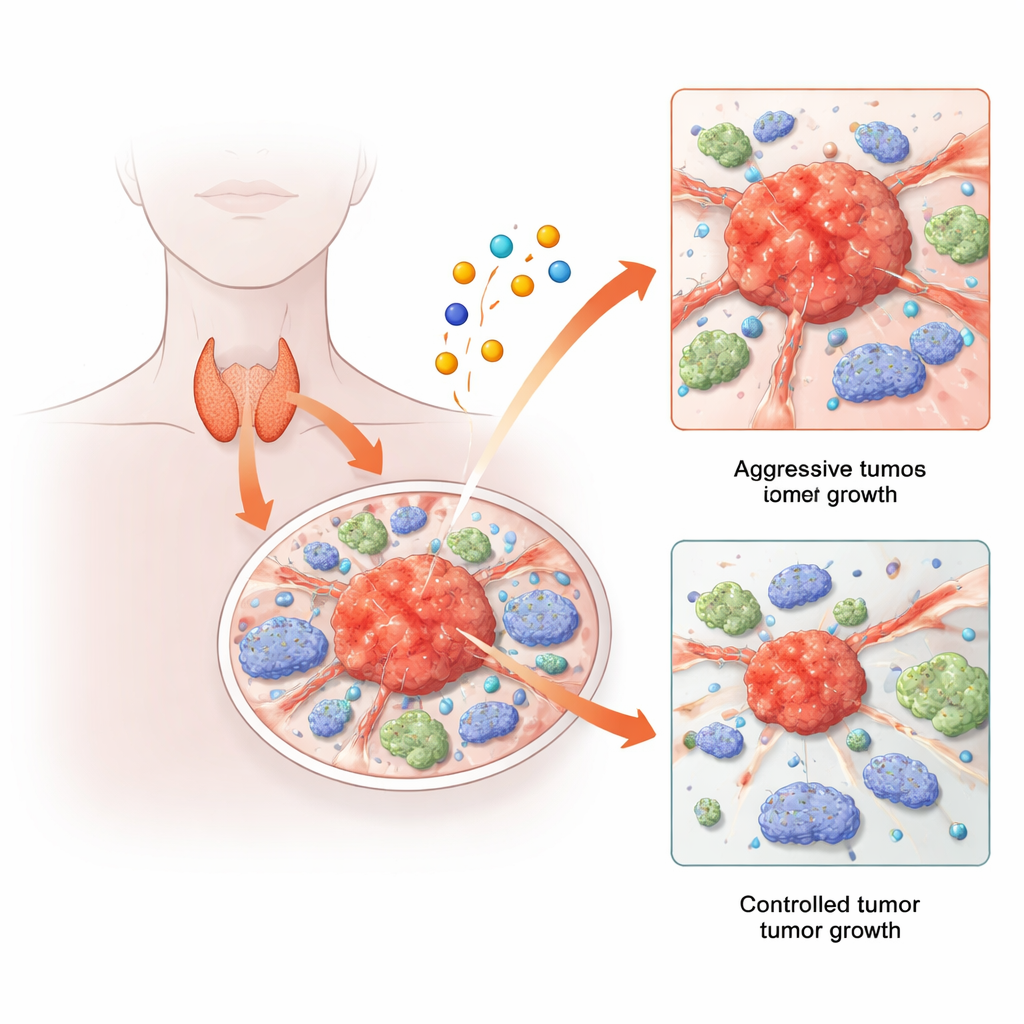
Analizando genes relacionados con el cobre en muchos pacientes
Los investigadores partieron de conjuntos de datos “multi-ómicos”, grandes colecciones de medidas genéticas y moleculares, procedentes de cientos de pacientes con cáncer de tiroides. Se centraron en 19 genes conocidos por participar en la muerte celular desencadenada por cobre y analizaron cómo se comportaban en los tumores frente al tejido tiroideo normal. Mediante clustering estadístico agruparon a los pacientes en dos subtipos moleculares según la actividad de estos genes relacionados con el cobre. Un subtipo mostró señales más fuertes relacionadas con respuestas inmunitarias, mientras que el otro se asoció más con alteraciones metabólicas, la maquinaria energética y de construcción de la célula. Estos patrones distintos sugirieron que la biología del cobre podría influir no solo en las células tumorales, sino también en cómo los tumores interactúan con las defensas del organismo.
El entorno inmunitario y el pronóstico del paciente
A continuación, el equipo examinó cómo se relacionaban estos subtipos vinculados al cobre con el microambiente tumoral—la mezcla de células inmunitarias y tejido de sostén alrededor del cáncer. Encontraron que un subtipo presentaba mayor expresión de moléculas inmunitarias de “punto de control”, que son blancos clave de los fármacos inmunoterapéuticos modernos, y una mayor infiltración por muchos tipos de células inmunitarias. También construyeron una puntuación de riesgo basada en genes asociados al cobre que podía separar a los pacientes con mejor y peor supervivencia. Los pacientes con puntuaciones altas tendían a tener una supervivencia global más corta y un equilibrio diferente de células inmunitarias en sus tumores, incluyendo menos células T antitumorales. Esto sugiere que las vías relacionadas con el cobre podrían influir en la capacidad del sistema inmunitario para reconocer y atacar los tumores tiroideos.
Focalizando un gen problemático clave
Entre los 19 genes vinculados al cobre, uno destacó: CDKN2A. A diferencia de la mayoría de los otros, que estaban reducidos en los tumores, CDKN2A se encontró consistentemente elevado en el cáncer de tiroides y fuertemente asociado a peores resultados. La secuenciación unicelular—un enfoque que mide la actividad génica en miles de células individuales—mostró que CDKN2A era especialmente activo en las células tumorales tiroideas y en ciertos tipos de células inmunitarias y de soporte. En experimentos de laboratorio, aumentar CDKN2A en células de cáncer de tiroides las hizo crecer, invadir y migrar con más agresividad, tanto en cultivos como en ratones. Silenciar CDKN2A tuvo el efecto contrario, reduciendo los tumores y las metástasis pulmonares. Estos hallazgos son llamativos porque CDKN2A se considera clásicamente un “freno” de la división celular en muchos cánceres; aquí parece actuar más como un acelerador, al menos en el contexto tiroideo.
Un circuito oculto de ARN que alimenta el crecimiento tumoral
Para entender por qué CDKN2A está tan activo, los autores buscaron un circuito regulatorio aguas arriba. Descubrieron una red de ARN de tres componentes que involucra un ARN largo no codificante llamado GAS5, un pequeño ARN regulador llamado miR-128-3p y el gen CDKN2A. En esencia, GAS5 actúa como una esponja que se une a miR-128-3p, impidiendo que este pequeño ARN se adhiera y reprima a CDKN2A. Cuando los niveles de GAS5 son altos, miR-128-3p queda secuestrado, CDKN2A escapa al control y las células cancerosas se vuelven más agresivas. Cuando se reduce GAS5, miR-128-3p se recupera, los niveles de CDKN2A caen y las células tumorales pierden gran parte de su capacidad para crecer y diseminarse. 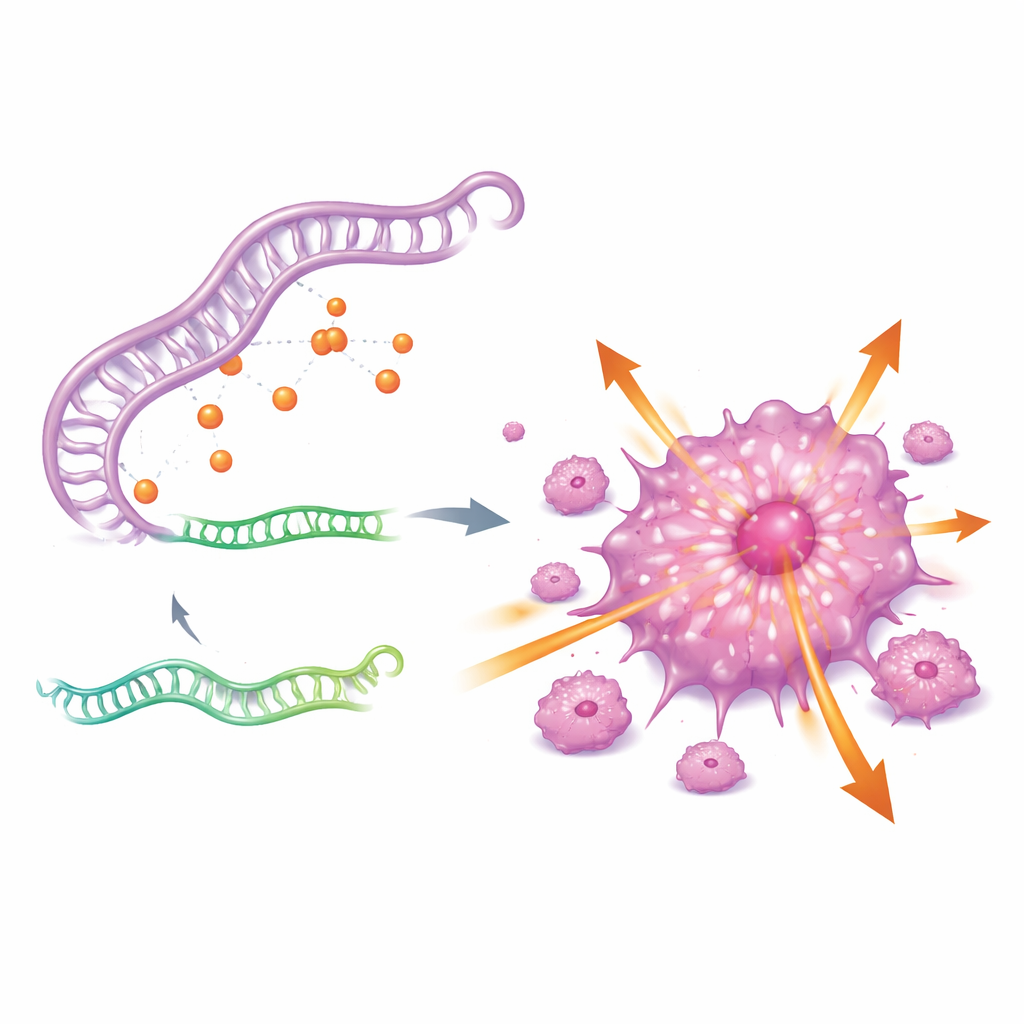
Qué implica esto para la atención futura
Este trabajo dibuja una imagen a nivel de sistemas de cómo una vía de muerte celular vinculada al cobre, las células tumorales tiroideas y las células inmunitarias circundantes están entrelazadas. Aunque el estudio aún no prueba que la cuproptosis esté directamente impulsando el cáncer de tiroides, muestra claramente que los genes relacionados con el cobre—y en especial la red GAS5/miR-128-3p/CDKN2A—se asocian con una enfermedad más peligrosa. Para los pacientes, eso podría traducirse eventualmente en nuevas pruebas de sangre o tejido para evaluar mejor el riesgo, y en fármacos que interrumpan este circuito de ARN o modulen procesos relacionados con el cobre para inclinar la balanza lejos del crecimiento tumoral y hacia el control del tumor.
Cita: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Palabras clave: cáncer de tiroides, cuproptosis, microambiente tumoral, CDKN2A, ARN no codificante