Clear Sky Science · fr
Analyse multi-omique intégrée et à cellule unique révèle des mécanismes de cuproptose médiés par CDKN2A favorisant la progression du carcinome thyroïdien
Pourquoi le cuivre et le cancer de la thyroïde comptent
Le cancer de la thyroïde est généralement traitable, mais une minorité préoccupante de patients développe des tumeurs qui récidivent, se propagent ou résistent aux traitements standards. Parallèlement, des chercheurs ont découvert un nouveau mode de mort cellulaire déclenché par le métal cuivre. Cette étude relie ces deux histoires : elle explore comment les voies de mort cellulaire liées au cuivre, et les gènes qui les régulent, influencent le comportement des tumeurs thyroïdiennes et des cellules immunitaires environnantes. En combinant analyses massives de données, séquençage à cellule unique et expériences animales, les auteurs dévoilent un réseau génique surprenant qui semble favoriser la croissance et la dissémination du cancer thyroïdien — et qui pourrait offrir de nouvelles cibles thérapeutiques à l’avenir. 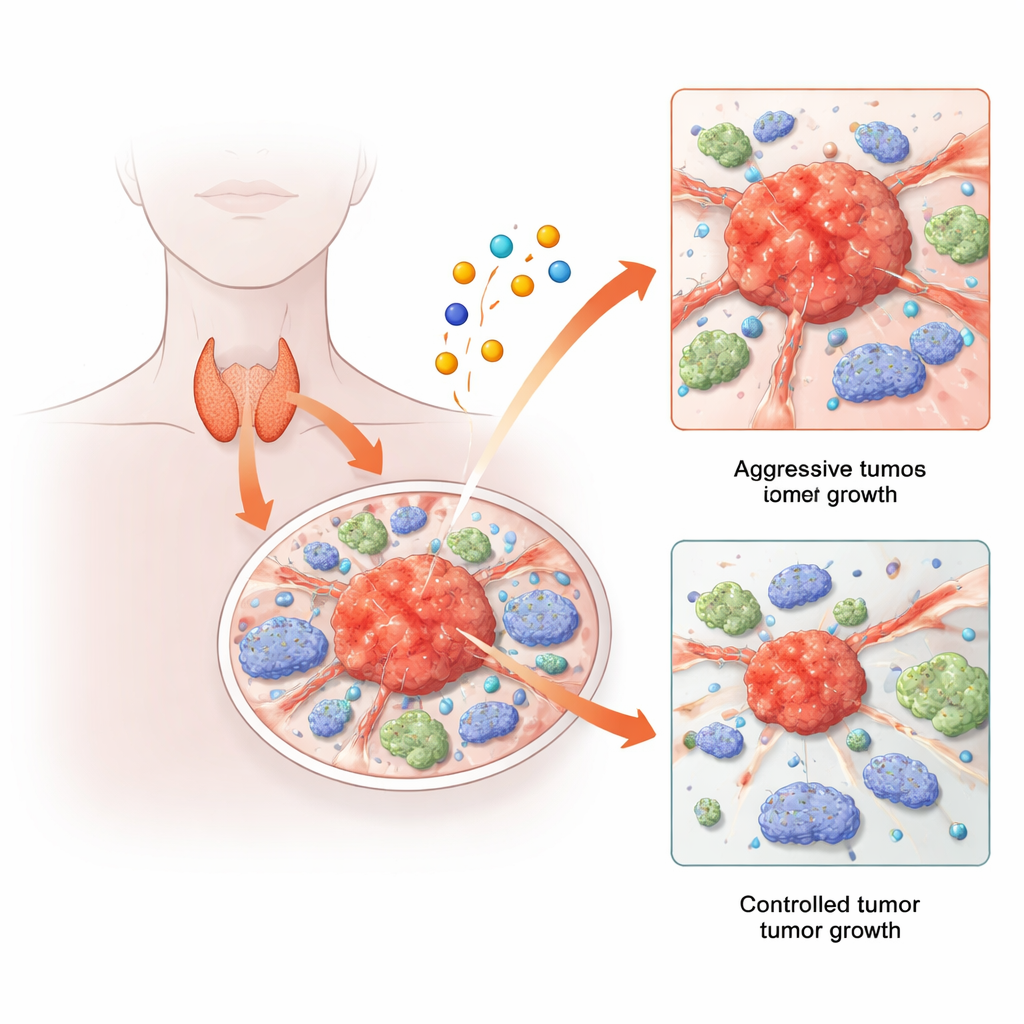
Étudier les gènes liés au cuivre chez de nombreux patients
Les chercheurs ont commencé par des jeux de données « multi-omiques » — de larges collections de mesures génétiques et moléculaires — provenant de centaines de patients atteints de cancer de la thyroïde. Ils se sont concentrés sur 19 gènes connus pour intervenir dans la mort cellulaire déclenchée par le cuivre et ont comparé leur comportement dans les tumeurs et dans le tissu thyroïdien normal. À l’aide de méthodes de regroupement statistique, ils ont classé les patients en deux sous-types moléculaires selon l’activité de ces gènes liés au cuivre. Un sous-type montrait des signaux plus marqués liés aux réponses immunitaires, tandis que l’autre était davantage associé à des altérations du métabolisme, la machinerie énergétique et biosynthétique de la cellule. Ces schémas distincts suggèrent que la biologie du cuivre pourrait influencer non seulement les cellules tumorales, mais aussi la manière dont les tumeurs interagissent avec les défenses de l’organisme.
Environnement immunitaire et pronostic des patients
Ensuite, l’équipe a examiné comment ces sous-types liés au cuivre se rapportaient au microenvironnement tumoral — le mélange de cellules immunitaires et de tissus de soutien autour du cancer. Ils ont constaté qu’un sous-type présentait une expression plus élevée de molécules de « point de contrôle » immunitaire, cibles clés des immunothérapies modernes, ainsi qu’une infiltration accrue par de nombreux types de cellules immunitaires. Ils ont aussi construit un score de risque fondé sur des gènes associés au cuivre capable de distinguer des patients à meilleur ou pire survie. Les patients avec des scores élevés avaient généralement une survie globale plus courte et un équilibre différent de cellules immunitaires dans leurs tumeurs, notamment moins de lymphocytes T effecteurs. Cela suggère que les voies liées au cuivre pourraient influencer la capacité du système immunitaire à reconnaître et à attaquer les tumeurs thyroïdiennes.
Focalisation sur un gène clé problématique
Parmi les 19 gènes associés au cuivre, un s’est détaché : CDKN2A. Contrairement à la plupart des autres, réduits dans les tumeurs, CDKN2A était systématiquement augmenté dans le cancer thyroïdien et fortement corrélé à de mauvais pronostics. Le séquençage à cellule unique — une approche qui mesure l’activité génique dans des milliers de cellules individuelles — a montré que CDKN2A était particulièrement actif dans les cellules tumorales thyroïdiennes et dans certains types cellulaires immunitaires et stromaux. En laboratoire, la surexpression de CDKN2A dans des cellules de cancer thyroïdien les a rendues plus proliférantes, invasives et migratoires, in vitro comme chez la souris. L’inhibition de CDKN2A produisait l’effet inverse, réduisant la taille des tumeurs et les métastases pulmonaires. Ces résultats sont marquants parce que CDKN2A est classiquement considéré comme un « frein » de la division cellulaire dans de nombreux cancers ; ici, il semble agir davantage comme un accélérateur, du moins dans le contexte thyroïdien.
Un circuit ARN caché qui alimente la croissance tumorale
Pour comprendre pourquoi CDKN2A est si actif, les auteurs ont cherché un circuit de régulation en amont. Ils ont mis au jour un réseau ARN tripartite impliquant un ARN long non codant nommé GAS5, un petit ARN régulateur miR-128-3p, et le gène CDKN2A. Essentiellement, GAS5 agit comme une éponge qui séquestre miR-128-3p, empêchant ce petit ARN de se lier à CDKN2A et d’en diminuer l’expression. Lorsque les niveaux de GAS5 sont élevés, miR-128-3p est piégé, CDKN2A échappe au contrôle et les cellules cancéreuses deviennent plus agressives. Lorsque GAS5 est réduit, miR-128-3p reprend son activité, CDKN2A diminue et les cellules tumorales perdent une grande partie de leur capacité à croître et à se disséminer. 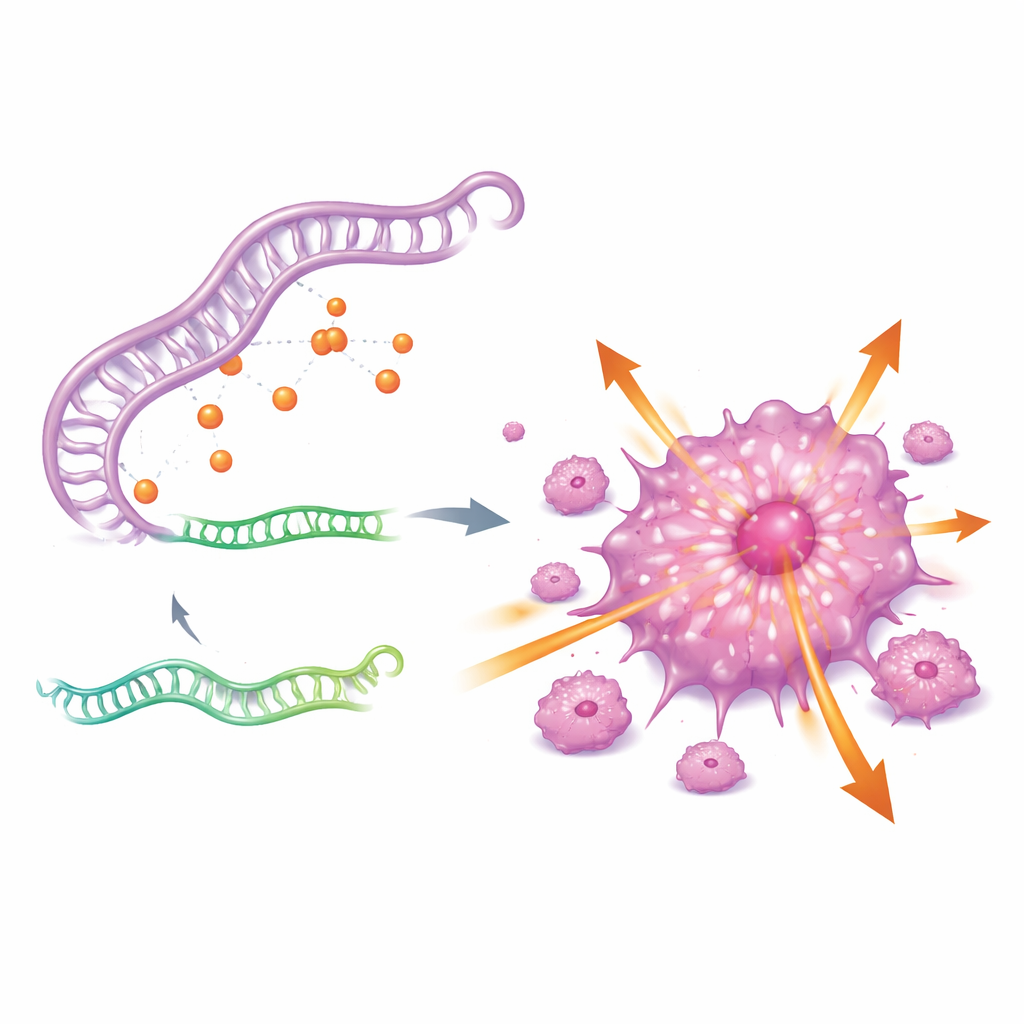
Ce que cela signifie pour les soins futurs
Ce travail dresse un tableau systémique de la manière dont une voie de mort cellulaire liée au cuivre, les cellules tumorales thyroïdiennes et les cellules immunitaires environnantes sont interconnectées. Si l’étude ne prouve pas encore que la cuproptose est directement responsable du développement du cancer thyroïdien, elle montre clairement que les gènes liés au cuivre — et en particulier le réseau GAS5/miR-128-3p/CDKN2A — sont associés à une maladie plus agressive. Pour les patients, cela pourrait à terme se traduire par de nouveaux tests sanguins ou tissulaires pour mieux évaluer le risque, et par des médicaments visant à perturber ce circuit ARN ou à moduler les processus liés au cuivre afin d’orienter l’équilibre vers le contrôle tumoral plutôt que la croissance.»
Citation: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Mots-clés: cancer de la thyroïde, cuproptose, microenvironnement tumoral, CDKN2A, ARN non codant