Clear Sky Science · de
Integrierte Multi-Omics- und Einzelzellanalyse enthüllt CDKN2A-vermittelte Cuproptose-Mechanismen, die das Fortschreiten von Schilddrüsenkarzinomen antreiben
Warum Kupfer und Schilddrüsenkrebs wichtig sind
Schilddrüsenkrebs ist in der Regel behandelbar, doch eine beunruhigende Minderheit von Patienten entwickelt Tumoren, die wiederkehren, metastasieren oder gegenüber Standardtherapien resistent sind. Gleichzeitig haben Forschende eine neue Form des Zelltods entdeckt, die durch das Metall Kupfer ausgelöst wird. Diese Studie verbindet diese beiden Themen: Sie untersucht, wie kupferverknüpfte Zelltodwege und die Gene, die sie steuern, das Verhalten von Schilddrüsentumoren und ihrer umgebenden Immunzellen formen. Durch die Kombination von groß angelegter Datenanalyse mit Einzelzell- und Tierexperimenten decken die Autorinnen und Autoren ein überraschendes Gen-Netzwerk auf, das offenbar das Wachstum und die Ausbreitung von Schilddrüsenkrebs fördert — und das potenziell neue Ansatzpunkte für künftige Therapien bietet. 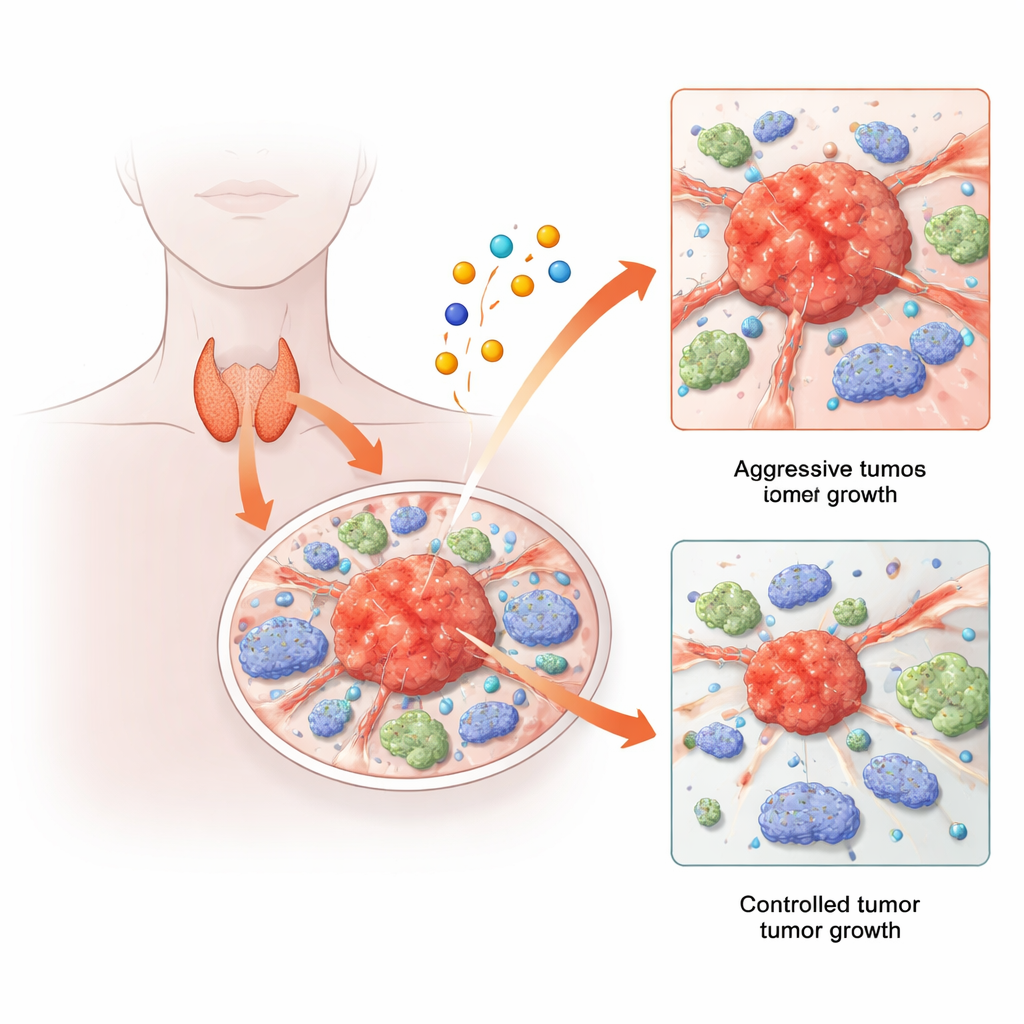
Betrachtung kupferverknüpfter Gene über viele Patienten hinweg
Die Forschenden begannen mit Multi-Omics-Datensätzen — umfangreichen Sammlungen genetischer und molekularer Messwerte — von Hunderten Schilddrüsenkrebspatienten. Sie konzentrierten sich auf 19 Gene, die an kupferindiziertem Zelltod beteiligt sind, und untersuchten, wie diese Gene in Tumoren im Vergleich zu normalem Schilddrüsengewebe exprimiert werden. Mit statistischer Clusteranalyse teilten sie die Patienten in zwei molekulare Subtypen ein, basierend auf der Aktivität dieser kupferbezogenen Gene. Ein Subtyp zeigte ausgeprägtere Signale, die mit Immunantworten zusammenhängen, während der andere stärker mit Veränderungen im Stoffwechsel, also den Energie- und Baustoffprozessen der Zelle, verknüpft war. Diese unterschiedlichen Muster deuteten darauf hin, dass Kupfer-Biologie nicht nur die Tumorzellen selbst beeinflussen könnte, sondern auch, wie Tumoren mit den Abwehrmechanismen des Körpers interagieren.
Immunsurroundings und Ausblick für Patienten
Als Nächstes untersuchte das Team, wie diese kupferbezogenen Subtypen mit der Tumormikroumgebung zusammenhängen — der Mischung aus Immunzellen und stützendem Gewebe um den Tumor herum. Sie fanden heraus, dass ein Subtyp eine höhere Expression von Immun-Checkpoint-Molekülen aufwies, die zentrale Ziele moderner Immuntherapien sind, sowie eine stärkere Infiltration durch verschiedene Arten von Immunzellen. Außerdem entwickelten sie einen Risikoscore auf Basis kupferassoziierter Gene, der Patienten mit besserer versus schlechterer Überlebensprognose unterscheiden konnte. Patienten mit hohen Scores hatten tendenziell eine kürzere Gesamtüberlebenszeit und ein anderes Gleichgewicht von Immunzellen im Tumor, einschließlich weniger krebsbekämpfender T‑Zellen. Das legt nahe, dass kupferbezogene Wege beeinflussen könnten, wie gut das Immunsystem Schilddrüsentumoren erkennt und angreift.
Fokussierung auf ein Schlüsselgen mit problematischer Rolle
Unter den 19 kupferverknüpften Genen stach eines besonders hervor: CDKN2A. Im Gegensatz zu den meisten anderen, die in Tumoren vermindert waren, zeigte CDKN2A in Schilddrüsenkrebs durchgängig erhöhte Werte und war stark mit schlechteren Ergebnissen assoziiert. Einzelzellsequenzierung — ein Ansatz, der die Genaktivität in Tausenden einzelner Zellen erfasst — zeigte, dass CDKN2A besonders in Schilddrüsentumorzellen sowie in bestimmten Immun- und Stütz-Zelltypen aktiv war. In Laborversuchen förderte eine Hochregulation von CDKN2A in Schilddrüsenkrebszellen deren Wachstum, Invasion und Migration sowohl in Zellkulturen als auch in Mäusen. Eine Herunterregulierung von CDKN2A bewirkte das Gegenteil: Tumoren schrumpften und Lungenmetastasen nahmen ab. Diese Befunde sind bemerkenswert, weil CDKN2A klassischerweise in vielen Krebsarten als ‚Bremse‘ für Zellteilung gilt; hier scheint es im Schilddrüsenkontext eher wie ein Beschleuniger zu wirken.
Ein verborgenes RNA‑Schaltkreis, das Tumorwachstum fördert
Um zu verstehen, warum CDKN2A so aktiv ist, suchten die Autorinnen und Autoren nach einer upstream-Regulationsschaltung. Sie identifizierten ein dreiteiliges RNA‑Netzwerk, bestehend aus einer langen nichtkodierenden RNA namens GAS5, einer kleinen regulatorischen RNA miR‑128‑3p und dem CDKN2A‑Gen. Im Wesentlichen wirkt GAS5 wie ein Schwamm, der miR‑128‑3p bindet und dadurch verhindert, dass diese kleine RNA an CDKN2A anlagert und dessen Expression dämpft. Bei hohen GAS5‑Spiegeln wird miR‑128‑3p sequestriert, CDKN2A entkommt der Kontrolle und Krebszellen werden aggressiver. Wird GAS5 herunterreguliert, erholt sich miR‑128‑3p, CDKN2A‑Spiegel fallen und die Tumorzellen verlieren viel von ihrer Fähigkeit zu wachsen und sich auszubreiten. 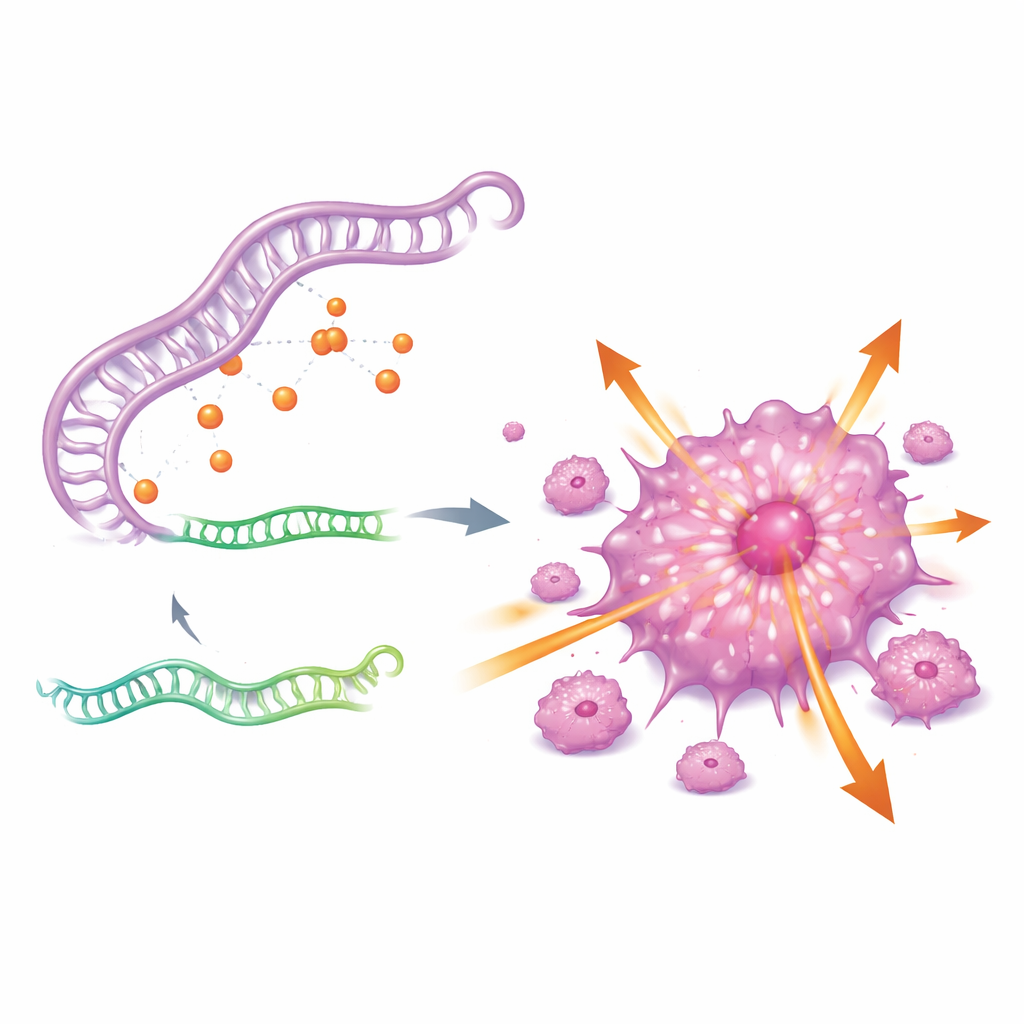
Was das für die zukünftige Versorgung bedeutet
Diese Arbeit zeichnet ein Systembild davon, wie ein kupferverknüpfter Zelltodweg, Schilddrüsentumorzellen und die umgebenden Immunzellen miteinander verflochten sind. Zwar beweist die Studie noch nicht, dass kupferausgelöster Zelltod direkt das Fortschreiten von Schilddrüsenkrebs verursacht, doch sie zeigt deutlich, dass kupferbezogene Gene — und insbesondere das GAS5/miR‑128‑3p/CDKN2A‑Netzwerk — mit aggressiverer Erkrankung verknüpft sind. Für Patienten könnte das letztlich in neue Blut‑ oder Gewebetests münden, um das Risiko besser einzuschätzen, sowie in neue Medikamente, die diesen RNA‑Kreislauf stören oder kupferbezogene Prozesse modulieren, um das Gleichgewicht weg vom Tumorwachstum hin zur Tumorkontrolle zu verschieben.
Zitation: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Schlüsselwörter: Schilddrüsenkrebs, Cuproptose, Tumormikroumgebung, CDKN2A, nichtkodierende RNA