Clear Sky Science · nl
Geïntegreerde multi-omics- en single-cell-analyse onthult CDKN2A-gemedieerde cuproptose-mechanismen die de progressie van schildkliercarcinoom aansturen
Waarom koper en schildklierkanker van belang zijn
Schildklierkanker is meestal behandelbaar, maar een zorgwekkende minderheid van patiënten ontwikkelt tumoren die terugkeren, uitzaaien of resistent worden tegen standaardtherapieën. Tegelijkertijd hebben onderzoekers een nieuwe manier ontdekt waarop cellen kunnen sterven, veroorzaakt door het metaal koper. Deze studie brengt die twee verhaallijnen samen: ze onderzoekt hoe koper-gerelateerde celdoodpaden en de genen die ze regelen, het gedrag van schildkliertumoren en de omringende immuuncellen beïnvloeden. Door big-data-analyse te combineren met single-cell- en dierexperimenten onthullen de auteurs een verrassend genennetwerk dat lijkt bij te dragen aan de groei en verspreiding van schildklierkanker — en dat mogelijke nieuwe doelen voor toekomstige behandelingen kan bieden. 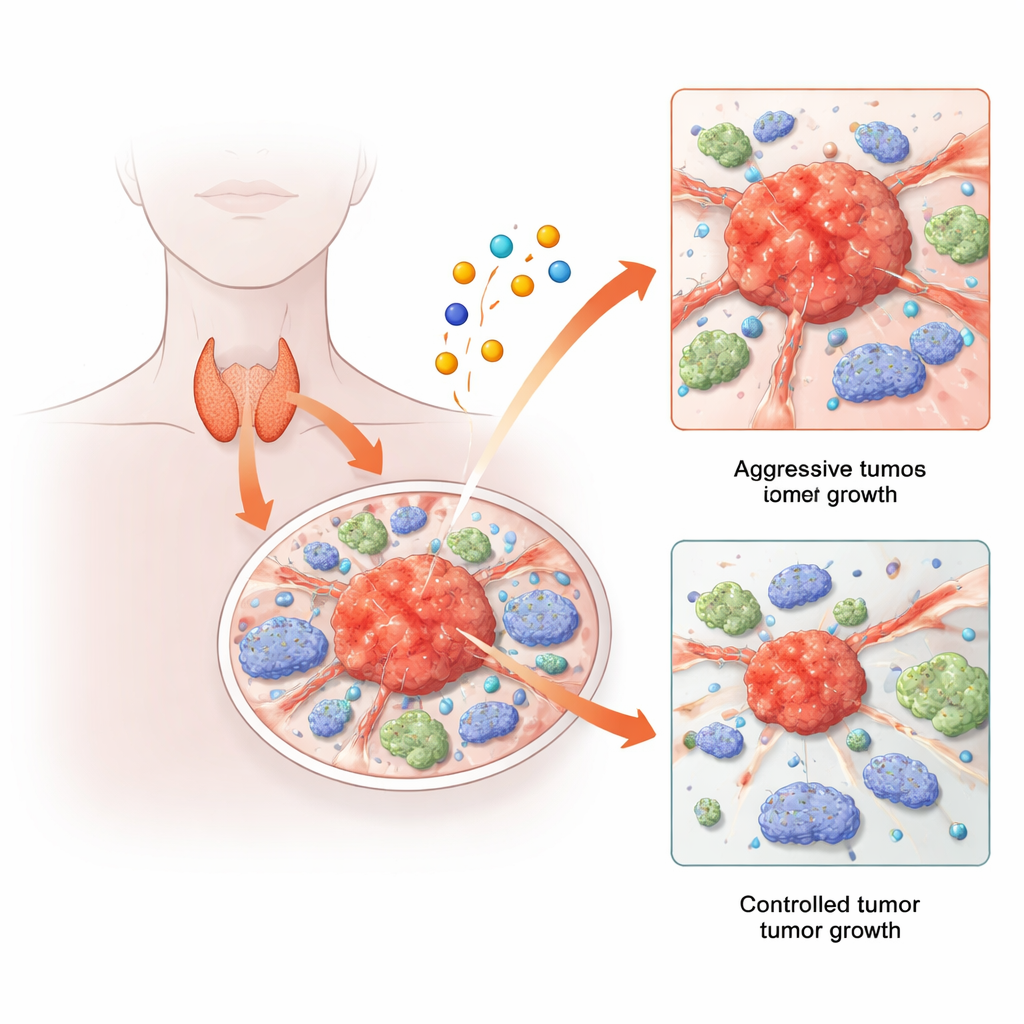
Het bekijken van koper-gerelateerde genen bij veel patiënten
De onderzoekers begonnen met “multi-omics”-datasets — grote verzamelingen genetische en moleculaire metingen — van honderden schildklierkankerpatiënten. Ze concentreerden zich op 19 genen waarvan bekend is dat ze betrokken zijn bij koper-geïnduceerde celdood en onderzochten hoe deze genen zich in tumoren verhouden tot normaal schildklierweefsel. Met behulp van statistische clustering deelden ze patiënten in twee moleculaire subtypes in op basis van de activiteit van deze koper-gerelateerde genen. Één subtype toonde sterkere signalen gerelateerd aan immuunresponsen, terwijl het andere meer gekoppeld leek aan veranderingen in de stofwisseling, de energie- en bouwstoffenfabriek van de cel. Deze verschillende patronen suggereerden dat koperbiologie niet alleen tumorcellen zelf kan beïnvloeden, maar ook hoe tumoren met de afweer van het lichaam interactieren.
Immuunomgeving en prognose
Vervolgens onderzocht het team hoe deze koper-gerelateerde subtypes zich verhouden tot de tumormicro-omgeving — de mix van immuuncellen en ondersteunend weefsel rondom de tumor. Ze vonden dat één subtype hogere expressie had van immuun-"checkpoint"-moleculen, die belangrijke doelwitten zijn van moderne immunotherapieën, en een grotere infiltratie door verschillende typen immuuncellen. Ze ontwikkelden ook een risicoscore gebaseerd op koper-geassocieerde genen die patiënten met betere versus slechtere overleving kon scheiden. Patiënten met hoge scores hadden doorgaans een kortere totale overleving en een andere balans van immuuncellen in hun tumoren, waaronder minder kankervijandige T-cellen. Dit suggereert dat koper-gerelateerde paden kunnen beïnvloeden hoe goed het immuunsysteem schildkliertumoren kan herkennen en aanvallen.
Inzoomen op een sleutelgen dat problemen veroorzaakt
Van de 19 koper-gerelateerde genen stak er één bovenuit: CDKN2A. In tegenstelling tot de meesten van de anderen, die in tumoren verlaagd waren, was CDKN2A consequent verhoogd in schildklierkanker en sterk geassocieerd met slechtere uitkomsten. Single-cell-sequencing — een methode die genactiviteit van duizenden individuele cellen uitleest — toonde dat CDKN2A bijzonder actief was in schildklier-tumorcellen en bepaalde immuun- en ondersteunende cellen. In laboratoriumexperimenten zorgde het verhogen van CDKN2A in schildklierkankercellen ervoor dat ze agressiever gingen groeien, invasief werden en meer migreerden, zowel in kweek als in muizen. Het uitschakelen van CDKN2A had het tegenovergestelde effect: tumoren werden kleiner en longmetastasen namen af. Deze bevindingen zijn opvallend omdat CDKN2A klassiek wordt gezien als een "rem" op celdeling in veel kankersoorten; hier lijkt het in de schildkliercontext meer als een gaspedaal te werken.
Een verborgen RNA-circuit dat tumorgroei voedt
Om te begrijpen waarom CDKN2A zo actief is, zochten de auteurs naar een upstream-regulerend circuit. Ze ontdekten een drieluik van RNA-regulatie bestaande uit een lang niet-coderend RNA genaamd GAS5, een klein regulerend RNA genaamd miR-128-3p, en het CDKN2A-gen. In wezen fungeert GAS5 als een spons die miR-128-3p bindt, waardoor dit kleine RNA niet kan binden aan en het niveau van CDKN2A kan dempen. Wanneer GAS5-niveaus hoog zijn, wordt miR-128-3p afgeschermd, ontsnapt CDKN2A aan controle en worden kankercellen agressiever. Wanneer GAS5 wordt gereduceerd, herstelt miR-128-3p zich, dalen CDKN2A-niveaus en verliezen tumorcellen veel van hun vermogen om te groeien en zich te verspreiden. 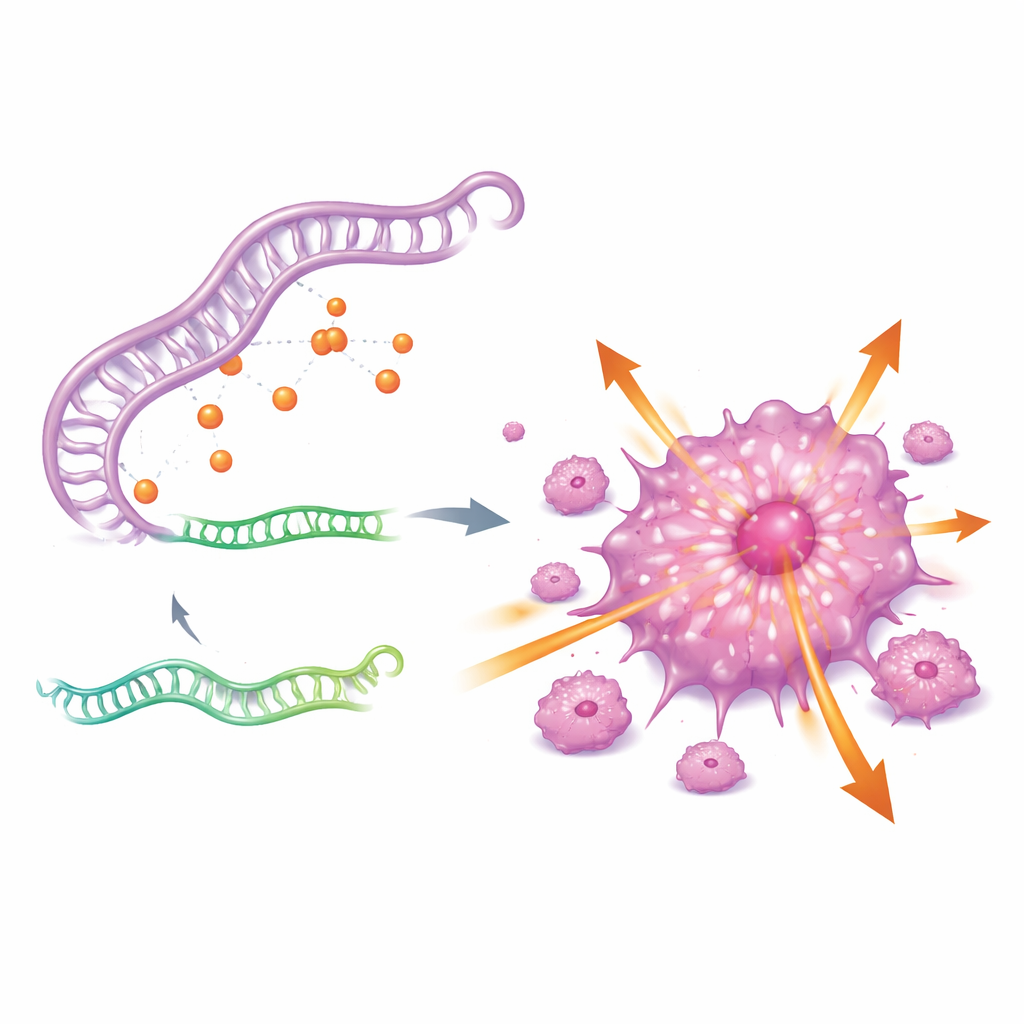
Wat dit betekent voor toekomstige zorg
Dit werk schetst een systeemniveaubeeld van hoe een koper-gerelateerd celdoodpad, schildklier-tumorcellen en omringende immuuncellen met elkaar verweven zijn. Hoewel de studie nog niet bewijst dat koper-geïnduceerde celdood direct schildklierkanker aandrijft, toont ze duidelijk aan dat koper-gerelateerde genen — en in het bijzonder het GAS5/miR-128-3p/CDKN2A-netwerk — geassocieerd zijn met agressievere ziekte. Voor patiënten kan dat uiteindelijk leiden tot nieuwe bloed- of weefseltesten om risico beter in te schatten, en nieuwe geneesmiddelen die dit RNA-circuit verstoren of koper-gerelateerde processen moduleren om de balans te verschuiven van tumorgroei naar tumorgroepscontrole.
Bronvermelding: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Trefwoorden: schildklierkanker, cuproptose, tumormicro-omgeving, CDKN2A, niet-coderende RNA