Clear Sky Science · sv
Integrerad multi-omik och single-cell-analys avslöjar CDKN2A-medierade cuproptosmekanismer som driver sköldkörtelkarcinomets progression
Varför koppar och sköldkörtelcancer spelar roll
Sköldkörtelcancer är vanligtvis behandlingsbar, men en oroväckande minoritet av patienterna utvecklar tumörer som återkommer, sprider sig eller är resistenta mot standardbehandlingar. Samtidigt har forskare upptäckt ett nytt sätt celler kan dö på, utlösts av metallen koppar. Denna studie förenar de två berättelserna: den undersöker hur kopparkopplade celldödsbanor, och generna som styr dem, påverkar beteendet hos sköldkörteltumörer och de omgivande immuncellerna. Genom att kombinera storskalig dataanalys med single-cell- och djurförsök avslöjar författarna ett överraskande gen-nätverk som verkar hjälpa sköldkörtelcancer att växa och sprida sig — och som kan erbjuda nya måltavlor för framtida behandlingar. 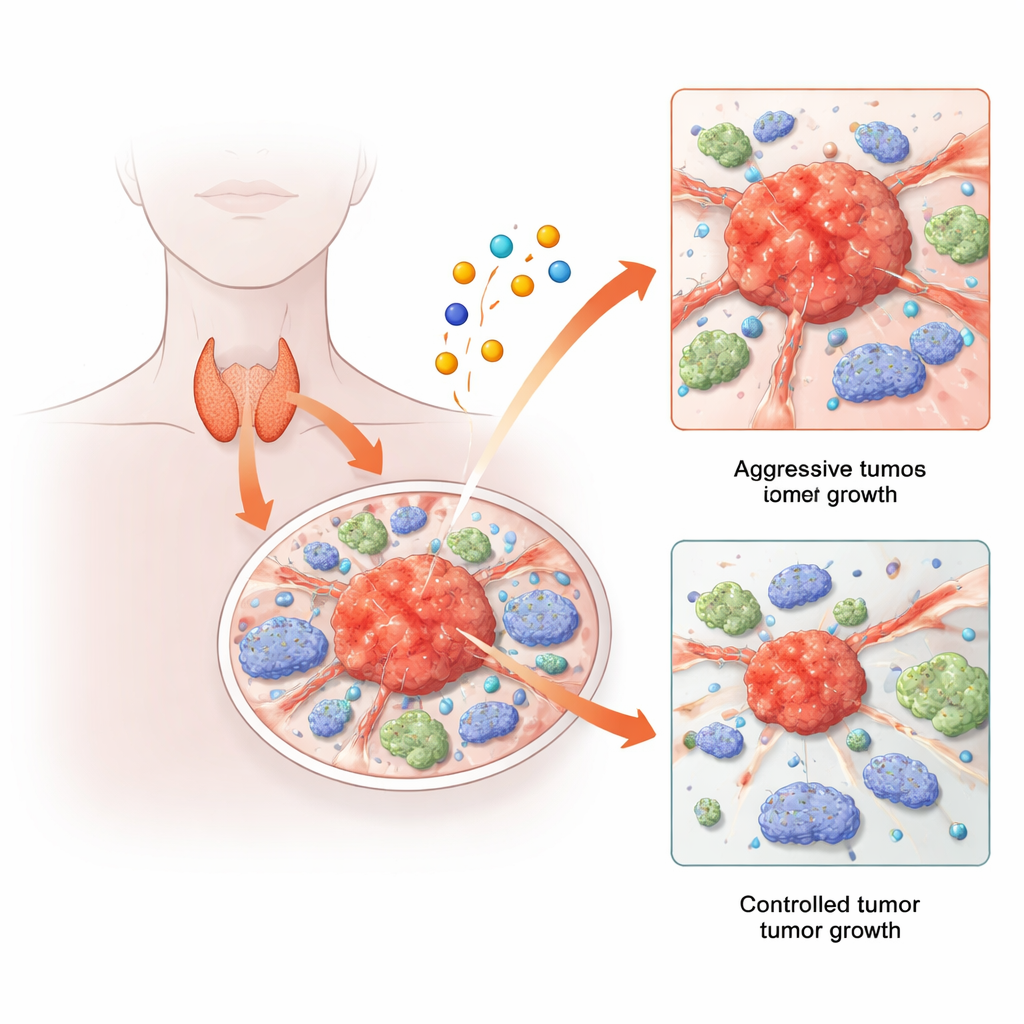
Att granska kopparrelaterade gener över många patienter
Forskarna började med ”multi-omik” dataset — stora samlingar av genetiska och molekylära mätningar — från hundratals patienter med sköldkörtelcancer. De fokuserade på 19 gener som är kända för att vara involverade i kopparutlösta celldödsprocesser och undersökte hur dessa gener betedde sig i tumörer jämfört med normalt sköldkörtelvävnad. Med hjälp av statistisk klustring grupperade de patienterna i två molekylära subtyper baserat på aktiviteten hos dessa kopparrelaterade gener. Den ena subtypen visade starkare signaler relaterade till immunsvar, medan den andra i större utsträckning kopplades till förändringar i metabolismen, cellens energioch byggstenmaskineri. Dessa distinkta mönster antydde att kopparbiologi kan påverka inte bara tumörcellerna själva utan också hur tumörer interagerar med kroppens försvar.
Immunsurroundingar och patientprognos
Därefter undersökte teamet hur dessa kopparkopplade subtyper relaterade till tumörmikromiljön — blandningen av immunceller och stödjevävnad runt cancern. De fann att en subtyp hade högre uttryck av immunkontrollpunktsmolekyler, vilka är viktiga mål för modern immunterapi, och större infiltrering av många typer av immunceller. De byggde också en riskpoäng baserad på kopparassocierade gener som kunde skilja patienter med bättre respektive sämre överlevnad. Patienter med höga poäng tenderade att ha kortare total överlevnad och en annan balans av immunceller i sina tumörer, inklusive färre cancerbekämpande T-celler. Detta tyder på att kopparrelaterade vägar kan påverka hur väl immunsystemet kan känna igen och attackera sköldkörteltumörer.
Fokusering på en nyckelgen som ställer till problem
Bland de 19 kopparkopplade generna stack en ut: CDKN2A. Till skillnad från de flesta andra, som var nedsatta i tumörer, var CDKN2A konsekvent förhöjt i sköldkörtelcancer och starkt kopplat till sämre utfall. Single-cell-sekvensering — en metod som läser genaktivitet i tusentals individuella celler — visade att CDKN2A var särskilt aktivt i sköldkörteltumörceller och i vissa immunceller och stödjeceller. I laboratorieförsök gjorde ökat CDKN2A i sköldkörtelcancerceller att de växte, invaderade och migrerade mer aggressivt, både i odlingsskålar och i möss. Att tysta CDKN2A gav motsatt effekt, krympte tumörer och minskade lungmetastaser. Dessa fynd är anmärkningsvärda eftersom CDKN2A klassiskt ses som en ”broms” för celldelning i många cancerformer; här verkar det snarare fungera som en accelerator, åtminstone i sköldkörtelsammanhanget.
En dold RNA-krets som ger tumörtillväxt
För att förstå varför CDKN2A är så aktivt letade författarna efter en upstream-reglerande krets. De identifierade ett treparts-RNA-nätverk som involverar ett långt icke-kodande RNA kallat GAS5, ett litet reglerande RNA kallat miR-128-3p, och genen CDKN2A. I praktiken fungerar GAS5 som en svamp som binder miR-128-3p och förhindrar detta lilla RNA från att fästa vid och dämpa CDKN2A. När GAS5-nivåerna är höga binds miR-128-3p upp, CDKN2A slipper reglering och cancerceller blir mer aggressiva. När GAS5 slås ned återhämtar sig miR-128-3p, CDKN2A-nivåerna sjunker och tumörceller förlorar mycket av sin förmåga att växa och sprida sig. 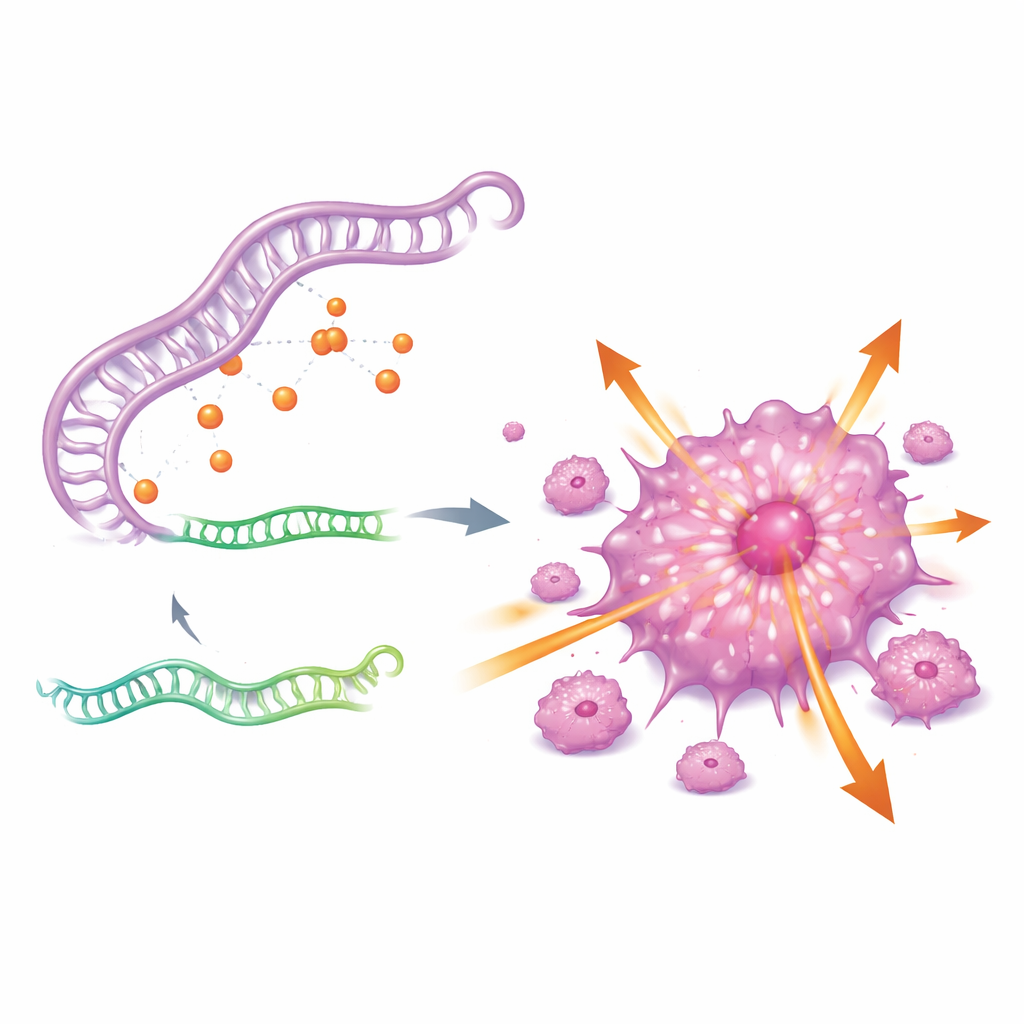
Vad detta betyder för framtida vård
Detta arbete målar upp en systemsnivåbild av hur en kopparkopplad celldödsväg, sköldkörteltumörceller och omgivande immunceller hänger ihop. Även om studien ännu inte bevisar att kopparutlöst celldöd direkt driver sköldkörtelcancer, visar den tydligt att kopparrelaterade gener — och särskilt GAS5/miR-128-3p/CDKN2A-nätverket — är kopplade till farligare sjukdom. För patienter skulle det så småningom kunna innebära nya blod- eller vävnadstester för att bättre bedöma risk, och nya läkemedel som stör denna RNA-krets eller påverkar kopparrelaterade processer för att skifta balansen bort från tumörtillväxt och mot tumörkontroll.
Citering: Huang, J., Wang, L. Integrated multi-omics and single-cell analysis reveals CDKN2A-mediated cuproptosis mechanisms driving thyroid carcinoma progression. npj Syst Biol Appl 12, 61 (2026). https://doi.org/10.1038/s41540-026-00663-w
Nyckelord: sköldkörtelcancer, cuproptos, tumörmikromiljö, CDKN2A, icke-kodande RNA