Clear Sky Science · zh
TGF-α/EGFR 介导的淋巴转移揭示乳腺癌中可重新定位的治疗靶点
这项研究为何对患者重要
当乳腺癌从乳房扩散时,常常首先出现在淋巴结中。临床上已知高表达 EGFR 的肿瘤往往表现为侵袭性强,但靶向抑制 EGFR 的药物在乳腺癌中疗效有限。本研究揭示了拼图中缺失的一块:EGFR 可能并非主要驱动肿瘤增殖,而是帮助肿瘤细胞“导航”进入淋巴管和淋巴结。这一视角的转变可能为在转移变成危及生命之前早期阻断其扩散,打开新的治疗途径。
肿瘤细胞的一条隐藏高速通道
研究者聚焦于三阴性乳腺癌——一种难治且常伴随高 EGFR 表达并早期累及淋巴结的亚型。在小鼠模型中,他们构建了过度表达 EGFR 的乳腺癌细胞并将其种植到乳腺组织中。出人意料的是,这些高 EGFR 肿瘤并没有更快生长,也没有比对照肿瘤产生更多肺转移。相反,更多的癌细胞出现在近旁的淋巴结中,即使在早期时间点也能观察到。显微镜显示淋巴管主要分布在肿瘤的外缘,提示肿瘤细胞必须主动向外移动以寻找并进入这些淋巴管。 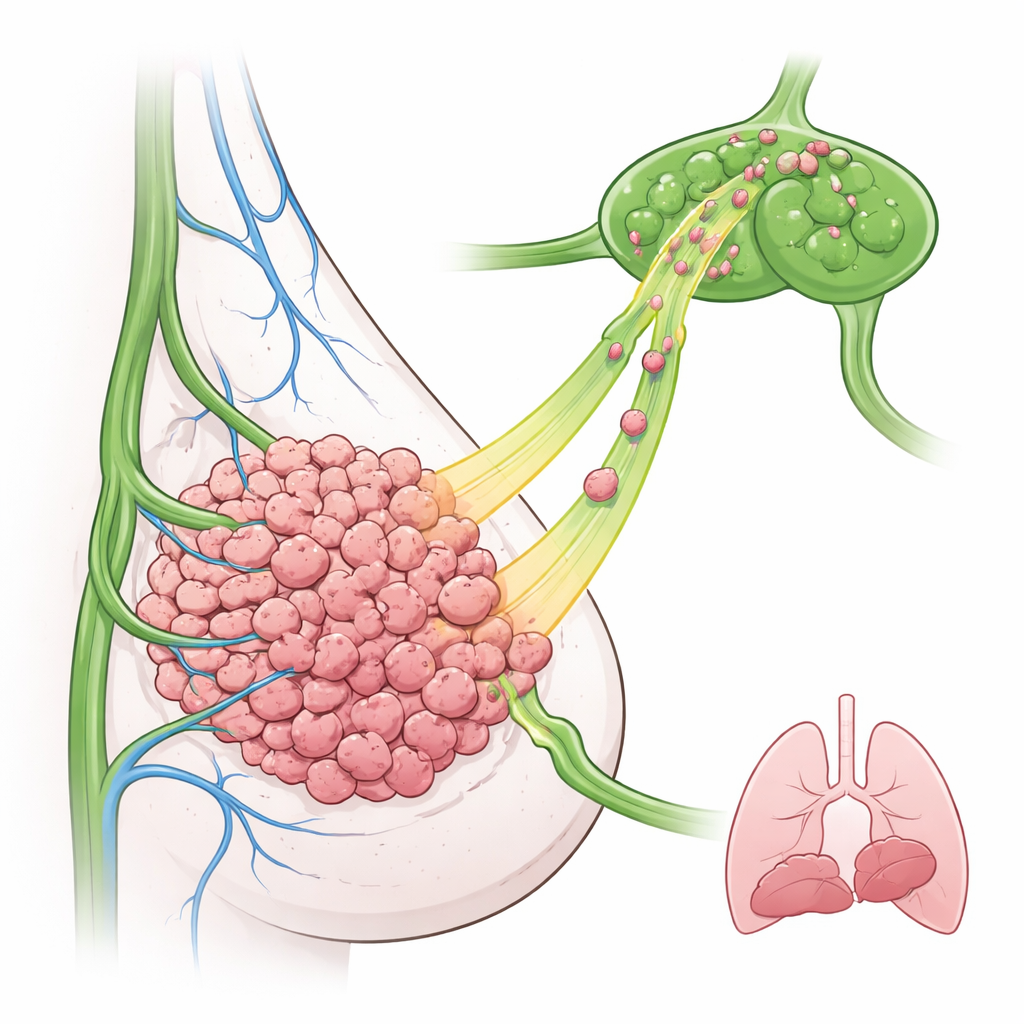
来自淋巴管本身的信号
研究团队接着问:淋巴管只是被动的管道,还是主动的引导者?他们在小鼠和人类乳腺肿瘤中研究了淋巴内皮细胞(构成淋巴管内壁的细胞)。当这些细胞暴露于另一种与肿瘤相关的分子 TGF-β 时,它们开始产生可激活 EGFR 的生长因子。其中一个因子 TGF-α 尤为突出:其表达显著上调,被释放到周围液体中,并在肿瘤组织中集中分布于淋巴管而非血管。人类数据表明,TGFA 水平较高的乳腺癌,尤其是与三阴性疾病相关的基底样亚型,预后更差。这些发现将 TGF-α 指向了可能的“嗅迹”,引导 EGFR 阳性的肿瘤细胞进入淋巴管。
肿瘤细胞如何沿着线索移动
为验证这一假设,研究者使用入侵和活细胞迁移实验。他们将过表达 EGFR 的肿瘤细胞置于凝胶上方,在下方提供淋巴内皮细胞的培养液或纯化的生长因子。富含 EGFR 的细胞明显向淋巴内皮细胞培养液和单独的 TGF-α 方向侵入,呈现出明确的定向移动,而不是随机游走。另一个与血管相关的因子 CTGF 不促进定向移动,甚至可能抑制 TGF-α 的作用。在肿瘤细胞内,TGF-α 激活了名为 STAT3 的信号分子以及其他通路。当用化学方法抑制 STAT3 时,肿瘤细胞向淋巴信号移动的能力大为减弱。在人类三阴性乳腺癌细胞系中也观察到相同的由 TGF-α 驱动、依赖 EGFR 的趋化迁移,证实这种行为并不限于小鼠模型。 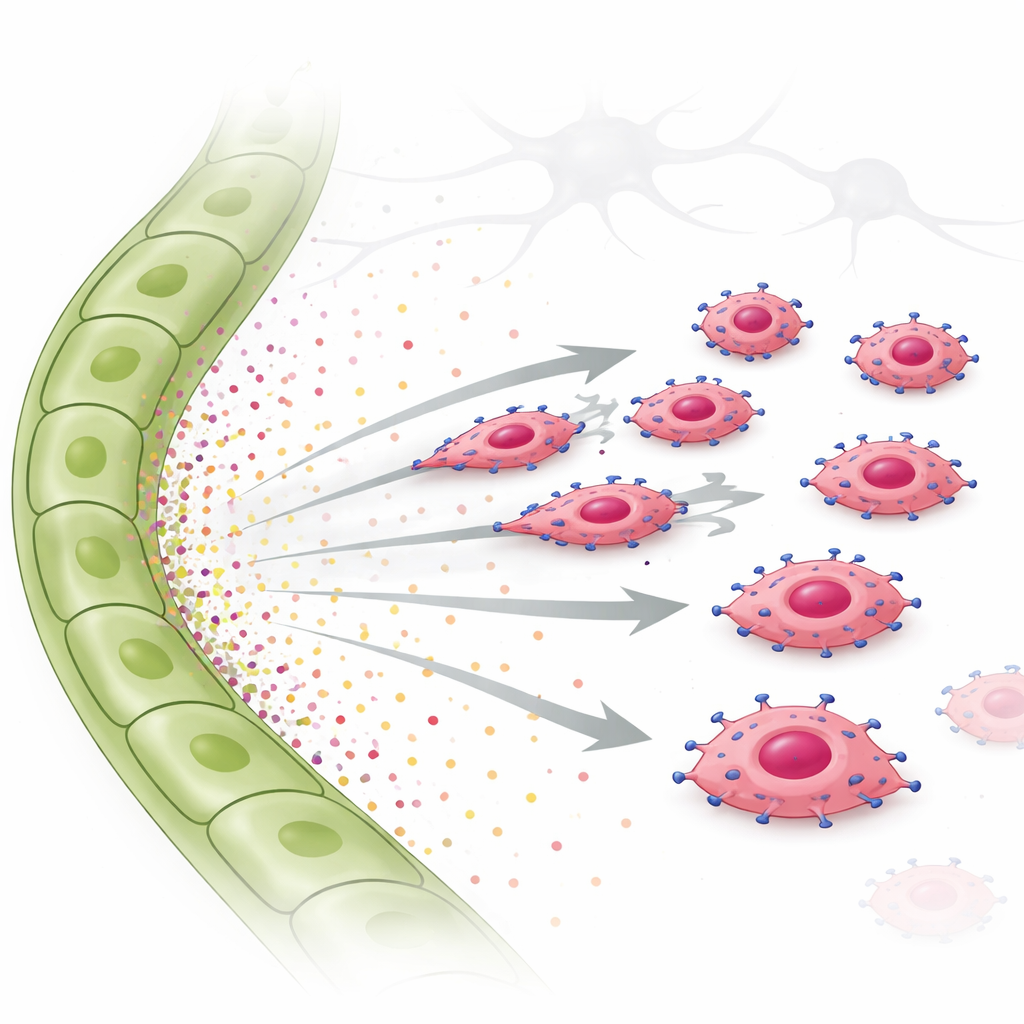
重新定位一种现有抗体
研究还探讨是否可以用药物打断这一引导系统。作者使用了 Fepixnebart,一种最初为中和 TGF-α 及相关因子在非肿瘤病症中开发的实验性抗体。在入侵实验中,该抗体显著降低了 EGFR 阳性细胞向淋巴来源液体移动的能力。在小鼠体内,当肿瘤细胞植入时给予单剂量处理,显著减少了后续在近旁淋巴结中发现的癌细胞数量,而对原发肿瘤大小没有影响。与此同时,高 EGFR 肿瘤的引流淋巴结中总体细胞数增加,但 CD8“杀伤”T 细胞相对不足且调节性 T 细胞增多,提示免疫环境向更抑制性方向转变,可能更有利于癌细胞定植。
对未来治疗的意义
综上所述,这项工作重新定义了三阴性乳腺癌中的 EGFR:它不仅仅是生长加速器,而是帮助肿瘤细胞感知并沿着淋巴管释放的 TGF-α 信号前进,将它们导入淋巴结,同时伴随可能有利于转移的免疫学改变。由于 Fepixnebart 及其他针对 EGFR 的药物已存在并在人体中进行了安全性测试,这一通路代表了一个“可重新定位”的治疗靶点。临床上或许不再单纯期望这些药物能够独自缩小已建立的肿瘤,而是将它们用于阻断早期的淋巴扩散并增强免疫疗法的效果,可能改变对高危乳腺癌的管理策略。
引用: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
关键词: 三阴性乳腺癌, 淋巴转移, EGFR 信号, TGF-α, 肿瘤免疫微环境