Clear Sky Science · it
La metastasi linfatica mediata da TGF-α/EGFR rivela un bersaglio terapeutico riposizionabile nel cancro al seno
Perché questo studio è importante per i pazienti
Quando il cancro al seno si diffonde oltre la ghiandola mammaria, spesso la prima comparsa è nei linfonodi. I medici sanno che i tumori con alti livelli di una proteina chiamata EGFR tendono a comportarsi in modo aggressivo, ma i farmaci che inibiscono EGFR non hanno dato buoni risultati nel cancro al seno. Questo studio mette in luce un pezzo mancante del puzzle: EGFR potrebbe non guidare principalmente la crescita tumorale, ma piuttosto aiutare le cellule tumorali a “navigare” verso i vasi linfatici e i linfonodi. Questo cambio di prospettiva potrebbe aprire la strada a nuovi modi per bloccare la metastasi in una fase precoce, prima che diventi pericolosa per la vita.
Un’autostrada nascosta per le cellule tumorali
I ricercatori si sono concentrati sul carcinoma mammario triplo negativo, un sottotipo difficile da trattare che spesso presenta alti livelli di EGFR e un coinvolgimento precoce dei linfonodi. In un modello murino hanno modificato le cellule tumorali in modo che sovrapproducessero EGFR e le hanno impiantate nella ghiandola mammaria. Sorprendentemente, questi tumori ricchi di EGFR non sono cresciuti più rapidamente e non hanno inviato più metastasi ai polmoni rispetto ai tumori di controllo. Al contrario, molte più cellule tumorali sono comparse nei linfonodi vicini, anche in tempi precoci. La microscopia ha mostrato che i vasi linfatici si trovavano per lo più intorno al margine esterno del tumore, suggerendo che le cellule tumorali devono muoversi attivamente verso l’esterno per trovare e entrare in questi vasi. 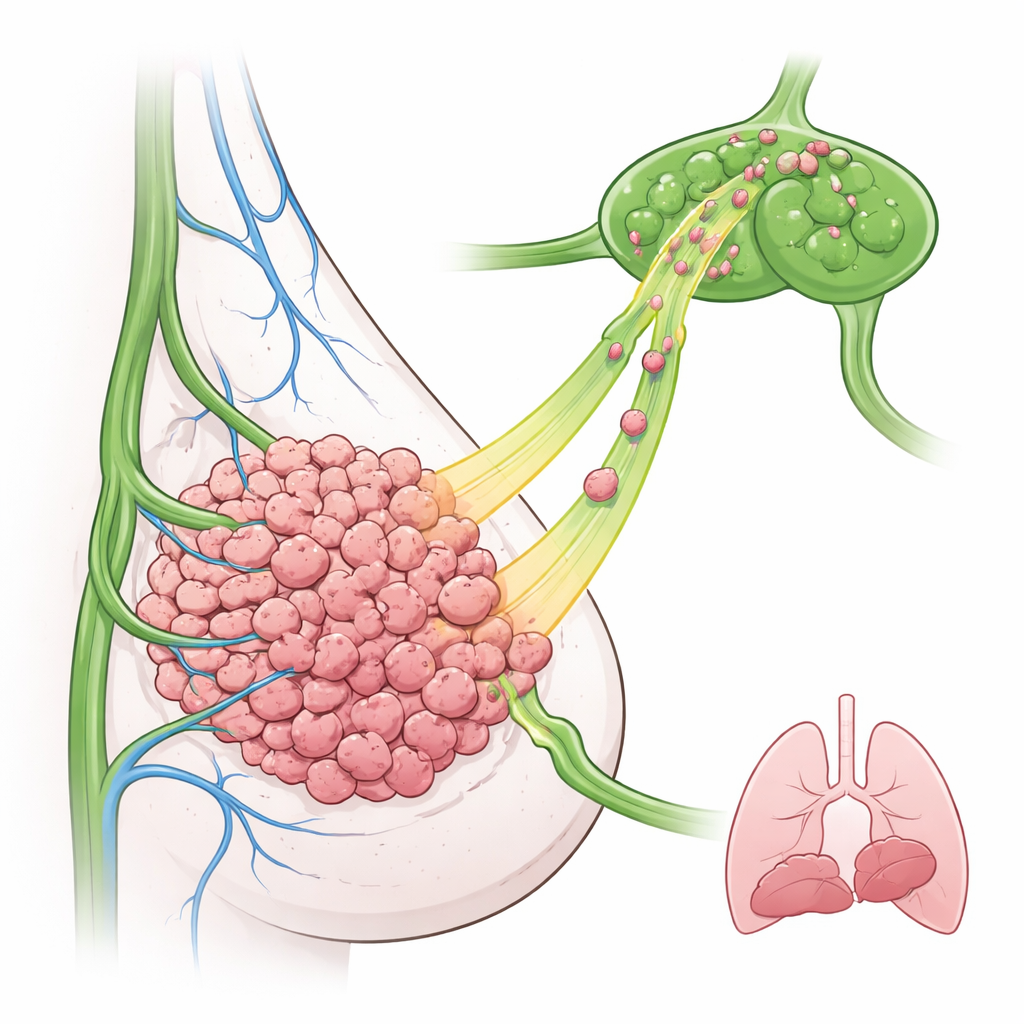
Segnali provenienti dagli stessi vasi linfatici
Il gruppo ha poi chiesto se i vasi linfatici siano semplici tubi passivi o guide attive. Hanno studiato le cellule endoteliali linfatiche, le cellule che rivestono i vasi linfatici, sia nei topi sia nei tumori mammari umani. Quando queste cellule sono state esposte a un’altra molecola legata al tumore, TGF-β, hanno iniziato a produrre fattori di crescita che possono attivare EGFR. Un fattore, TGF-α, è emerso come particolarmente rilevante: era fortemente aumentato, rilasciato nel fluido circostante e nei tessuti tumorali si concentrava sui vasi linfatici, non su quelli sanguigni. Dati umani hanno mostrato che i tumori al seno con livelli più alti di TGFA, specialmente il sottotipo basale correlato alla malattia triplo negativa, erano associati a peggiori esiti per i pazienti. Questo indica TGF-α come una probabile “scia olfattiva” che indirizza le cellule tumorali EGFR-positive verso i linfatici.
Come le cellule tumorali seguono la scia
Per verificare questa idea, i ricercatori hanno usato saggi di invasione e di migrazione cellulare in tempo reale. Hanno posto le cellule tumorali sovraespresse per EGFR sopra un gel e hanno messo sotto o il fluido delle cellule linfatiche o fattori di crescita purificati. Le cellule ricche di EGFR hanno mostrato una forte invasione verso il fluido delle cellule linfatiche e verso la sola TGF-α, muovendosi in modo chiaro e diretto anziché vagare casualmente. Un altro fattore, CTGF, più associato ai vasi sanguigni, non ha promosso un movimento direzionale e poteva persino attenuare l’effetto della TGF-α. All’interno delle cellule tumorali, la TGF-α ha attivato una molecola di segnalazione chiamata STAT3, insieme ad altre vie. Quando STAT3 è stato bloccato chimicamente, le cellule tumorali hanno in gran parte perso la capacità di muoversi verso i segnali linfatici. La stessa chemotassi guidata da TGF-α e dipendente da EGFR è stata osservata in una linea cellulare umana di carcinoma mammario triplo negativo, confermando che questo comportamento non è limitato ai topi. 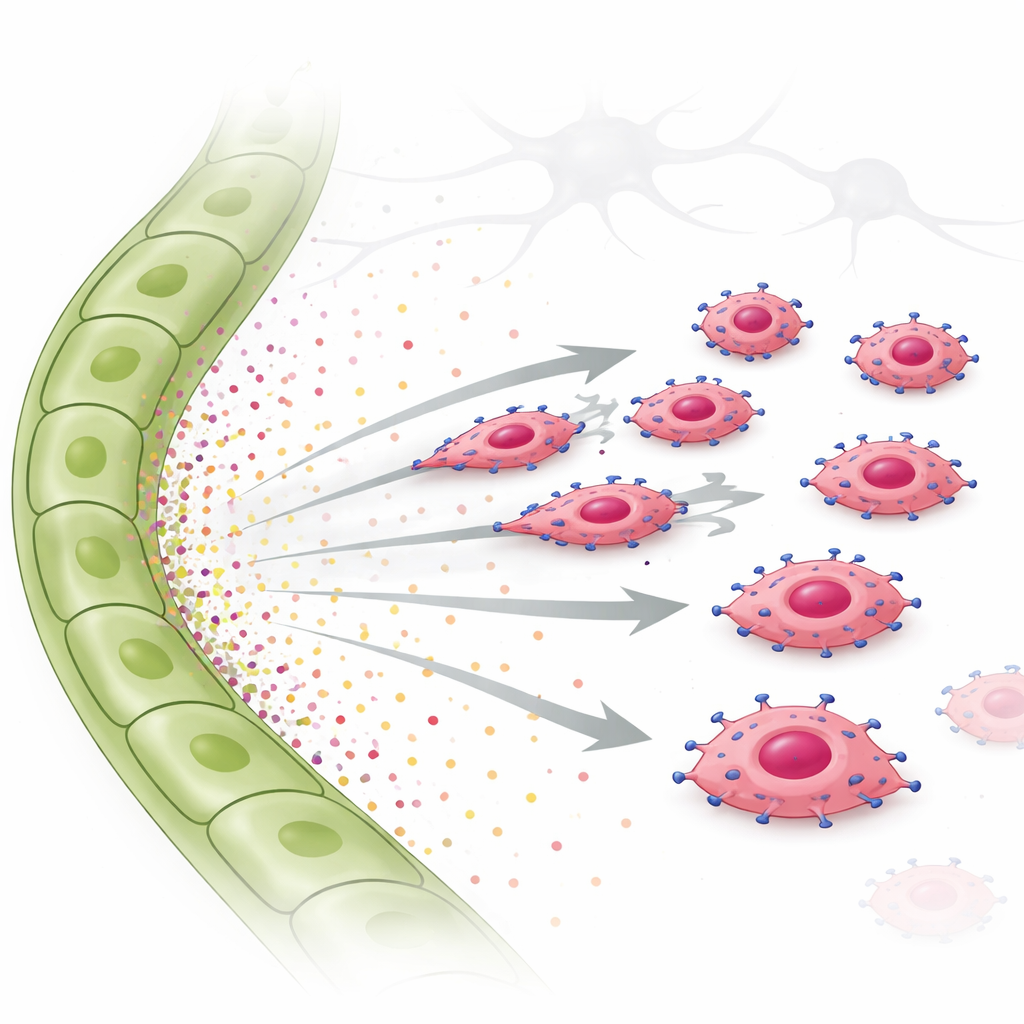
Riposizionare un anticorpo esistente
Lo studio ha inoltre esplorato se questo sistema di guida possa essere interrotto con un farmaco. Gli autori hanno usato Fepixnebart, un anticorpo di laboratorio sviluppato originariamente per neutralizzare TGF-α e un fattore correlato in condizioni non cancerose. Nei saggi di invasione, questo anticorpo ha ridotto nettamente la capacità delle cellule EGFR-positive di muoversi verso il fluido derivato dalle cellule linfatiche. Nei topi, una singola dose somministrata al momento dell’impianto delle cellule tumorali ha ridotto in modo significativo il numero di cellule tumorali rilevate più tardi nei linfonodi vicini, senza influire sulle dimensioni del tumore primario. Allo stesso tempo, i tumori con alto EGFR erano associati a linfonodi drenanti il tumore che contenevano un numero totale maggiore di cellule ma una carenza relativa di cellule T CD8 “killer” e un aumento delle cellule T regolatorie, suggerendo uno spostamento verso un ambiente immunitario più soppressivo in cui il cancro può insediarsi più facilmente.
Cosa significa per i trattamenti futuri
Complessivamente, il lavoro riformula il ruolo di EGFR nel carcinoma mammario triplo negativo: invece di essere semplicemente un acceleratore di crescita, EGFR aiuta le cellule tumorali a percepire e seguire un segnale di TGF-α emesso dai vasi linfatici, indirizzandole verso i linfonodi e accompagnando uno spostamento immunitario che può favorire la metastasi. Poiché Fepixnebart e altri agenti mirati a EGFR esistono già e sono stati testati per la sicurezza nell’uomo, questa via rappresenta un bersaglio terapeutico “riposizionabile”. Invece di aspettarsi che questi farmaci riducano da soli tumori già stabiliti, i clinici potrebbero un giorno usarli per bloccare la diffusione linfatica precoce e migliorare l’efficacia delle terapie basate sul sistema immunitario, cambiando potenzialmente la gestione dei tumori mammari ad alto rischio.
Citazione: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Parole chiave: cancro al seno triplo negativo, metastasi linfatica, segnalazione EGFR, TGF-alpha, microambiente immunitario tumorale