Clear Sky Science · sv
TGF-α/EGFR-medierad lymfatisk metastasering avslöjar ett omplaceringsbart terapeutiskt mål vid bröstcancer
Varför denna studie är viktig för patienter
När bröstcancer sprider sig bortom bröstet visar den sig ofta först i lymfkörtlarna. Läkare vet att tumörer med höga nivåer av ett protein kallat EGFR tenderar att vara mer aggressiva, men läkemedel som stänger av EGFR har inte fungerat väl mot bröstcancer. Denna studie identifierar en saknad pusselbit: EGFR driver kanske inte i första hand tumörtillväxt, utan hjälper istället tumörceller att ”leta sig fram” in i lymfkärl och lymfkörtlar. Denna förändrade syn kan öppna för nya sätt att stoppa metastasering tidigt, innan den blir livshotande.
En dold motorväg för tumörceller
Forskarna fokuserade på trippelnegativ bröstcancer, en svårbehandlad undergrupp som ofta har höga EGFR-nivåer och tidigt engagemang i lymfkörtlarna. I en musmodell modifierade de bröstcancerceller så att de överproducerade EGFR och implanterade dem i mjölkgången. Överraskande nog växte dessa EGFR-rika tumörer inte snabbare och spred sig inte mer till lungorna än kontrolltumörer. Istället påträffades betydligt fler cancerceller i närliggande lymfkörtlar, redan vid tidiga tidpunkter. Mikroskopi visade att lymfkärlen främst låg runt tumörens yttre kant, vilket tyder på att tumörcellerna måste röra sig aktivt utåt för att hitta och ta sig in i dessa kärl. 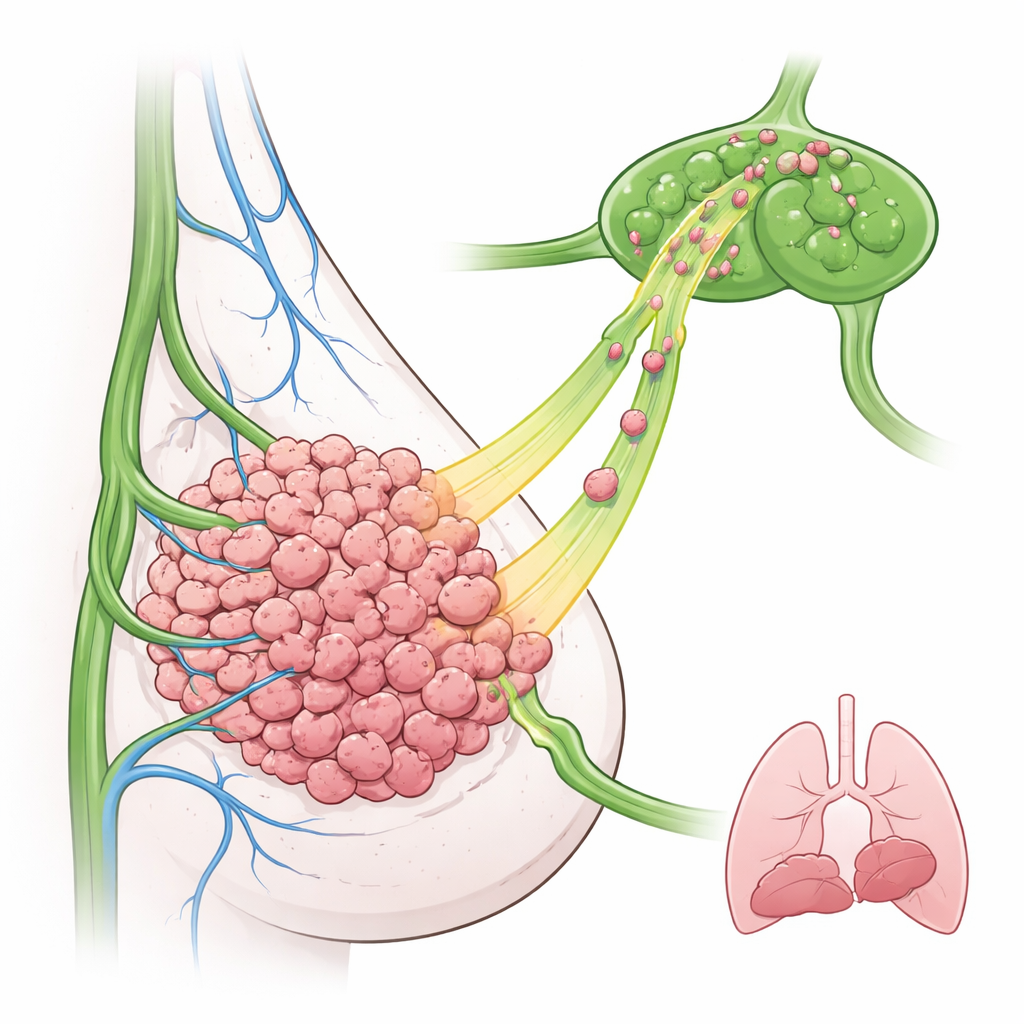
Signaler från lymfkärlen själva
Teamet frågade sedan om lymfkärlen bara är passiva rör eller aktiva vägvisare. De studerade lymfatisk endotelceller, cellerna som bekläder lymfkärl, både i möss och mänskliga brösttumörer. När dessa celler exponerades för en annan tumörrelaterad molekyl, TGF-β, började de producera tillväxtfaktorer som kan aktivera EGFR. En faktor, TGF-α, stack ut: den ökade kraftigt, släpptes ut i omgivande vätska och i tumörvävnad var den koncentrerad kring lymfkärl och inte blodkärl. Mänskliga data visade att bröstcancer med högre TGFA-nivåer, särskilt den basal-lika subtyp som är knuten till trippelnegativ sjukdom, var kopplad till sämre patientutfall. Detta pekade på TGF-α som en sannolik ”doftspår” som leder EGFR-positiva tumörceller in i lymfan.
Hur tumörceller följer spåret
För att testa idén använde forskarna invasion- och live-cell-migrationsassays. De placerade EGFR-överuttryckande tumörceller ovanpå en gel och tillförde antingen vätska från lymfatiska celler eller renade tillväxtfaktorer under gelén. De EGFR-rika cellerna invaderade starkt mot lymfatisk cellvätska och mot TGF-α ensam, och rörde sig på ett tydligt riktat sätt snarare än att vandra slumpmässigt. En annan faktor, CTGF, som är mer associerad med blodkärl, främjade inte riktad rörelse och kunde till och med dämpa TGF-α:s effekt. Inne i tumörcellerna aktiverade TGF-α ett signalsubstans kallat STAT3, tillsammans med andra vägar. När STAT3 kemiskt blockerades förlorade tumörcellerna i stort sett förmågan att röra sig mot lymfatiska signaler. Samma TGF-α-drivna, EGFR-beroende kemotaxi observerades i en mänsklig trippelnegativ bröstcancercellinje, vilket bekräftar att detta beteende inte är begränsat till möss. 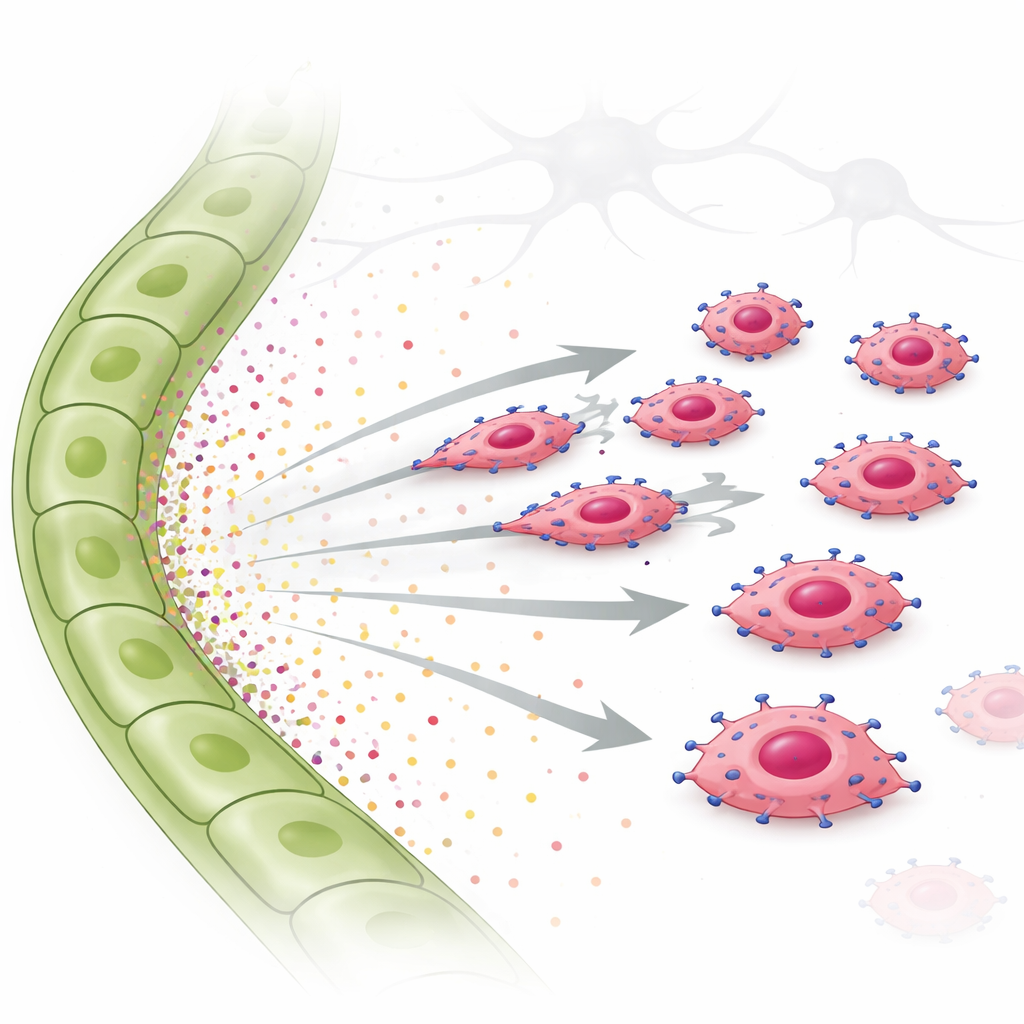
Omplacering av en befintlig antikropp
Studien undersökte också om detta vägvisningssystem kan avbrytas med ett läkemedel. Författarna använde Fepixnebart, en laboratorieantikropp ursprungligen utvecklad för att neutralisera TGF-α och en närbesläktad faktor vid icke-cancerrelaterade tillstånd. I invasionsassays minskade denna antikropp kraftigt EGFR-positiva cellers förmåga att röra sig mot lymfatisk härledd vätska. I möss gav en enda dos vid implantation av tumörceller en betydande minskning av antalet cancerceller som senare hittades i närliggande lymfkörtlar, utan att påverka primärtumörens storlek. Samtidigt associerades tumörer med hög EGFR med dränerande lymfkörtlar som innehöll fler totala celler men en relativ brist på CD8 "mördarceller" och en ökning av regulatoriska T‑celler, vilket tyder på en förskjutning mot en mer hämmande immunmiljö där cancer lättare kan få fäste.
Vad detta betyder för framtida behandling
Sammantaget omformulerar arbetet EGFR:s roll i trippelnegativ bröstcancer: snarare än att enbart vara en accelerant för tillväxt, hjälper EGFR tumörceller att uppfatta och följa en TGF-α-signal utsänd från lymfkärl, vilket styr dem in i lymfkörtlar och åtföljs av en immunförskjutning som kan gynna metastasering. Eftersom Fepixnebart och andra EGFR-riktade medel redan finns och har testats för säkerhet hos människor, utgör denna väg ett ”omplaceringsbart” terapeutiskt mål. Istället för att förvänta sig att dessa läkemedel själva ska krympa etablerade tumörer, kan kliniker en dag använda dem för att blockera tidig lymfatisk spridning och förbättra effekten av immunbaserade terapier, vilket potentiellt kan förändra hur högriskbröstcancer hanteras.
Citering: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Nyckelord: trippelnegativ bröstcancer, lymfatisk metastasering, EGFR-signalering, TGF-alfa, tumörens immunmikromiljö