Clear Sky Science · ru
Метастазирование в лимфатические узлы, опосредованное TGF-α/EGFR, выявляет перенаправляемую терапевтическую мишень при раке молочной железы
Почему это исследование важно для пациентов
Когда рак молочной железы выходит за пределы железы, он часто первым обнаруживается в лимфатических узлах. Врачи знают, что опухоли с высоким уровнем молекулы EGFR склонны к агрессивному течению, но препараты, блокирующие EGFR, не показали хорошей эффективности при раке молочной железы. В этом исследовании обнаружен недостающий элемент: EGFR может не столько стимулировать рост опухоли, сколько помогать опухолевым клеткам «ориентироваться» и проникать в лимфатические сосуды и узлы. Эта смена точки зрения может открыть новые пути для предотвращения метастазирования на ранних стадиях, до того как болезнь станет угрожающей жизни.
Скрытая «магистраль» для опухолевых клеток
Исследователи сосредоточились на тройном отрицательном раке молочной железы — трудно поддающемся лечению подтипе, который часто характеризуется высоким уровнем EGFR и ранним вовлечением лимфатических узлов. В модельных экспериментах на мышах они модифицировали опухолевые клетки так, чтобы те сверхэкспрессировали EGFR, и внедрили их в молочную железу. Удивительно, но такие опухоли с высоким EGFR не росли быстрее и не давали больше метастазов в легкие по сравнению с контролем. Вместо этого значительно больше клеток рака обнаруживалось в ближайших лимфатических узлах, даже на ранних этапах. Микроскопия показала, что лимфатические сосуды расположены преимущественно по периферии опухоли, что подразумевает необходимость активного движения опухолевых клеток наружу, чтобы найти и проникнуть в эти сосуды. 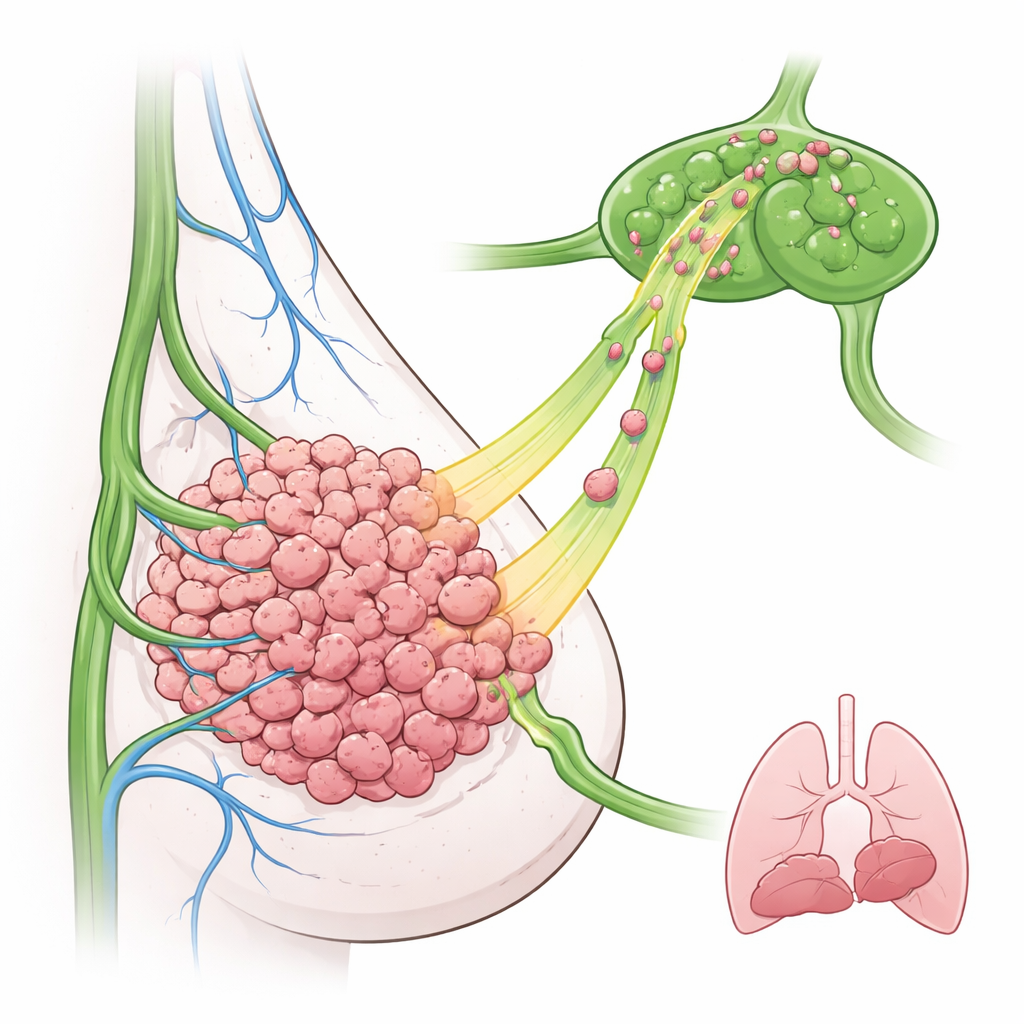
Сигналы от самих лимфатических сосудов
Дальше команда задалась вопросом: являются ли лимфатические сосуды пассивными трубами или активными ориентирами. Они изучали лимфатические эндотелиальные клетки — выстилку лимфатических сосудов — в образцах мышей и человеческих опухолях молочной железы. При воздействии другой опухолевой молекулы, TGF-β, эти клетки начали продуцировать факторы роста, способные активировать EGFR. Один фактор, TGF-α, выделялся особенно ярко: его уровень резко повышался, он выделялся в окружающую жидкость, а в тканях опухоли концентрировался на лимфатических, а не кровеносных сосудах. Данные от пациентов показали, что раки молочной железы с более высоким уровнем TGFA, особенно базальноподобный подтип, связанный с тройно‑отрицательной формой, ассоциируются с худшим прогнозом. Это указывало на TGF-α как на вероятный «обонятельный след», ведущий EGFR‑положительные опухолевые клетки в лимфатические сосуды.
Как опухолевые клетки следуют по следу
Чтобы проверить эту идею, исследователи использовали тесты инвазии и миграции живых клеток. Они размещали опухолевые клетки с высокой экспрессией EGFR над гелем и помещали либо жидкость от лимфатических клеток, либо очищенные факторы роста под ним. Клетки с высоким EGFR активно проникали в направлении жидкости от лимфатических клеток и в направлении чистого TGF-α, двигаясь законно направленно, а не беспорядочно. Другой фактор, CTGF, который больше ассоциируется с кровеносными сосудами, не вызывал направленного движения и даже мог ослаблять эффект TGF-α. Внутри опухолевых клеток TGF-α включал сигнальную молекулу STAT3 вместе с другими путями. При химической блокаде STAT3 клетки в значительной степени теряли способность двигаться к лимфатическим сигналам. Такая же хемо‑таксис, управляемая TGF-α и зависящая от EGFR, была показана и в человеческой клеточной линии тройного отрицательного рака молочной железы, что подтверждает, что это явление не ограничивается мышами. 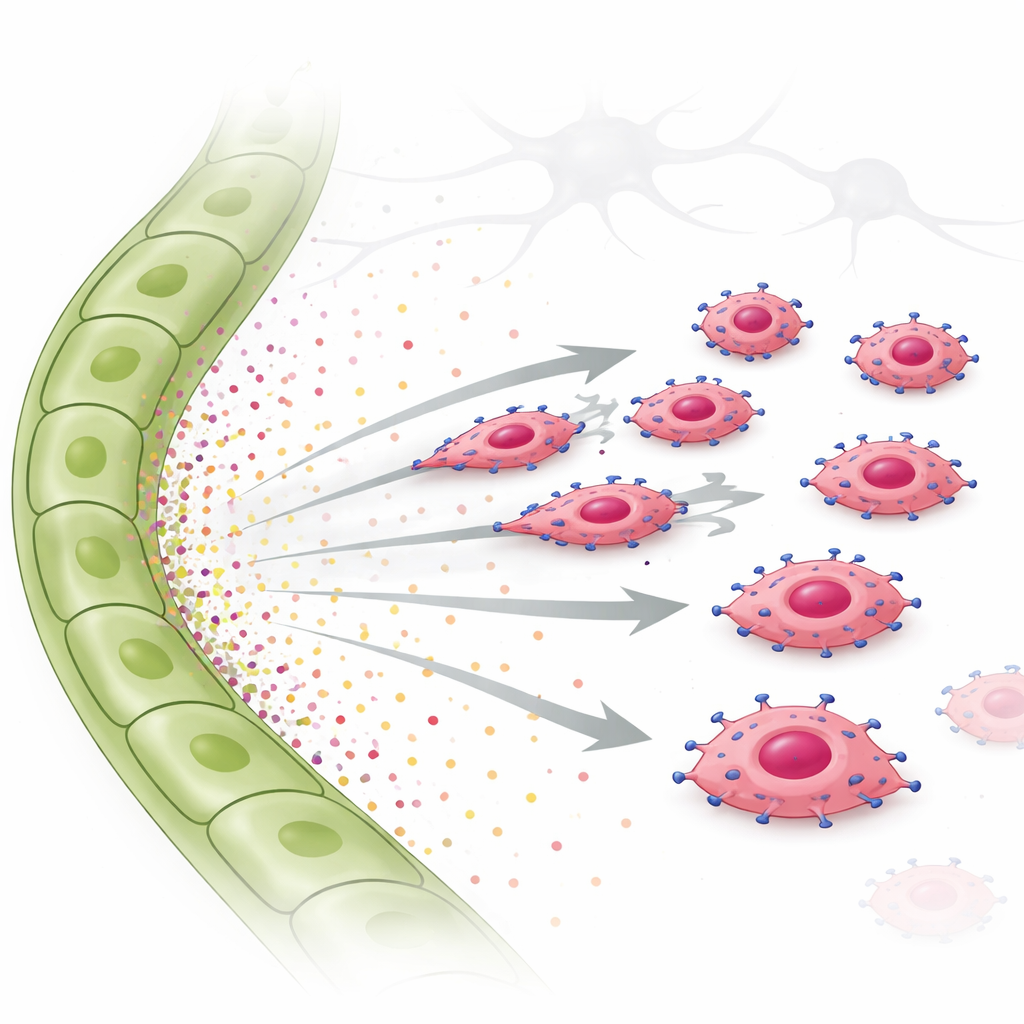
Перенаправление существующего антитела
Исследование также оценивало, можно ли прервать эту систему навигации с помощью лекарства. Авторы использовали Fepixnebart, лабораторное антитело, изначально разработанное для нейтрализации TGF-α и родственного фактора в неонкологических состояниях. В тестах инвазии это антитело заметно снижало способность EGFR‑положительных клеток двигаться в сторону жидкости, производимой лимфатическими клетками. У мышей однократная доза, введенная при имплантации опухолевых клеток, существенно уменьшала число раковых клеток, обнаруживаемых позже в ближайших лимфатических узлах, не влияя на размер первичной опухоли. При этом опухоли с высоким EGFR были связаны с лимфатическими узлами, дренирующими опухоль, в которых наблюдалось больше общего числа клеток, но относительный дефицит CD8 «киллерных» Т‑клеток и увеличение числа регуляторных Т‑клеток, что указывает на смещение в сторону более подавляющей иммунной среды, где рак легче приживается.
Что это значит для будущего лечения
В целом работа переосмысливает роль EGFR при тройном отрицательном раке молочной железы: вместо простой функции ускорителя роста EGFR помогает опухолевым клеткам распознавать и следовать за сигналом TGF-α, испускаемым лимфатическими сосудами, направляя их в лимфатические узлы и сопровождаясь иммунной перестройкой, которая может способствовать метастазированию. Поскольку Fepixnebart и другие препараты, нацеленные на EGFR, уже существуют и были протестированы на безопасность у людей, этот путь представляет собой «перенаправляемую» терапевтическую мишень. Вместо ожидания, что эти препараты сами по себе сократят уже сформированные опухоли, клиницисты в будущем могут использовать их для блокирования раннего лимфатического распространения и повышения эффективности иммунных терапий, что потенциально изменит подход к лечению пациентов с высоким риском при раке молочной железы.
Цитирование: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Ключевые слова: тройной отрицательный рак молочной железы, лимфатические метастазы, сигнальный путь EGFR, TGF-alpha, опухолевая иммунная микросреда