Clear Sky Science · nl
TGF-α/EGFR-gemedieerde lymfatische metastase onthult een herpositioneerbaar therapeutisch doelwit bij borstkanker
Waarom deze studie belangrijk is voor patiënten
Wanneer borstkanker zich buiten de borst verspreidt, verschijnt dat vaak eerst in de lymfeklieren. Artsen weten dat tumoren met hoge niveaus van een molecuul genaamd EGFR doorgaans agressief gedrag vertonen, maar geneesmiddelen die EGFR uitschakelen hebben bij borstkanker niet goed gewerkt. Deze studie onthult een ontbrekend puzzelstuk: EGFR drijft mogelijk niet primair de tumorgroei aan, maar helpt tumoren in plaats daarvan om zich te "navigeren" naar lymfatische vaten en lymfeklieren. Die verschuiving in perspectief kan de deur openen naar nieuwe manieren om metastase vroegtijdig te stoppen, voordat het levensbedreigend wordt.
Een verborgen snelweg voor tumorcellen
De onderzoekers richtten zich op triple-negatieve borstkanker, een moeilijk te behandelen subtype dat vaak hoge EGFR-niveaus en vroege betrokkenheid van lymfeklieren vertoont. In een muismodel pasten ze borstkankercellen aan zodat ze te veel EGFR produceerden en implanteren deze in de melkklier. Verrassend genoeg groeiden deze EGFR-rijke tumoren niet sneller en zonden ze niet meer uitzaaiingen naar de longen dan controletumoren. In plaats daarvan verschenen veel meer kankercellen in nabijgelegen lymfeklieren, zelfs op vroege tijdstippen. Microscopen toonden dat lymfatische vaten zich voornamelijk rond de buitenrand van de tumor bevonden, wat suggereert dat tumorcellen zich actief naar buiten moeten verplaatsen om deze vaten te vinden en binnen te dringen. 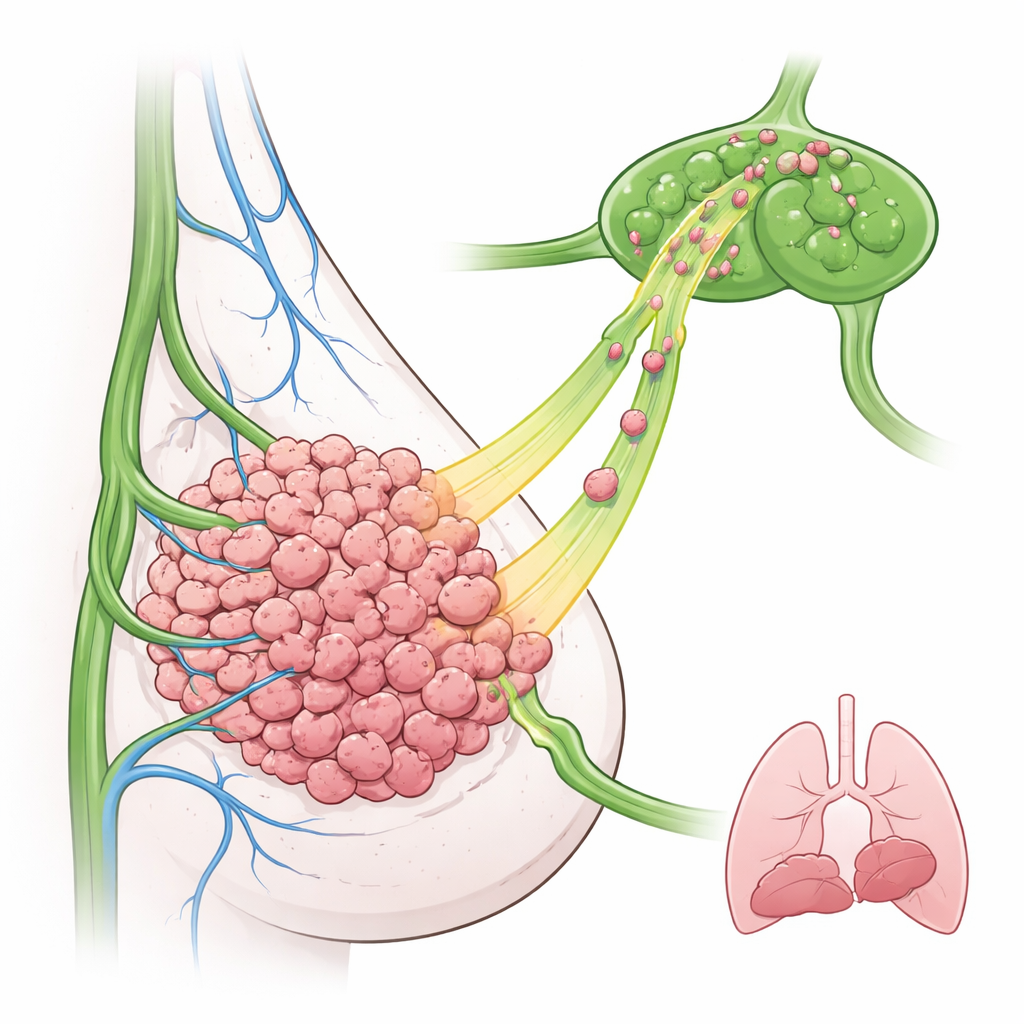
Signalen van de lymfevaten zelf
Het team vroeg zich vervolgens af of de lymfevaten slechts passieve leidingen zijn of actieve gidsen. Ze bestudeerden lymfe-endotheelcellen, de cellen die de lymfevaten bekleden, in zowel muizen als menselijke borsttumoren. Wanneer deze cellen werden blootgesteld aan een ander tumor-gerelateerd molecuul, TGF-β, begonnen ze groeifactoren te produceren die EGFR kunnen activeren. Eén factor, TGF-α, sprong eruit: die was sterk verhoogd, vrijgegeven in de omringende vloeistof en in tumorkweefsel geconcentreerd op lymfevaten, niet op bloedvaten. Gegevens van mensen lieten zien dat borsttumoren met hogere TGFA-niveaus, vooral het basaalachtige subtype gerelateerd aan triple-negatieve ziekte, geassocieerd waren met slechtere patiëntuitkomsten. Dit wees op TGF-α als een waarschijnlijke "geurspoor" die EGFR-positieve tumorcellen naar de lymfevaten leidt.
Hoe tumorcellen het spoor volgen
Om dit idee te testen gebruikten de onderzoekers invasie- en levende-cel migratie-assays. Ze plaatsten EGFR-overexpressie tumorcellen boven een gel en leverden ofwel vloeistof van lymfecellen of gezuiverde groeifactoren onderaan. De EGFR-rijke cellen vielen sterk aan richting vloeistof van lymfecellen en richting TGF-α alleen, en bewogen op een duidelijke, gerichte manier in plaats van willekeurig rond te zwerven. Een andere factor, CTGF, meer geassocieerd met bloedvaten, bevorderde geen gerichte beweging en kon zelfs het effect van TGF-α dempen. Binnenin de tumorcellen schakelde TGF-α een signaalmolecuul genaamd STAT3 in, samen met andere paden. Toen STAT3 chemisch werd geblokkeerd, verloren de tumorcellen grotendeels hun vermogen om naar lymfatische signalen te bewegen. Dezelfde door TGF-α gedreven, EGFR-afhankelijke chemotaxis werd waargenomen in een menselijke triple-negatieve borstkankercellijn, wat bevestigt dat dit gedrag zich niet beperkt tot muizen. 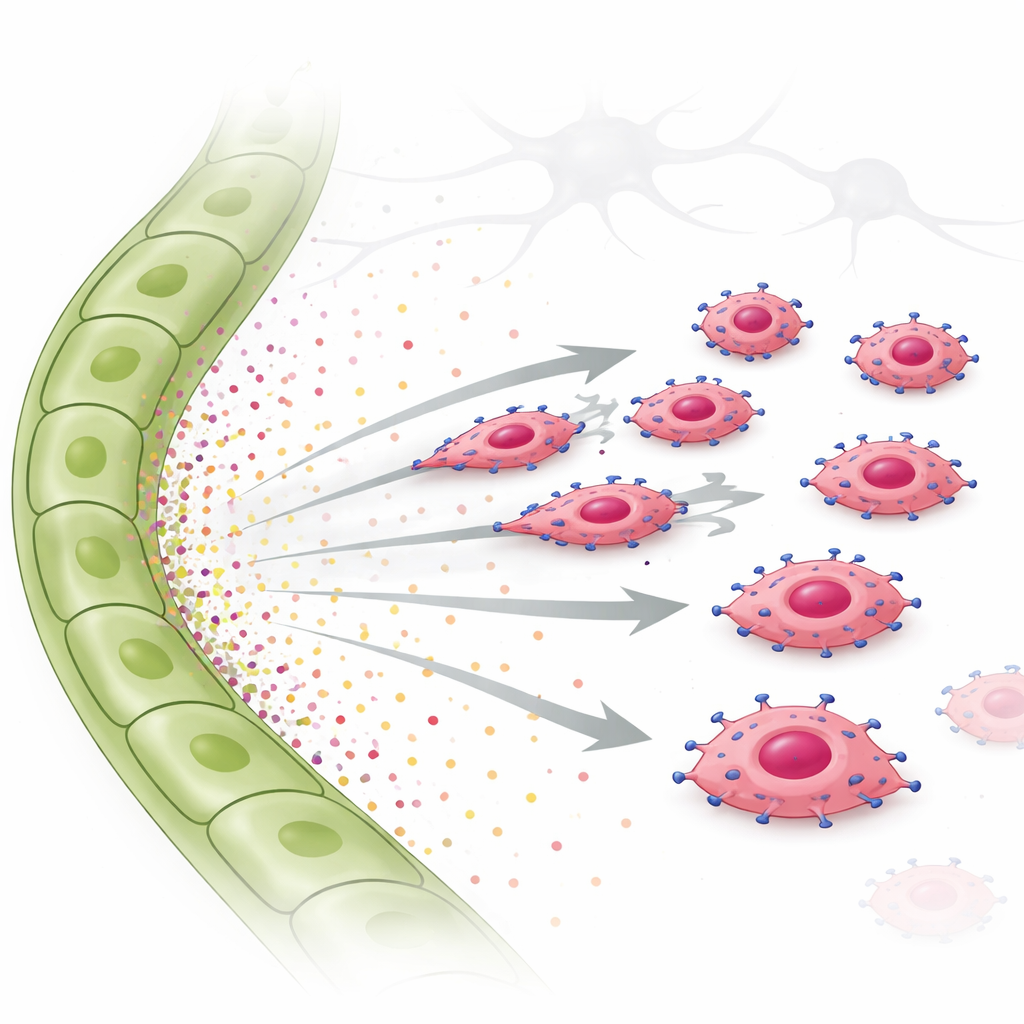
Herpositionering van een bestaand antilichaam
De studie onderzocht ook of dit geleidingssysteem kan worden onderbroken met een geneesmiddel. De auteurs gebruikten Fepixnebart, een laboratoriumantilichaam dat oorspronkelijk is ontwikkeld om TGF-α en een verwante factor te neutraliseren bij niet-kankerachtige aandoeningen. In invasieassays verminderde dit antilichaam scherp het vermogen van EGFR-positieve cellen om te bewegen naar door lymfe afgeleide vloeistof. Bij muizen leidde een enkele dosis gegeven op het moment van het implanteren van tumorcellen tot aanzienlijk minder kankercellen in latere nabijgelegen lymfeklieren, zonder de grootte van de primaire tumor te beïnvloeden. Tegelijkertijd waren tumoren met hoge EGFR-geassocieerd met tumor-drainerende lymfeklieren die meer totale cellen bevatten maar een relatieve tekort aan CD8 "killer" T-cellen en een toename van regulerende T-cellen, wat wijst op een verschuiving naar een meer onderdrukkende immuunomgeving waarin kanker zich gemakkelijker kan vestigen.
Wat dit betekent voor toekomstige behandeling
Samen nemen herformuleert dit werk de rol van EGFR bij triple-negatieve borstkanker: in plaats van simpelweg een groeiversneller te zijn, helpt EGFR tumorcellen een TGF-α-signaal dat door lymfevaten wordt uitgezonden te detecteren en te volgen, waardoor ze naar lymfeklieren worden gestuurd en dit gepaard gaat met een immuunverschuiving die metastase kan bevorderen. Omdat Fepixnebart en andere EGFR-gerichte middelen al bestaan en op veiligheid bij mensen zijn getest, vertegenwoordigt deze route een "herpositioneerbaar" therapeutisch doelwit. In plaats van te verwachten dat deze geneesmiddelen gevestigde tumoren op zichzelf laten krimpen, zouden clinici ze op een dag kunnen gebruiken om vroege lymfatische verspreiding te blokkeren en de effectiviteit van immuun-gebaseerde therapieën te verbeteren, mogelijk leidend tot een verandering in de behandeling van hoog-risico borstkankers.
Bronvermelding: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Trefwoorden: triple-negatieve borstkanker, lymfatische metastase, EGFR-signaaltransductie, TGF-alpha, tumor immuunmicro-omgeving