Clear Sky Science · pl
TGF-α/EGFR‑zależna przerzutowość do węzłów chłonnych ujawnia możliwy do repozycjonowania cel terapeutyczny w raku piersi
Dlaczego to badanie ma znaczenie dla pacjentów
Gdy rak piersi rozprzestrzenia się poza gruczoł, często jako pierwszy daje przerzuty do węzłów chłonnych. Lekarze wiedzą, że guzy z wysokim poziomem cząsteczki zwanej EGFR zwykle zachowują się agresywnie, ale leki blokujące EGFR nie sprawdziły się dobrze w raku piersi. To badanie odkrywa brakujący element układanki: EGFR może nie napędzać przede wszystkim wzrostu guza, lecz pomagać komórkom nowotworowym „nawigować” do naczyń limfatycznych i węzłów chłonnych. Ta zmiana perspektywy może otworzyć drogę do nowych sposobów powstrzymania przerzutów już na wczesnym etapie, zanim staną się zagrożeniem życia.
Ukryta autostrada dla komórek nowotworowych
Naukowcy skoncentrowali się na raku piersi potrójnie ujemnym, trudnym do leczenia podtypie, który często ma wysoki poziom EGFR i wczesne zajęcie węzłów chłonnych. W modelu myszy zmodyfikowali komórki raka piersi tak, by nadmiernie produkowały EGFR i wszczepili je do gruczołu mlekowego. Ku zaskoczeniu, guzy bogate w EGFR nie rosły szybciej i nie dawały więcej przerzutów do płuc niż guzy kontrolne. Zamiast tego znacznie więcej komórek nowotworowych pojawiło się w pobliskich węzłach chłonnych, nawet we wczesnych punktach czasowych. Mikroskopia wykazała, że naczynia limfatyczne leżały głównie wokół zewnętrznego obwodu guza, co sugeruje, że komórki muszą aktywnie przemieszczać się na zewnątrz, by je odnaleźć i wniknąć do nich. 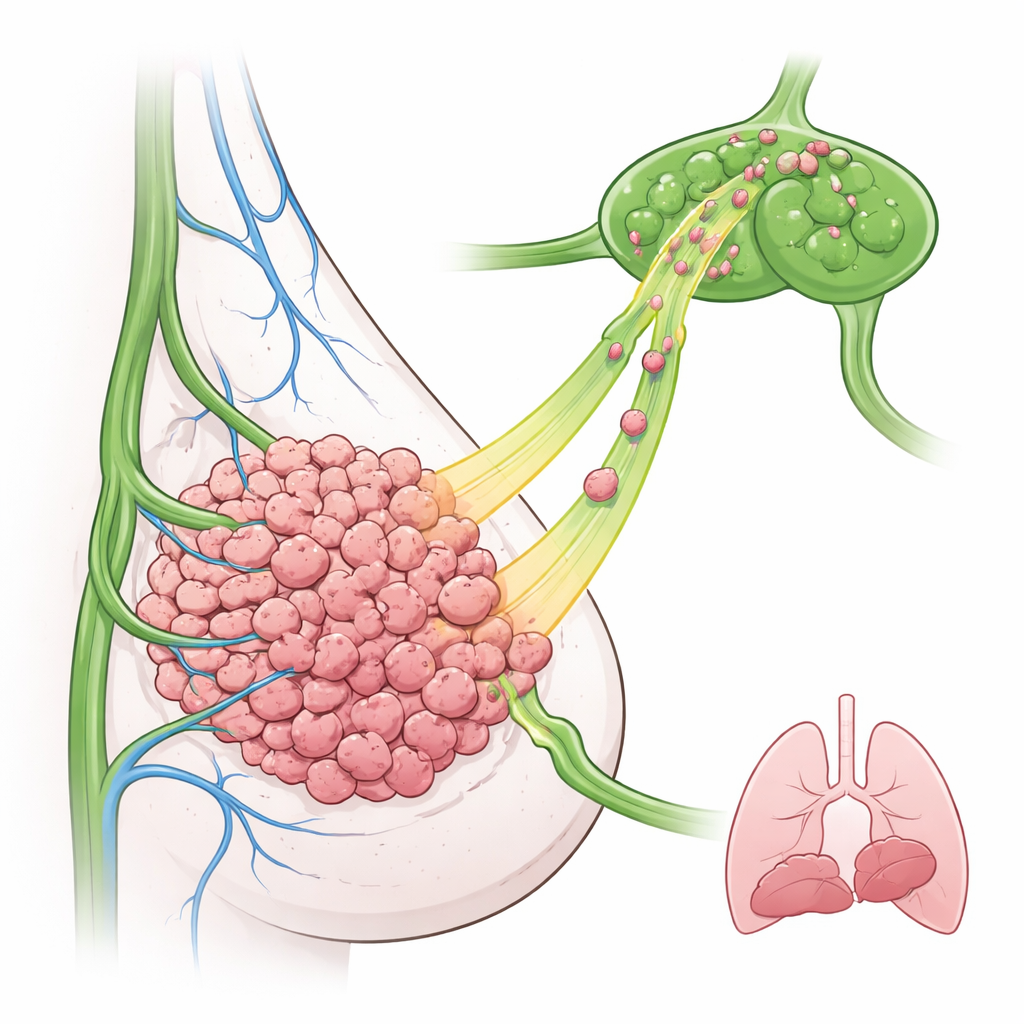
Sygnały pochodzące od samych naczyń limfatycznych
Zespół zapytał następnie, czy naczynia limfatyczne są jedynie biernymi rurami, czy też aktywnymi przewodnikami. Badali komórki śródbłonka limfatycznego — komórki wyściełające naczynia limfatyczne — zarówno u myszy, jak i w ludzkich guzach piersi. Gdy te komórki były eksponowane na inną cząsteczkę związaną z guzem, TGF‑β, zaczęły produkować czynniki wzrostu mogące aktywować EGFR. Jednym z nich wyróżniała się TGF‑α: była silnie zwiększona, uwalniana do otaczającego płynu, a w tkance guza skoncentrowana na naczyniach limfatycznych, nie na naczyniach krwionośnych. Dane z badań na ludziach pokazały, że raki piersi z wyższymi poziomami TGFA, szczególnie podtyp bazalny powiązany z chorobą potrójnie ujemną, korelowały z gorszymi wynikami u pacjentów. Wskazywało to na TGF‑α jako prawdopodobny „szlak zapachowy” prowadzący komórki EGFR‑dodatnie do limfatyki.
Jak komórki nowotworowe podążają za śladem
Aby przetestować ten pomysł, badacze wykorzystali testy inwazji i migracji komórek na żywo. Umieszczali komórki nadekspresyjne dla EGFR nad żelem i dostarczali poniżej albo płyn z komórek limfatycznych, albo oczyszczone czynniki wzrostu. Komórki bogate w EGFR silnie nacierały w stronę płynu z komórek limfatycznych i w stronę samego TGF‑α, poruszając się w wyraźnie ukierunkowany sposób, a nie w sposób przypadkowy. Inny czynnik, CTGF, bardziej związany z naczyniami krwionośnymi, nie sprzyjał ruchowi kierunkowemu, a nawet mógł osłabiać efekt TGF‑α. Wewnątrz komórek nowotworowych TGF‑α włączała białko sygnałowe STAT3 oraz inne szlaki. Gdy STAT3 został chemicznie zablokowany, komórki w dużej mierze traciły zdolność poruszania się w stronę sygnałów limfatycznych. Ten sam TGF‑α‑zależny, EGFR‑dependentny chemotaksję zaobserwowano w ludzkiej linii komórkowej raka piersi potrójnie ujemnego, potwierdzając, że to zachowanie nie ogranicza się do myszy. 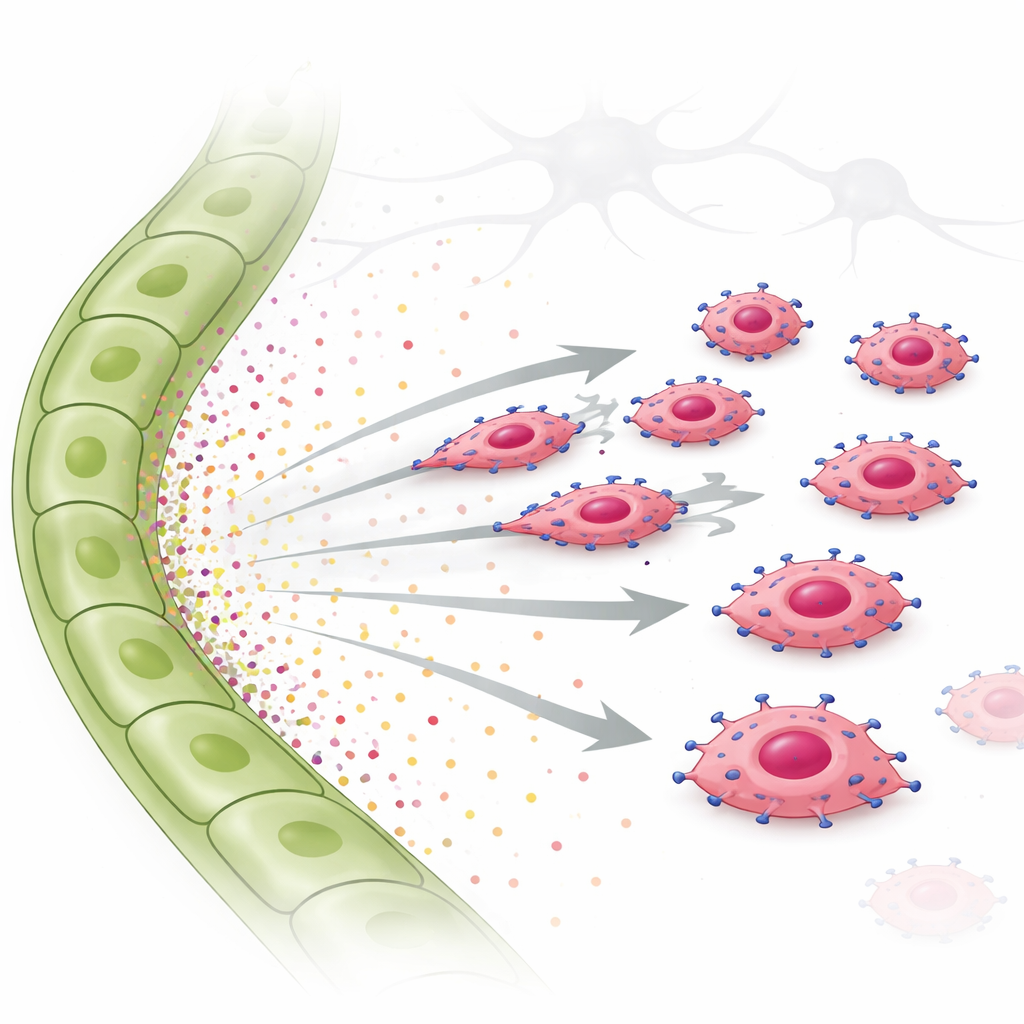
Repozycjonowanie istniejącego przeciwciała
Badanie sprawdziło też, czy ten system prowadzenia da się przerwać lekiem. Autorzy użyli Fepixnebartu, laboratoryjnego przeciwciała pierwotnie opracowanego do neutralizacji TGF‑α i pokrewnego czynnika w stanach niezwiązanych z rakiem. W testach inwazji to przeciwciało wyraźnie zmniejszyło zdolność komórek EGFR‑dodatnich do przemieszczania się w stronę płynu pochodzącego z komórek limfatycznych. U myszy pojedyncza dawka podana w momencie wszczepiania komórek nowotworowych znacząco obniżyła liczbę komórek raka później wykrywanych w pobliskich węzłach chłonnych, nie wpływając przy tym na rozmiar guza pierwotnego. Jednocześnie guzy o wysokim EGFR wiązały się z węzłami chłonnymi odprowadzającymi guz, które zawierały więcej komórek łącznie, ale względny niedobór komórek CD8 „zabójczych” oraz wzrost komórek regulatorowych T, co sugeruje przesunięcie w kierunku bardziej supresyjnego środowiska immunologicznego sprzyjającego osiedleniu się raka.
Co to oznacza dla przyszłego leczenia
W sumie praca przewartościowuje rolę EGFR w raku piersi potrójnie ujemnym: zamiast jedynie być akceleratorem wzrostu, EGFR pomaga komórkom nowotworowym wyczuwać i podążać za sygnałem TGF‑α emitowanym przez naczynia limfatyczne, kierując je do węzłów chłonnych i towarzysząc temu przesunięciu immunologicznemu, które może sprzyjać przerzutom. Ponieważ Fepixnebart i inne środki ukierunkowane na EGFR już istnieją i były badane pod kątem bezpieczeństwa u ludzi, ta ścieżka stanowi „repozycjonowalny” cel terapeutyczny. Zamiast oczekiwać, że te leki same w sobie znacząco skurczą ugruntowane guzy, klinicyści mogliby w przyszłości stosować je do blokowania wczesnego rozprzestrzeniania się limfatycznego i poprawy skuteczności terapii opartych na układzie odpornościowym, co potencjalnie zmieni sposób postępowania w przypadku pacjentek z wysokim ryzykiem raka piersi.
Cytowanie: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Słowa kluczowe: rak piersi potrójnie ujemny, przerzuty do węzłów chłonnych, sygnalizacja EGFR, TGF‑alpha, mikrośrodowisko immunologiczne guza