Clear Sky Science · ar
الانتقال اللمفي بوساطة TGF-α/EGFR يكشف هدفًا علاجيًا قابلاً لإعادة الاستخدام في سرطان الثدي
لماذا تهم هذه الدراسة المرضى
عندما ينتشر سرطان الثدي خارج الغدة الثديية، يظهر غالبًا أولاً في العقد اللمفاوية. الأطباء يعرفون أن الأورام التي تحتوي على مستويات عالية من جزيء يسمى EGFR تميل إلى التصرف بشكل عدائي، لكن الأدوية التي توقف EGFR لم تنجح جيدًا ضد سرطان الثدي. تكشف هذه الدراسة قطعة مفقودة من اللغز: قد لا يكون EGFR هو المحرك الرئيسي لنمو الورم، بل يساعد خلايا الورم على «التنقل» إلى داخل الأوعية اللمفاوية والعقد اللمفاوية. هذا التغير في وجهة النظر قد يفتح الباب لطرق جديدة لوقف النقائل مبكرًا قبل أن تصبح مهددة للحياة.
طريق خفي لخلايا الورم
ركز الباحثون على سرطان الثدي ثلاثي السلبية، وهو نوع صعب العلاج وغالبًا ما يملك مستويات عالية من EGFR وتورطًا مبكرًا للعقد اللمفاوية. في نموذج فأر، عدّلوا خلايا سرطان الثدي لإفراز EGFR بكميات زائدة وزرعوها في الغدة الثديية. ومن المدهش أن هذه الأورام الغنية بـEGFR لم تنم أسرع ولم ترسل نقاطًا انتكاسية أكثر إلى الرئتين مقارنة بالأورام الضابطة. بدلًا من ذلك، ظهرت خلايا سرطانية بمعدلات أعلى بكثير في العقد اللمفاوية القريبة، حتى في نقاط زمنية مبكرة. أظهرت المجاهر أن الأوعية اللمفاوية كانت غالبًا محاطة بحافة خارجية للورم، مما يوحي بأن خلايا الورم يجب أن تتحرك فعليًا إلى الخارج لتجد هذه الأوعية وتدخلها. 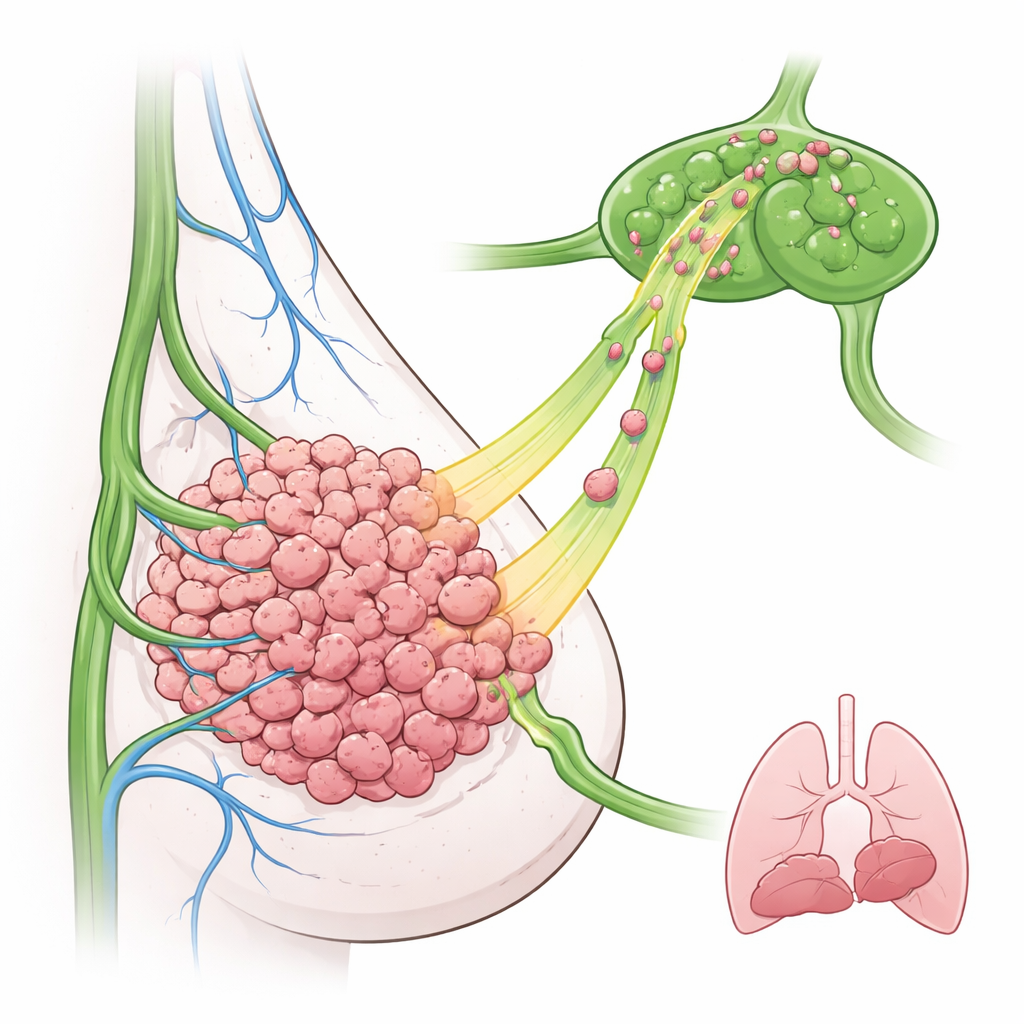
إشارات من الأوعية اللمفاوية نفسها
سأل الفريق بعد ذلك ما إذا كانت الأوعية اللمفاوية مجرد أنابيب سلبية أم دلائل نشطة. درسوا خلايا البطانة اللمفاوية، خلايا التي تبطن الأوعية اللمفاوية، في كل من الفئران وأورام الثدي البشرية. عندما تعرضت هذه الخلايا لجزيء مرتبط بالأورام آخر، TGF-β، بدأت تنتج عوامل نمو يمكنها تنشيط EGFR. برز عامل واحد، TGF-α: فقد زاد بقوة، وأُفرج عنه في السوائل المحيطة، وفي نسيج الورم كان مركزًا على الأوعية اللمفاوية لا الأوعية الدموية. أظهرت بيانات بشرية أن سرطانات الثدي ذات مستويات أعلى من TGFA، خصوصًا النوع القاعدي المرتبط بثلاثي السلبية، كانت مرتبطة بنتائج أسوأ للمرضى. هذا أشار إلى TGF-α كـ«أثر عطري» محتمل يقود الخلايا الموجبة لـEGFR نحو الأجهزة اللمفاوية.
كيف تتبع خلايا الورم الأثر
لاختبار هذه الفكرة، استخدم الباحثون تجارب غزو وهجرة الخلايا الحية. وضعوا خلايا ورمية مفرطة التعبير لـEGFR فوق هلام وموّدوا إما بسائل من خلايا لمفاوية أو بعوامل نمو مكررة في الأسفل. غزت الخلايا الغنية بـEGFR بقوة نحو سائل الخلايا اللمفاوية ونحو TGF-α وحده، متحركة بشكل واضح وموجه بدلاً من الترحال العشوائي. عامل آخر، CTGF، المرتبط أكثر بالأوعية الدموية، لم يعزز الحركة التوجيهية وقد يضعف حتى تأثير TGF-α. داخل خلايا الورم، شغّل TGF-α جزيء إشارة يسمى STAT3، إلى جانب مسارات أخرى. عندما تم حجب STAT3 كيميائيًا، فقدت خلايا الورم إلى حد كبير قدرتها على الحركة نحو إشارات اللمف. لوحظت نفس الحركة الكيميائية الموجهة بواسطة TGF-α والمعتمدة على EGFR في سطر خلوي بشري من سرطان الثدي ثلاثي السلبية، مؤكدين أن هذا السلوك ليس مقصورًا على الفئران. 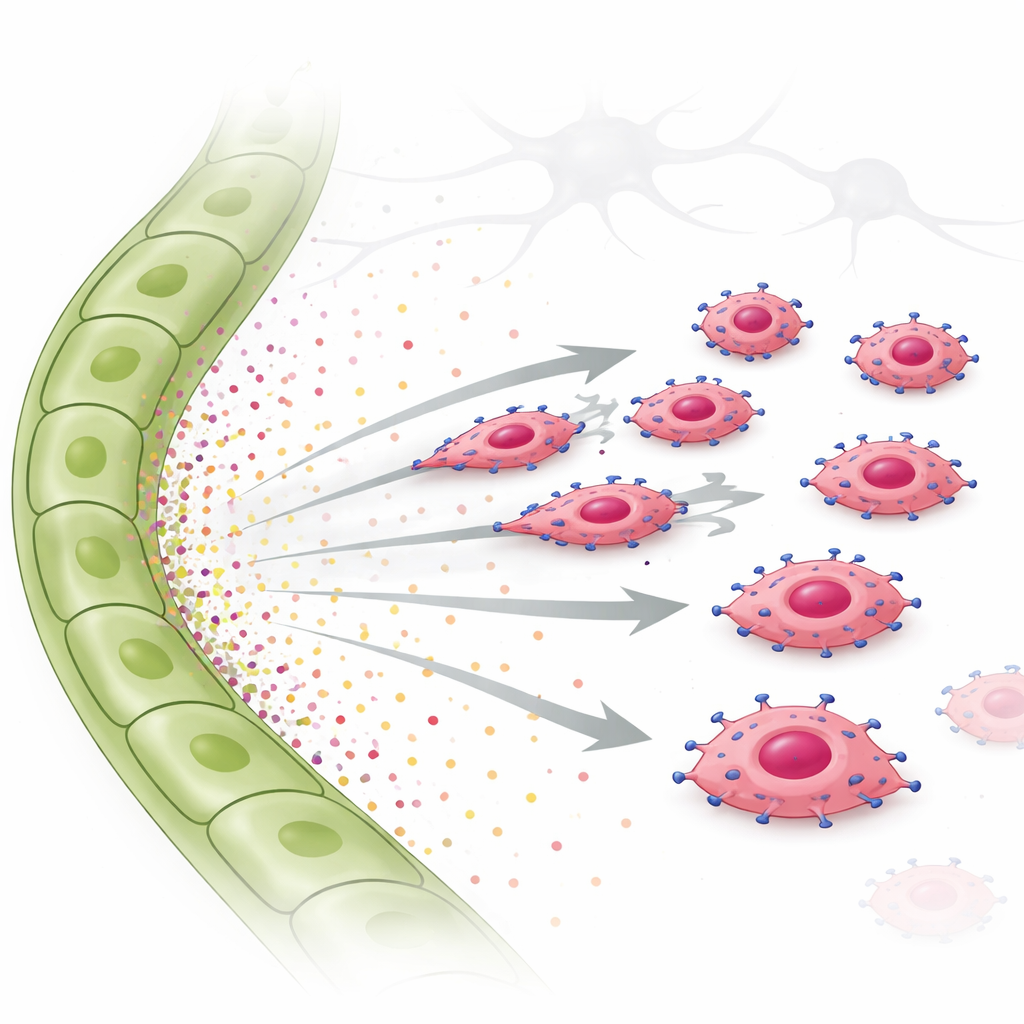
إعادة توظيف جسم مضاد موجود
استكشفت الدراسة أيضًا ما إذا كان يمكن قطع نظام الإرشاد هذا بدواء. استخدم المؤلفون Fepixnebart، جسمًا مضادًا مخبريًا طور في الأصل لتحييد TGF-α وعامل ذي صلة في حالات غير سرطانية. في تجارب الغزو، قلل هذا الجسم المضاد بشكل حاد قدرة الخلايا الموجبة لـEGFR على الحركة صوب سائل مشتق من الخلايا اللمفاوية. في الفئران، جرعة واحدة أعطيت عند زرع خلايا الورم خفضت بشكل ملحوظ عدد الخلايا السرطانية التي وُجدت لاحقًا في العقد اللمفاوية القريبة، دون التأثير على حجم الورم الأولي. في الوقت نفسه، ارتبطت الأورام ذات EGFR المرتفع بعقد لمفاوية مصرفة للورم تحتوي على عدد إجمالي أكبر من الخلايا لكن بنقص نسبي في الخلايا T القاتلة CD8 وزيادة في الخلايا التسيطرية، مشيرة إلى تحول نحو بيئة مناعية أكثر قمعًا حيث يمكن للسرطان أن يستقر بسهولة أكبر.
ماذا يعني هذا لعلاج المستقبل
تجميعًا، تعيد هذه الدراسة تأطير دور EGFR في سرطان الثدي ثلاثي السلبية: بدلاً من كونه مجرد مسرع للنمو، يساعد EGFR خلايا الورم على استشعار واتباع إشارة TGF-α المنبعثة من الأوعية اللمفاوية، موجهًا إياها إلى العقد اللمفاوية ومصحوبًا بتحول مناعي قد يفضّل النقائل. وبما أن Fepixnebart وعوامل مستهدفة لـEGFR أخرى موجودة بالفعل وقد خضعت لاختبارات أمان في البشر، فإن هذا المسار يمثل هدفًا علاجيًا «قابلًا لإعادة الاستخدام». بدلًا من توقع أن تُقلص هذه الأدوية الأورام المستقرة بمفردها، قد يستخدمها الأطباء يومًا ما لوقف الانتشار اللمفي المبكر وتحسين فاعلية العلاجات المناعية، مما قد يغير طريقة إدارة سرطانات الثدي عالية الخطورة.
الاستشهاد: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبية, الانتقال اللمفي, إشارة EGFR, TGF-alpha, البيئة المناعية المحيطة بالورم