Clear Sky Science · de
TGF-α/EGFR-vermittelte lymphatische Metastasierung zeigt ein umnutzbares therapeutisches Ziel bei Brustkrebs
Warum diese Studie für Patientinnen und Patienten wichtig ist
Wenn Brustkrebs über die Brust hinausstreut, zeigt sich das oft zunächst in den Lymphknoten. Ärztinnen und Ärzte wissen, dass Tumoren mit hohen Mengen eines Moleküls namens EGFR tendenziell aggressiv sind, doch Wirkstoffe, die EGFR blockieren, haben bei Brustkrebs nur begrenzt Erfolg gezeigt. Diese Studie liefert ein fehlendes Puzzleteil: EGFR treibt möglicherweise nicht primär das Tumorwachstum, sondern hilft den Tumorzellen vielmehr dabei, in Lymphgefäße und Lymphknoten „einzunavigieren“. Diese Verschiebung der Perspektive könnte neue Wege eröffnen, Metastasen früh zu stoppen, bevor sie lebensbedrohlich werden.
Eine verborgene Autobahn für Tumorzellen
Die Forscher konzentrierten sich auf den dreifach-negativen Brustkrebs, einen schwer zu behandelnden Subtyp, der häufig hohe EGFR-Werte und frühe Lymphknotenbeteiligung aufweist. In einem Mausmodell konstruierten sie Brustkrebszellen, die EGFR überproduzieren, und implantierten sie in die Brustdrüse. Überraschenderweise wuchsen diese EGFR-reichen Tumoren nicht schneller und verursachten auch nicht mehr Lungenmetastasen als Kontrolltumoren. Stattdessen fanden sich deutlich mehr Krebszellen in benachbarten Lymphknoten, selbst zu frühen Zeitpunkten. Die Mikroskopie zeigte, dass sich Lymphgefäße überwiegend am äußeren Rand des Tumors befanden, was darauf hindeutet, dass Tumorzellen aktiv nach außen wandern müssen, um diese Gefäße zu finden und zu betreten. 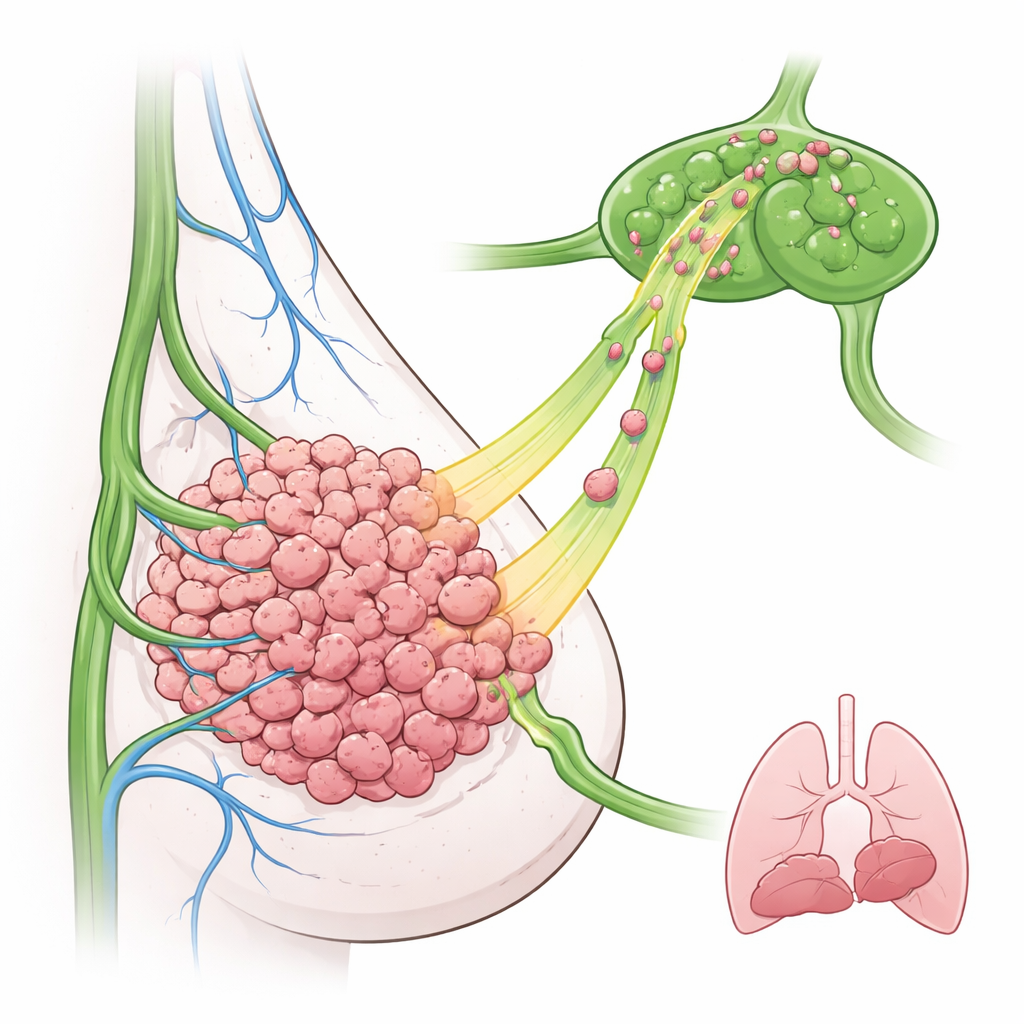
Signale aus den Lymphgefäßen selbst
Das Team fragte sich dann, ob Lymphgefäße bloß passive Rohre oder aktive Wegweiser sind. Sie untersuchten lymphatische Endothelzellen, die die Lymphgefäße auskleiden, sowohl in Mäusen als auch in menschlichen Brusttumoren. Wenn diese Zellen einem weiteren tumorrelevanten Molekül, TGF-β, ausgesetzt wurden, begannen sie, Wachstumsfaktoren zu produzieren, die EGFR aktivieren können. Ein Faktor stach heraus: TGF-α – es war stark erhöht, wurde in die umgebende Flüssigkeit freigesetzt und im Tumorgewebe vor allem an lymphatischen, nicht an Blutgefäßen angereichert. Menschliche Daten zeigten, dass Brustkrebserkrankungen mit höheren TGFA-Spiegeln, insbesondere der basal-ähnliche Subtyp, der mit dreifach-negativer Erkrankung verwandt ist, mit schlechteren Patientenergebnissen assoziiert waren. Das deutet darauf hin, dass TGF-α eine wahrscheinliche „Duftspur“ ist, die EGFR-positive Tumorzellen in die Lymphgefäße leitet.
Wie Tumorzellen der Spur folgen
Um diese Idee zu testen, nutzten die Forscher Invasions- und Live-Zell-Migrationsassays. Sie platzierten EGFR-überexprimierende Tumorzellen über einem Gel und gaben entweder Flüssigkeit aus lymphatischen Zellen oder gereinigte Wachstumsfaktoren darunter. Die EGFR-reichen Zellen drangen stark zur lymphatischen Zellflüssigkeit und zu TGF-α allein hin ein und bewegten sich klar gerichtet statt zufällig umher. Ein anderer Faktor, CTGF, der eher mit Blutgefäßen assoziiert ist, förderte keine gerichtete Bewegung und konnte sogar die Wirkung von TGF-α abschwächen. Innerhalb der Tumorzellen schaltete TGF-α ein Signalmolekül namens STAT3 sowie andere Signalwege ein. Als STAT3 chemisch blockiert wurde, verloren die Tumorzellen weitgehend ihre Fähigkeit, sich zu lymphatischen Signalen zu bewegen. Dieselbe TGF-α-getriebene, EGFR-abhängige Chemotaxis wurde in einer menschlichen Zelllinie des dreifach-negativen Brustkrebses beobachtet, was bestätigt, dass dieses Verhalten nicht auf Mäuse beschränkt ist. 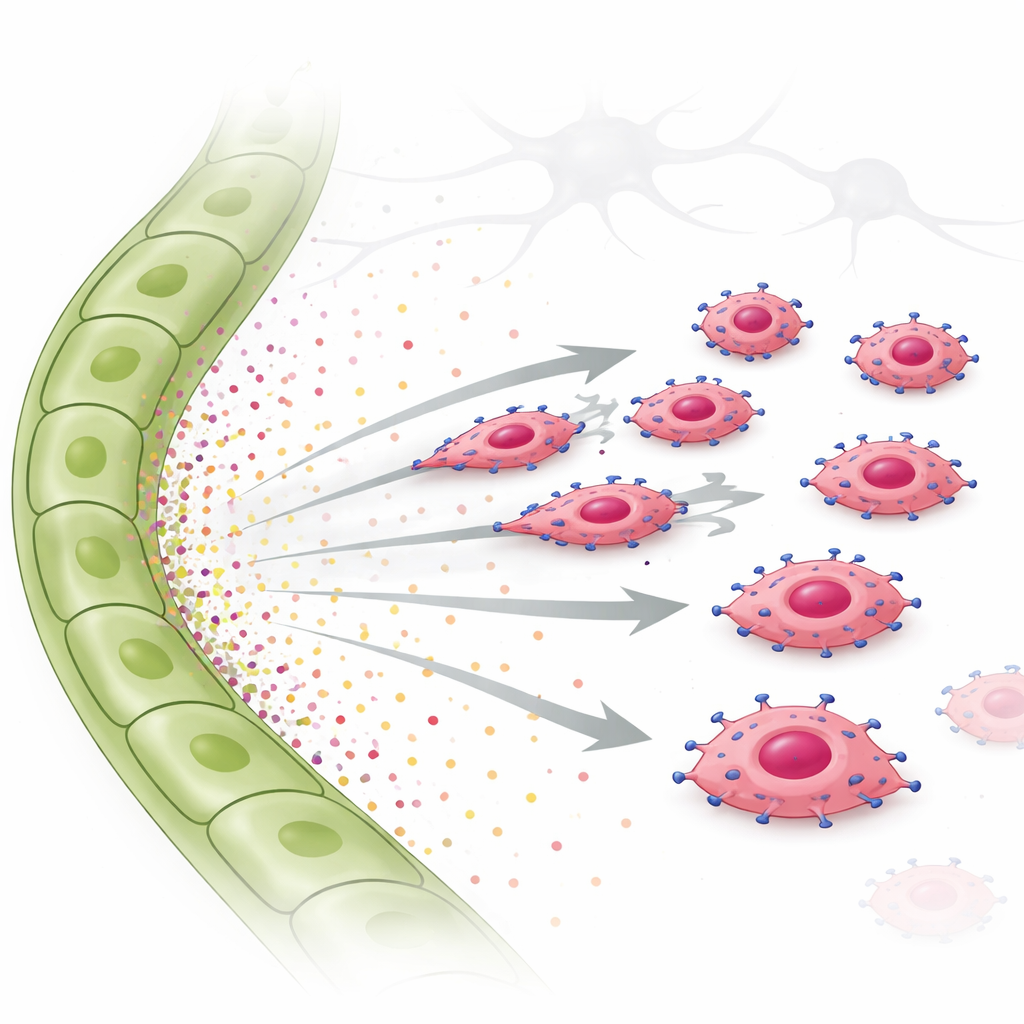
Umunutzung eines vorhandenen Antikörpers
Die Studie prüfte auch, ob sich dieses Orientierungssystem pharmakologisch unterbrechen lässt. Die Autorinnen und Autoren verwendeten Fepixnebart, einen im Labor entwickelten Antikörper, der ursprünglich zur Neutralisierung von TGF-α und einem verwandten Faktor bei nichtonkologischen Erkrankungen gedacht war. In Invasionsassays reduzierte dieser Antikörper die Fähigkeit von EGFR-positiven Zellen, sich zur lymphatisch abgeleiteten Flüssigkeit zu bewegen, deutlich. In Mäusen führte eine einzelne Dosis zum Zeitpunkt der Tumorimplantation zu einer signifikanten Verringerung der später in den benachbarten Lymphknoten nachweisbaren Krebszellen, ohne die Größe des Primärtumors zu beeinflussen. Gleichzeitig waren Tumoren mit hohem EGFR mit tumor-drainierenden Lymphknoten assoziiert, die zwar mehr Gesamtzellen enthielten, jedoch relativ weniger CD8-“Killer”-T-Zellen und eine Zunahme regulatorischer T-Zellen aufwiesen, was auf eine Verschiebung hin zu einem stärker unterdrückenden Immunumfeld hindeutet, in dem sich Krebs leichter etablieren kann.
Was das für zukünftige Behandlungen bedeutet
Zusammengefasst stellt die Arbeit EGFR beim dreifach-negativen Brustkrebs neu dar: Statt lediglich ein Wachstumsbeschleuniger zu sein, hilft EGFR Tumorzellen, ein von Lymphgefäßen ausgesendetes TGF-α-Signal zu erkennen und zu verfolgen, lenkt sie in Lymphknoten und geht mit einer Immunverschiebung einher, die Metastasen begünstigen kann. Da Fepixnebart und andere EGFR-gezielte Wirkstoffe bereits existieren und in Menschen auf Sicherheit geprüft wurden, stellt dieser Weg ein „umnutzbares“ therapeutisches Ziel dar. Anstatt zu erwarten, dass diese Medikamente etablierte Tumoren allein verkleinern, könnten sie eines Tages eingesetzt werden, um frühe lymphatische Ausbreitung zu blockieren und die Wirksamkeit immunbasierter Therapien zu verbessern – und damit die Behandlung von Hochrisiko-Brustkrebserkrankungen zu verändern.
Zitation: Shi, W., Pan, Y., Rathod, B. et al. TGF-α/EGFR-mediated lymphatic metastasis reveals a repositionable therapeutic target in breast cancer. npj Breast Cancer 12, 52 (2026). https://doi.org/10.1038/s41523-026-00941-0
Schlüsselwörter: dreifach-negativer Brustkrebs, lymphatische Metastasierung, EGFR-Signalgebung, TGF-alpha, tumorales Immunmikromilieu